为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。
试填空。
(1)D装置中主要反应的离子方程式为 ,
F仪器的作用是: 。
(2)为验证通入D装置中气体是Cl2还是SO2过量,兴趣小组的同学准备了以下试剂: ① 氯化铁稀溶液 ② 氯化亚铁溶液 ③ 硫氰化钾溶液
① 氯化铁稀溶液 ② 氯化亚铁溶液 ③ 硫氰化钾溶液
④ 苯酚溶液 ⑤ 品红溶液 ⑥ 酸性高锰酸钾溶液
若Cl2过量:取适量D中溶液滴加至盛有 (选填一个序号)试剂的试管内,再加入 (选填一个序号)试剂,发生的现象是: ;
若SO2过量:取适量D中溶液滴加至盛有 (选填一个序号)试剂的试管内,发生的现象是: 。
实验室利用下图所示装置制取乙酸乙酯。请回答: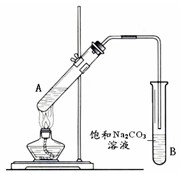
(1)试管A中盛放的试剂为乙酸、 和浓硫酸,它们之间发生反应生成乙酸乙酯的化学方程式为 。
(2)加热一段时间后,可观察到B试管中液面上有无色油状液体生成。B试管中的导管不伸入液面下的原因是 (填序号)。
①防止溶液倒吸 ②避免反应过快
某同学为探究碳酸钠的性质,进行了如下实验,请你按要求回答有关问题。
(1)配制100 mL 0.5 mol/L的Na2CO3溶液。该同学先用天平称量Na2CO3固体的质量,然后配制该溶液,要用到的玻璃仪器有量筒、烧杯、 、 。
(2)用pH试纸测所配溶液的pH,pH>7,说明Na2CO3溶液呈 (填“酸性”、“碱性”或“中性”);用试管取少量所配溶液,向溶液中滴加几滴酚酞试液,溶液变红,再用酒精灯加热,溶液的颜色变深,说明升高温度,对Na2CO3的水解有 作用。
请填写下列空白
实验室有下列仪器:
请从A~G中选择适当的装置填空(填字母)。
①有零刻度且在上方的是 ;
②需要垫上石棉网才可以加热的是 ;
③常盛放固体干燥剂,用以干燥气体的是 。
实验室常用的几种气体发生装置如下图所示:
(1)现用两种方法来制取氧气,可供选用的药品有:KClO3、Na2O2、NaOH、H2O、Na2CO3、MnO2。
第一种方法是选择装置图2,则需选用的试剂为:______________________;第二种方法是选择装置图3,则需选用的试剂为:_____________________________。
(2)若把装置图1与装置图4相连,在实验室可用来制取下列气体中的_________(填序号)。

①CH2=CH2 ②NO ③Cl2 ④C2H2 ⑤NH3
制取这种气体时,除选用(1)所提供的几种药品外,还需要的一种试剂是___________。
(3)若把装置图3与装置图5相连,进行实验,将溶液A逐滴加入试剂E中;溶液恰好澄清时,关闭B,然后往烧杯中加入热水,静置片刻,观察到试管内壁出现光亮的银镜,则溶液A是 ___________(写名称),C是__________(写化学式)与乙醛(或葡萄糖)的混合液。该反应的离子方程式为_____________________,仪器D在此实验中的作用是__________________________。
侯德榜是我国著名的工业化学家,又是一个伟大的爱国者,他所发明的制碱法为中国化学工业乃至世界化学工业作出了重要的贡献,被誉为“侯氏制碱法”。请你回答以下问题:
(1)“侯氏制碱法”中的“碱”其实不是烧碱,请实际情况出向它的溶液中滴加少量稀盐酸的离子方程式____________________________________。
(2)某同学为了验证 和
和 的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。
的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。
(3)某化学研究性学习小组在老师的指导下,模拟侯德榜先生的制碱原理设计了如图乙的实验装置。
A.实验的操作步骤中,你认为打开旋塞 、
、 的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。
的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。
B.在盛饱和食盐水的装置中发生反应的离子方程式为________________________;能析出碳酸氢钠晶体的原因是_________(填序号)。
a. 碳酸氢钠难溶于水 b. 碳酸氢钠受热易分解
c. 碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
装置中气胆的作用是___________________________________________________。
C.工业上若需制备纯碱,则上述原料中除了饱和食盐水外,其他原料用工业常用方法制取,写出工业制备两种原料气的主要化学反应方程式__________________。
(4)请你再写出一种实验室制取少量碳酸氢钠的方法:___________________________。
(5)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:原子利用率(%)=_______________。
某化学兴趣小组模拟测定 、
、 、
、 混合气体中
混合气体中 的体积分数,下图是它们在测定中使用的部分实验装置:
的体积分数,下图是它们在测定中使用的部分实验装置:
(1)在答卷的方框中画出所缺实验装置(含试剂)。
(2)当装置①出现________________________现象时,应立即停止通气。若此时没有及时停止通气,则测定的 体积分数_____________(填“偏高”、“偏低”或“不受影响”);若通入气体速度过快,则测定的
体积分数_____________(填“偏高”、“偏低”或“不受影响”);若通入气体速度过快,则测定的 体积分数__________(填“偏高”、“偏低”或“不受影响”)
体积分数__________(填“偏高”、“偏低”或“不受影响”)
(3)装置①中发生反庆的离子方程式为____________________________。
(4)你认为下列试剂中,可以用来代替试管中碘的淀粉溶液的是________(填编号)
A.酸性 溶液 溶液 |
B. 溶液 溶液 |
C.溴水 | D.氨水 |
(5)若碘溶液的浓度为 、体积为10mL,收集到的
、体积为10mL,收集到的 和
和 的体积为148.8mL(已折换为标准状况下的体积),
的体积为148.8mL(已折换为标准状况下的体积), 体积分数为___________。
体积分数为___________。
某研究小组在查阅资料中发现,常温下氯气可以氧化氨气获得氮气。该小组由此设计出制取氮气的思路,设计装置图如下。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用_________(填序号)。
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(2)装置F发生反应的离子方程式是___________________________。
(3)B装置的作用_________;E装置的作用__________________。
(4)写出制取 的化学方程式__________________;反应生成
的化学方程式__________________;反应生成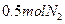 ,转移的电子数是_________
,转移的电子数是_________ 。
。
(5)当反应装置里的氨气和氯气的物质的量之比大于_________时,尾气里一定含有氨气;当反应装置里的氯气和氨气的物质的量之比大于_________时,尾气里一定含有氯气。
(16分)
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的结论是浓硝酸的氧化性强于稀硝酸.
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应.2NO2+2NaOH=NaNO3+NaNO2+H2O(1)装置①中发生反应的离子方程式是 .
(2)装置②的目的是 ,发生反应的化学方程式是 .
(3)实验应避免有害气体排放到空气中,装置③、④、⑤、⑥中盛放的药品依次是
.
(4)实验的具体操作是:先检验装置的气密性,再加入药品,然后打开弹簧夹,通入
目的是 .
(5)该小组得出的结论所依据的实验现象是 .
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的结论是浓硝酸的氧化性强于稀硝酸.
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应.2NO2+2NaOH=NaNO3+NaNO2+H2O (1)装置①中发生反应的离子方程式是 .
(2)装置②的目的是 ,发生反应的化学方程式是 .
(3)实验应避免有害气体排放到空气中,装置③、④、⑤、⑥中盛放的药品依次是
.
(4)实验的具体操作是:先检验装置的气密性,再加入药品,然后打开弹簧夹,通入
目的是 .
(5)该小组得出的结论所依据的实验现象是 .
工业上用固体硫酸亚铁制取Fe2O3,反应原理是: 2FeSO4 Fe2O3 +SO2↑+SO3↑某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
Fe2O3 +SO2↑+SO3↑某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
请回答相关问题:
(1)Fe2O3俗称为 不溶于水而易溶于酸,Fe2O3与稀盐酸反应的离子方程式为
(2)A瓶所盛试剂的作用是 C瓶所盛试剂的作用是
,用冷水冷却的原因是 ;B瓶所盛的试剂是
(3)将此反应生成的气体通入A瓶的BaCI2溶液中,下列说法正确的是 (填编号)
| A.析出BaSO3沉淀 | B.析出BaSO4沉淀 | C.逸出SO3气体 | D.逸出SO2气体 |
理由是
(4)在用固体硫酸亚铁制取Fe2O3的反应中,还原产物是 ,标准状况下每生成11. 2L SO2气体,转移电子的物质的量为 mol.
工业上用固体硫酸亚铁制取Fe2O3,反应原理是: 2FeSO4 Fe2O3 +SO2↑+SO3↑某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
Fe2O3 +SO2↑+SO3↑某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
请回答相关问题:
(1)Fe2O3俗称为 不溶于水而易溶于酸,Fe2O3与稀盐酸反应的离子方程式为
(2)A瓶所盛试剂的作用是 C瓶所盛试剂的作用是
,用冷水冷却的原因是 ;B瓶所盛的试剂是
(3)将此反应生成的气体通入A瓶的BaCI2溶液中,下列说法正确的是 (填编号)
| A.析出BaSO3沉淀 | B.析出BaSO4沉淀 | C.逸出SO3气体 | D.逸出SO2气体 |
理由是
(4)在用固体硫酸亚铁制取Fe2O3的反应中,还原产物是 ,标准状况下每生成11. 2L SO2气体,转移电子的物质的量为 mol.
(每空2分,共8分)
(1)下列所列的是中学化学实验室中几种常见的玻璃仪器:
①集气瓶 ②容量瓶 ③滴定管 ④烧杯 ⑤圆底烧瓶 ⑥量筒 ⑦温度计
可作反应容器并可加热的是 (填写编号),用以精确量取液体体积的是
(填写编号)
(2)在“用氢氧化钠溶液、碳酸钠溶液、氯化钡溶液、盐酸、水等试剂除去粗盐中的Ca2+、Mg2+、SO42-等杂质离子以获得纯净的食盐”的实验中,玻璃棒的作用可能是
(填写编号)
①搅拌 ②引流 ③蘸取溶液
(3)在仪器:①漏斗②容量瓶③蒸馏烧瓶④分液漏斗⑤烧杯⑥蒸发皿中,分离两种沸点接近且互不相溶的液体时会用到的有 (填写编号)
化合物KxFe(C2O4)y·3H2O(Fe为+3价)是一种光敏材料,实验室可以用如下的方法来制备这种材料并测定这种材料的组成。 Ⅰ.制备
Ⅰ.制备
K2C2O4
FeCl3
(1)结晶时应将溶液用冰水冷却并在黑暗处等待晶体的析出,这样操作的原因是:__________________。
(2)操作Ⅲ的名称是___________ 。
Ⅱ.组成测定
称取一定质量的晶体置于锥形瓶中,加入足量的蒸馏水和稀H2SO4,将C2O42-转化为H2C2O4后用0.1000 mol·L-1KMnO4溶液滴定,当消耗KMnO4溶液24.00mL时恰好完全反应;再向溶液中加入适量的还原剂,恰好将Fe3+完全转化为Fe2+,用KMnO4溶液继续滴定,当Fe2+完全氧化时,用去KMnO4溶液4.00mL。第二次滴定的离子化学方程式为:
_____________________________ __________________________
(3)配制100mL 0.1000 mol·L-1KMnO4溶液及滴定实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒、锥形瓶外还有_______________________________(填仪器名称)。
(4)该化合物KxFe(C2O4)y·3H2O中,x=_______。
向0.1mol/L的草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色总是先慢后快。对其原因,某研究性学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究:
| 实验组别 |
试管标号 |
所加药品 |
实验现象 (褪色时间) |
| 一 (室温) |
1 |
10ml 0.1mol/L的草酸(H2C2O4)溶液(用少量硫酸酸化)0.1mol/L的KMnO4溶液适量 + 少量硫酸锰固体 |
2s |
| 2 |
10ml 0.1mol/L的草酸(H2C2O4)溶液(用少量硫酸酸化)0.1mol/L的KMnO4溶液适量 |
30s |
|
| 二 (室温) |
1 |
5ml 0.1mol/L的草酸(H2C2O4)溶液 5滴0.1mol/L的KMnO4溶液+10滴稀硫酸 |
90s |
| 2 |
5ml 0.1mol/L的草酸(H2C2O4)溶液 5滴0.1mol/L的KMnO4溶液 |
100s |
|
| 三 (65℃ 的水浴) |
1 |
5ml 0.1mol/L的草酸(H2C2O4)溶液 5滴0.1mol/L的 KMnO4溶液 +10滴稀硫酸 |
90s |
| 2 |
5ml 0.1mol/L的草酸(H2C2O4)溶液 5滴0.1mol/L的KMnO4溶液 +1ml稀硫酸 |
100s |
|
| 3 |
5ml 0.1mol/L的草酸(H2C2O4)溶液 5滴0.1mol/L的KMnO4溶液 +2ml稀硫酸 |
120s |
(1) 该研究性学习小组的实验目是: 。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法
叫 法;
(3)设计第一组实验对应的假设是 ;
(4)由第二组实验和第三组实验得出的结论有 (填序号)
①温度对该反应速率影响不大
②硫酸对草酸和高锰酸钾溶液的反应有影响
③加入少量硫酸,可以促进草酸和高锰酸钾溶液的反应,而加入大量硫酸,反应速率比较慢
④在酸性范围呢,PH值越小,可能对反应越有利
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:
。