用如图所示装置进行下列实验。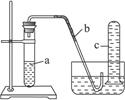
(1)在检查装置气密性后,向试管a中加入10 mL 6 mol·L-1稀硝酸和1 g铜片,立即将带有导管的橡皮塞塞紧管口。请写出试管a中有可能发生的所有反应的化学方程式________________________________________。
(2)该实验刚开始速率缓慢,随后逐渐加快,这是由于_______________________________。
(3)为了使产生的气体不至于逸散到空气中,请写出向试管a中加入试剂的操作方法______________________________________________________________________________。
(4)欲较快地制取NO,可采取的措施有(列举两种)_________________________________、________________________________________。
试样X由氧化亚铁和氧化铜组成。取质量相等的两份试样按下图所示进行实验:
(1)请写出步骤③中所发生的全部反应的离子方程式。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中氧化铜的质量为___________ (用m表示)。
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6 mol·L-1的盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
图1 图2
填写下列空白:
(1)实验进行时试管A中应加入的试剂是;烧瓶B的作用是______________________;烧瓶C的作用是______________________;在试管D中收集得到的是
____________________________。
(2)实验时,U形管G中应加入的试剂是___________;长颈漏斗H中应加入___________。
(3)两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母) ___________。
(4)烧瓶I中发生的反应有时要加入少量硫酸铜溶液,其目的是__________________________。
(5)试管E中发生反应的化学方程式是______________________________________________。
(6)为了安全,在E管中的反应发生前,在F出口处必须___________;E管中的反应开始后,在F出口处应___________。
现有0.1 mol·L-1的AlCl3溶液和0.1 mol·L-1的NaOH溶液,进行下面的实验。
(1)在试管中盛有上述AlCl3溶液10 mL,向其中逐渐滴入上述的NaOH溶液。
①加入10 mL NaOH溶液时的现象是___________;加入30 mL NaOH溶液时的现象是___________;加入35 mL NaOH溶液时的现象是___________。
②生成沉淀质量最多时,需NaOH溶液___________mL。
(2)向盛有10 mL NaOH溶液的试管中滴入AlCl3溶液,同时不停摇动试管,出现的现象是___________,至加入___________mL AlCl3溶液时开始出现沉淀,至加入___________mL AlCl3溶液使沉淀达最大值。写出上述过程的离子方程式
_______________________________。
已知X为FeO和CuO的混合物,取两份等质量的X样品进行下列实验:
(1)写出①②和③步所有反应的化学方程式:
_____________________________________;______________________________________。
_____________________________________;______________________________________。_____________________________________;______________________________________。
(2)设从③步所得固体D的质量为32 g,溶液E中只含有一种金属离子,气体F在标准状况下的体积为5.6 L,试计算取用的每份X的质量和X中FeO与CuO的质量比。
聚合硫酸铁(PPS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原成Fe2+。实验步骤如下:

(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有______________。
a.容量瓶 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_____________________________。
a.控制溶液中Fe2+与Fe3+含量比 b.确定下一步还原所需铁的量
c.确定氧化Fe2+所需NaClO3的量 d.确保铁的氧化物酸溶完全
(3)聚合硫酸铁溶液中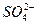 与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中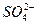 与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
a.NaOH b.FeSO4 c.BaCl2 d.NaClO3
(10分)某铝合金中含有合金元素镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请完成有关问题:
(1)称取样品a g,称量时应该使用的主要仪器的名称是
_______________________________。
(2)将样品溶解于足量的稀盐酸,过滤。滤液中主要含有______________________________,滤渣中含有_______________________,溶解、过滤用到的玻璃仪器是__________________。
(3)滤液中加过量氢氧化钠溶液、过滤。有关的离子方程式是_______________________,____________________________________。
(4)步骤(3)的滤液中通入足量二氧化碳气体,过滤。有关的离子方程式是______________。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称重,其质量为b g。有关的化学方程式是____________________,原样品中铝的质量分数是_________。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏___________(“高”“低”或“不影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏___________;若滤渣灼烧不充分,则实验结果偏___________。
粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.15 L 6.0 mol·L-1盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12 L(标准状态)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填写:
(1)产物中的单质B是_________________。
(2)②中所发生的各反应的化学方程式是___________________,______________________。
(3)③中所发生的各反应的离子方程式是
___________________________________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液c(Mg2+)为____________________,c(Fe2+)为_____________________。
镁是一种很活泼的金属,常用作脱硫剂、脱氧剂。在电子工业中利用镁制取硅的反应为2Mg+SiO2 2MgO+Si(玻璃中含有一定量的二氧化硅),同时有副反应发生:2Mg+Si
2MgO+Si(玻璃中含有一定量的二氧化硅),同时有副反应发生:2Mg+Si Mg2Si。Mg2Si遇盐酸迅速反应生成SiH4(硅烷)。SiH4在常温下是一种不稳定、易分解的气体。
Mg2Si。Mg2Si遇盐酸迅速反应生成SiH4(硅烷)。SiH4在常温下是一种不稳定、易分解的气体。
(1)图(甲)是进行Mg与SiO2反应的实验装置。
Ⅰ.由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气。X气体应选用①CO2、②N2、③H2中的________________。
Ⅱ.实验开始时,必须先通入X的气体,再接通电源加热反应物。其理由是_____________________________;当反应引发后,切断电源,反应能继续进行,其原因是_____________________________。
Ⅲ.反应结束时,待冷却至常温后,关闭K,从分液漏斗处加入稀盐酸,可观察到导管口a处有闪亮的火星。据此现象可推知____________________在空气中能自燃。
(2)图(乙)所示装置进行的实验如下:先关闭K,使A中反应进行;加热玻璃管C,可观察到C管中发出耀眼白光,产生白烟,管壁上附着有淡黄色物质。实验完成后,将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成。
Ⅰ.C中的Mg应放在不锈钢垫片上而不能直接接触管壁,这是因为______________________。
Ⅱ.停止实验时,先打开K,再停止滴加浓硫酸并熄灭酒精灯。橡胶气胆B在实验中的作用是_______________________________。
Ⅲ.C中全部反应产物有___________、___________、___________(填化学式)。
实验室用下图所示实验装置制取纯净的CuCl2,完成下列问题:
(1)实验室里,实验前检查整套装置的气密性方法是:_____________________________。
(2)装置A中发生的化学反应方程式为_____________________________。
(3)装置B的广口瓶盛__________,其作用是_____________________________________。装置C的广口瓶盛__________,其作用是___________________。装置E的烧杯中盛有,其作用是_____________________________。
(4)待充分反应后,装置D的玻璃管中剩余物呈_________色,冷却后,将制得的产物配成饱和溶液,溶液呈_________色。
有人设计了如图所示实验装置,目的是做钠与水反应实验并验证:①钠的物理性质;②钠与水反应的产物是什么?
(1)当进行适当操作时还需要的仪器有_____________________________。
(2)如何进行操作?_____________________________________________。
(3)实验现象是_________________________________________________。
(创新题)做一个家庭小实验:
(1)将蜡烛点燃,并燃烧几秒钟,等火焰稳定后,在其上方撒下小苏打粉末,火焰会出现什么现象?
(2)不慎将食盐水洒在煤气灶上,观察火焰的颜色。
解释上述两实验现象产生的原因。
(12分)右图是某老师设计的一个微型实验装置图,请你说出实验过程中可能出现的现象,试写出有关化学方程式。
图中a、b、c、d均为止水夹,e、f为红皮头
已除去泥沙的粗盐中,仍含有Mg2+、Ca2+和 ,请填写下表中的空格,完成将粗盐提纯,得到氯化钠晶体的实验设计。
,请填写下表中的空格,完成将粗盐提纯,得到氯化钠晶体的实验设计。
| ① |
溶解 |
将粗盐放入烧杯中,加入适量的蒸馏水,充分搅拌,直至固体全部溶解 |
| ② |
沉淀 |
逐渐加入氢氧化钠溶液,直至不再出现沉淀为止 |
| ③ |
|
|
| ④ |
|
|
| ⑤ |
过滤 |
安装好过滤器,将④烧杯中的悬浊液沿玻璃棒加入过滤器中过滤 |
| ⑥ |
|
|
| ⑦ |
|
|
实验目的:粗盐提纯,得到纯净氯化钠晶体
实验用品:(1)药品:粗盐、NaOH溶液、HCl溶液、Na2CO3溶液、BaCl2溶液、pH试纸和蒸馏水。
(2)仪器:略
(不必叙述如何组装实验装置)实验问题讨论
(1)甲同学在多次过滤后,发现烧杯中的滤液仍浑浊,分析他的操作不当的原因可能是:
①_______________________________________________________________________。
②______________________________________________________________________。
(2)乙同学过滤后,滤液是澄清的,当取少量蒸发后的氯化钠晶体溶于水滴加硫酸钠溶液时,却出现白色沉淀。分析乙在实验步骤设计上存在的问题可能是____________________。
有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,现做以下实验:
①将部分粉末加入水中,振荡有白色沉淀生成。
②向①的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生。
③取少量②的溶液,滴加稀硫酸,有白色沉淀生成。
④另取少量②的溶液,滴加AgNO3溶液,有白色沉淀生成。
请回答:
(1)根据上述实验现象,判断原白色粉末的组成成分是___________(填写名称)。
(2)写出①—④中涉及的化学方程式:
①______________________________
②_____________________________
③______________________________
④_____________________________