粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质。为了除去杂质在实验室中可将粗盐溶于水然后进行下列操作:(1)过滤;(2)加入过量的氢氧化钠溶液;(3)加入适量的盐酸;(4)加过量Na2CO3溶液;(5)加过量的BaCl2溶液。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)以上操作的正确顺序是( )
| A.(5)(4)(2)(1)(3) | B.(1)(2)(3)(4)(5) |
| C.(5)(4)(3)(2)(1) | D.(1)(5)(4)(2)(3) |
(2)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作顺序为___________。
(3)如何运用最简的方法检验溶液中有无SO42―离子?______________________________。
如果有,应该如何除去SO42―离子?
___________________________________________。
(4)在粗盐经过溶解等步骤后,在过滤前的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。这步操作的目的是
______________________________________________。
(5)将经过操作(4)后的溶液过滤。请问这一操作能除掉哪些杂质?
(6)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:________________________________________。过滤时:________________________________________。蒸发时:________________________________________。
用18 mol / L的硫酸溶液配制500 mL 1 mol / L的硫酸溶液,有下列操作步骤:
(1)将溶解后的硫酸溶液立即沿玻璃棒转入容量瓶中;
(2)将量得浓硫酸倒入烧杯中,加水溶解,然后用蒸馏水洗涤量筒2~3次倒入烧杯中;
(3)盖上瓶塞,轻轻摇匀即配制完毕。
(4)洗涤烧杯和玻璃棒2~3次,将洗涤液全部转入容量瓶中,加水至离刻度1~2 cm处,改用胶头滴管加水至刻度线;
(5)用量筒量取27.78 mL的浓硫酸。
先将以上步骤按实际操作的先后顺序排列,________________指出操作中所有的错误和不妥之处。
电制法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42―杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下: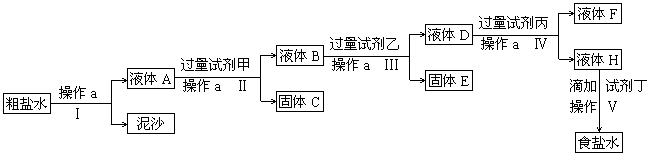
请回答以下问题:
(1)操作a的名称是____________,所用玻璃仪器是________________________________。
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为________溶液。
(3)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式________________。
(1)用质量分数为98%、密度为1.84g·cm-3的浓硫酸配制100mL1.84mol·L-1的稀硫酸,若实验仪器有:A.100mL量筒;B.托盘天平;C.玻璃棒;D.50mL容量瓶;E.10mL量筒,F.胶头滴管;G.50mL烧杯;H.100mL容量瓶,实验时应选用仪器的先后顺序是(填入编号):________。
(2)在容量瓶的使用方法中,下列操作不正确的是(填编号)________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线2~3cm处,用滴管加蒸馏水到标线
D.配制溶液时,如果试样是液体,用量筒量取试样后,直接倒入容量瓶中,缓慢加入蒸馏水到标线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
F.往容量瓶中转移溶液时应用玻璃棒引流
(1)浓硫酸与木炭粉在加热条件下的化学方程式为_________________________。
(2)已知酸性KMnO4溶液可以吸收SO2,试用图4-6所示各装置设计一个实验,验证上述反应所产生的各种产物。
这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):
__________→__________→__________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是______________________,B瓶溶液的作用是____________________,C瓶溶液的作用是_________________________。
(4)装置②中所加的固体药品是_______________,可确证的产物是_______,确定装置②在整套装置中位置的理由是_____________________。
(5)装置③中所盛溶液是__________,可验证的产物是__________。
在某NaOH溶液里加入几滴酚酞试液,溶液显红色,向其中逐滴加入新制的饱和氯水,当滴到最后一滴时,红色突然褪去。回答下列问题:
(1)产生该现象的原因可能有:
①__________________________;
②__________________________。
(2)简述怎样用实验证明红色褪色的原因是①或者是②。
____________________________________。
某学生设计了三个实验方案,用以检验淀粉的水解情况。
(1)方案甲:
淀粉液 水解液
水解液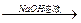 中和液
中和液 溶液变蓝。结论:淀粉没有水解。
溶液变蓝。结论:淀粉没有水解。
(2)方案乙:
淀粉液 水解液
水解液 无红色沉淀。结论:淀粉完全没有水解。
无红色沉淀。结论:淀粉完全没有水解。
(3)方案丙:
淀粉液 水解液
水解液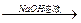 中和液
中和液 有红色沉淀。结论:淀粉已水解。
有红色沉淀。结论:淀粉已水解。
(4)方案丁: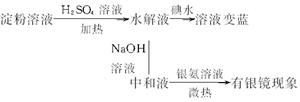
结论:淀粉部分水解。
以上四种方案的设计及结论是否正确?如不正确,请简述理由。
为了测定某有机物的分子式和结构式,进行下列各步实验,根据实验事实逐一分析推断,推断出各步实验的结论。
(1)将此有机物完全燃烧,只生成CO2和H2O。
(2)该有机物1 mol在一定条件下与5 mol乙酸反应生成有香味的液体。
(3)该有机物能使溴水褪色,且1 mol该有机物与银氨溶液反应生成2 molAg。
(4)该有机物的相对分子质量是乙烷的6倍,且被H2还原为直链多元醇。
(8分)
(1)在一定条件下,乙烯和乙烷都能制备氯乙烷。
请回答:
①由乙烷制备氯乙烷的化学方程式是____________,该反应属于____________反应。
②由乙烯制备氯乙烷的化学方程式是____________,该反应属于____________反应。
③比较两种方法,____________种方法较好,其原因是________________________________。
(2)沼气是一种廉价能源,农村存在大量的秸杆、杂草等废弃物,它们经微生物发酵后,便可产生沼气,可用来点火做饭。
①已知:(C6H10O5)n+nH2O 3nCO2↑+3nCH4↑+能量,试说明这个总反应的实际价值与意义:____________。
3nCO2↑+3nCH4↑+能量,试说明这个总反应的实际价值与意义:____________。
②煤的主要成分是碳,写出煤和沼气的主要成分燃烧的化学方程式____________;并指出哪一种燃料对环境污染小。____________。
③若建立沼气发电站,可实现把____________转化成电能,沼气可称为____________能源。
(7分)下表数据是在某高温下,金属镁和镍分别在氧气中进行氧化反应时,在金属表面生成氧化薄膜的实验记录。
| 反应时间t/h |
1 |
4 |
9 |
16 |
25 |
| MgO层厚y/nm |
0.05a |
0.20a |
0.45a |
0.18a |
1.25a |
| NiO层厚y′/nm |
B |
2b |
3b |
4b |
5b |
注:a和b均为与温度有关的常数。
(1)金属高温氧化腐蚀速率可以用金属氧化膜的生长速率来表示,其理由是_______________
_______________________________________________________________________________;
(2)金属氧化膜厚y跟时间t所呈现的关系是(填“直线”、“抛物线”、“对数”或“双曲线”等类型):MgO氧化膜的膜厚y与时间t的关系属________型;NiC氧化膜的膜厚y′与时间t的关系属________型;
(3)Mg与Ni比较,哪一种金属具有更良好的耐氧化腐蚀性?阐述其理由。
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
_______________________________________________________________________________。
(11分)下图表示两种溶液进行电解的装置:
电极A由金属R制成,R的硫酸盐的化学式为RSO4,B、C、D都是Pt。P和Q是电池的两极,电路接通后,金属离子R2+离子沉积于电极B上,同时电极C、D上产生气泡。
(1)P和Q中正极是__________。
(2)A极上的电极反应式为_______________________。
(3)罩在电极C、D上的两集气瓶中收集到气体的体积比是__________。
(4)当电流强度为2 A,通电3 min 13 s后,电极B上生成金属R 0.127 g。已知1 mol电子的电量为96 500 C,则R的相对原子质量为__________,它是__________(填元素符号)。
(5)将P和Q变换位置接线,使电流方向反过来,电流强度为2 A,5 min后在B极上看到了_____________、_______________________两种现象。
含苯酚的工业废水处理的流程如下图:
(1)上述流程中,设备Ⅰ中进行的是操作__________(填写操作名称)。实验室里这一步操作可以用__________进行(填写仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是__________,由设备Ⅲ进入设备Ⅳ的物质B是__________。
(3)在设备Ⅲ中发生反应的化学方程式为______________________________。
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和_________。通过__________操作(填写操作名称),可以使产物相互分离。
(5)在上图中,能循环使用的物质是C6H6、CaO、__________、__________。
如图是某化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图。在烧瓶A中放一些新制的无水硫酸铜粉末,并加入20 mL无水乙醇;锥形瓶B中盛放浓盐酸;分液漏斗C和广口瓶D中分别盛浓H2SO4;干燥管F中填满碱石灰;烧杯作水浴器。当打开分液漏斗C的活塞后,由于浓H2SO4流入B中,则D中导管口有气泡产生。过几分钟后,无水硫酸铜粉末由无色变为蓝色。此时水浴加热后,发生化学反应生成的气体从F处逸出,点燃气体,有绿色火焰。试回答:
(1)B中逸出的气体主要成分是______________。
(2)D瓶的作用是__________________。
(3)E管的作用是__________________。
(4)F管口点燃的气体是_________________。
(5)A瓶中无水硫酸铜粉末变蓝的原因是____________________________________。
(6)由A中发生的反应事实,可推断出的结论是___________________________。
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。加热聚丙烯废塑料得到的产物如下表:
| 产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
| 质量分数(%) |
12 |
24 |
12 |
16 |
20 |
10 |
6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
写出反应②③的化学方程式:______________________、___________________________。
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有_______________种。
(3)锥形瓶C中观察到的现象____________________________________________________。
经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为___________。
(4)写出C中逸出的气体在工业上的两种用途:______________________________________、_________________________________________________。
图4-39是用石墨和铁作电极电解饱和食盐水的装置。请填空:
图4-39
(1)X的电极名称是_________极,发生的电极反应式为________,Y极的电极材料是_______。检验X极的产物方法是_____________________。
(2)某同学在实验时误将两种电极材料接反,导致X极上未收到预期产物。一段时间后又将两极的连接方式纠正过来,发现X一端出现了白色沉淀,此沉淀是_______(填化学式)。其形成原因是___________,该沉淀在空气中放置,现象是________________________。
(3)工业上电解饱和食盐水的方法之一,是将两个极室用离子交换膜隔开(如图4-40)其目的是_______,阳极室(A处)加入_______,阴极室(B处)加入_______,离子交换膜只许_________离子通过。
图4-40