有机物的结构可用键线式简化表示,如CH3 — CH=="CH—" CH3可表示为
有一种有机物X的键线式如图所示。
(1)X的分子式为_______________________________。
(2)有机物Y是X的同分异构体,且属于芳香族化合物。则Y的结构简式是_____________________。
(3)Y在一定条件下可发生反应生成高分子化合物,该反应的化学方程式_____________。
(4)Y可以与溴水反应,该反应的化学方程式是___________________________。
已知:
完成下列填空:
(1)分子式为C8H8的某烃,在臭氧作用下发生反应为:
则该烃的结构简式为______________________________________。
(2)若分子式为C8H8的某烃其一氯代物只有一种,写出1种其可能的结构简式_________。
分子式为C8H8的烃有很多,其中有一种苯乙烯,性质活泼,易被氧化,是合成橡胶和塑料的单体,用途广泛。苯乙烯可以通过下列途径制备(反应条件下所有物质均呈气态):
(3)上述流程中各物质,属于苯的同系物的是__________(填结构简式);能与溴水发生加成反应的是_________________________(均填结构简式)
(4)反应①是强吸热可逆反应。要既快又多地获取苯乙烯,反应①适宜条件是__________;为了进一步提高反应物的转化率,有研究者用加入O2与H2反应的方法获取了更多的苯乙烯,试推测其中的原因___________(写出一条)。
Na2S又称臭碱、硫化碱,是应用广泛的化工原料,也常用于吸收工业废气中的SO2。
完成下列填空:
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因___________________________。
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式________。结合你所学习过的其它离子反应分析,离子互换反应进行的方向是_________________。向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐_____________(填“变大”、“变小”),生成的沉淀是_____________;
(4)关于反应后得到的溶液,下列离子浓度关系正确的是___________。
a.c(Na+) = c(S2O32-) + 2 c(HSO3-) + 2c(H2SO3) + 2 c(HS-)
b.c(Na+) + c(H+) =" 2" c(S2O32-) + c(HSO3-) + c(HS-) + c(OH-)
c.c(Na+) =" 2" c(HS-)
二氧化氯(ClO2)是国际公认高效、安全的杀菌、保鲜剂,是氯制剂的理想替代品。工业上制备ClO2的方法很多,NaClO3和NaClO2是制取ClO2的常见原料。
完成下列填空:
(1)以下反应是制备ClO2的一种方法:H2C2O4 + 2 NaClO3 + H2SO4 → Na2SO4 + 2 CO2↑ + 2 ClO2↑ + 2 H2O,上述反应物中属于第三周期的元素的原子半径大小顺序是__________;其中原子半径最大元素的原子,其核外有 种不同能量的电子。
(2)ClO2的分子构型为“V”形,则ClO2是______________(选填“极性”、“非极性”)分子,其在水中的溶解度比氯气__________(选填“大”、“小”、“一样”)。
(3)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,ClO2的消毒能力是等质量Cl2的___________倍(保留2位小数)。
(4)若以NaClO2为原料制取ClO2,需要加入具有________(填“氧化”、“还原”)性的物质。
(5)工业上将氯碱工业和制取NaClO3联合进行。研究发现,电解时,不同反应环境下的总反应分别为:
4 NaCl + 18 H2O → 4 NaClO3 + 3 O2↑+ 18 H2↑(中性环境)
NaCl + 3 H2O → NaClO3 + 3 H2↑(微酸性环境)
①电解时,氢气在__________极产生。
②更有利于工业生产NaClO3的反应环境是___________,理由__________________。
某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+。当加入一种淡黄色固体并加热溶液时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系,如图所示。

(1)写出反应②和④的离子方程式
② 。
④ 。
(2)溶液中含有的离子是 ,它们的物质的量浓度之比为 。
铬是用途广泛的金属,但在生产过程中易产生有害的含铬工业废水。
I. 还原沉淀法处理含Cr2O72-和CrO42-,工业废水的一种常用方法,其工艺流程如下:
CrO42- Cr2O72-
Cr2O72- Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
(1)若平衡体系的pH=0,该溶液显 色。
(2)第②步反应的离子方程式是 。
已知:常温下Ksp[Cr(OH)3] =6.0×10-31, Ksp[Fe(OH)3]=4.0×10-38
向第②步反应后的溶液中加入一定量烧碱,若溶液中c(Fe3+)=4.0×10-14 mol/L,溶液的pH值为 ,此时溶液中c(Cr3+)= mol/L。
II.探究 CrO3的强氧化性和热稳定性
(3)CrO3具有强氧化性,遇到有机物(如酒精)时,剧烈反应以至着火.若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的Cr2(SO4)3.完成该反应的化学方程式:
CrO3 + C2H5OH+ H2SO4= Cr2(SO4)3+ CH3COOH+
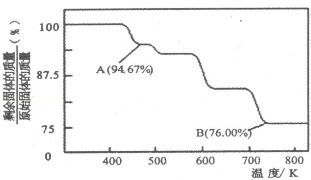
(4))CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。B点时剩余固体的成分是 (填化学式 )。
工农业生产和科学实验中常常涉及溶液的酸碱性,人们的生活健康也与溶液的酸碱性有关,因此,测试和控制溶液的pH具有重要意义。
(1)常温下,下列事实一定能证明HA是弱电解质的是 。
①常温下HA溶液的pH小于7
②用HA溶液做导电实验,灯泡很暗
③常温下NaA溶液的pH大于7
④0.1mol/L HA溶液的pH=2.1
⑤将等体积的pH=2的HCl与HA分别与足量的Zn反应,放出的H2体积HA多
⑥pH=1的HA溶液稀释至100倍,pH约为2.8
(2)常温下,①将 pH=3的HA溶液与将 pH=11的NaOH溶液等体积混合后,溶液可能呈 (选填字母:a酸性、b碱性、c中性 )。
②将等物质的量浓度的HA溶液与NaOH溶液等体积混合后,溶液可能呈 (选填字母:a酸性、b碱性、c中性)。用离子方程式解释混合液②呈酸性或碱性的原因 。
(3)甲、乙两烧杯均盛有5 mL pH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4。关于甲、乙烧杯中溶液的描述正确的是( )
A.溶液的体积10V甲≥V乙
B.水电离出的OH―浓度:10c(OH―)甲=c(OH―)乙
C.若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙
D.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙
(4)若HA为弱酸,一定浓度的HA和NaA的混合溶液可作为控制体系pH的缓冲溶液,向缓冲溶液中加入少量的酸或碱,溶液pH 的变化很小,下列体系可作为缓冲溶液的有 。
A.氨水和氯化铵混合溶液 B.硝酸和硝酸钠溶液
C.盐酸和氯化钠混合溶液 D.醋酸和醋酸钠溶液
(5)某二元酸(化学式用H2B表示 )在水中的电离方程式是:H2B=H++HB﹣;HB﹣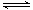 H++B2﹣。在0.1mol·L﹣1的Na2B溶液中,c(B2﹣ ) + =0.1mol·L﹣1。
H++B2﹣。在0.1mol·L﹣1的Na2B溶液中,c(B2﹣ ) + =0.1mol·L﹣1。
(6)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中
c(NH4+)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=__________。
面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的主要方向。
(1) “生物质”是由植物或动物生命体衍生得到的物质的总和。生物质能主要是指用树木、庄稼、草类等植物直接或间接提供的能量.秸秆、杂草等废弃物经微生物发酵之后,便可以产生沼气,利用沼气是解决人类能源危机的重要途径之一。下面说法不正确的是( )
| A.利用生物质能就是间接利用太阳能,生物质能是可再生能源 |
| B.生物质能是解决农村能源的重要途径之一 |
| C.生物质能的缺点是严重污染环境 |
| D.若建立沼气发电站,则可以实现把生物质能转化为电能 |
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO和H2,已知CH4、H2和CO的燃烧热(△H)分别为 -890.3 KJ·mol-1、-285.8 KJ·mol-1、-283.0 KJ·mol-1,则该重整的热化学方式为 ;
(3)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:
C(s) +CO2(g ) 2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:已知气体分压(P分 )=气体总压(P总 )×体积分数,则925℃时,用平衡分压代替平衡浓度表示的化学平衡常数= 。T℃时,若充入等体积的CO2和CO,平衡 (填“正向移动、逆向移动、不移动”)。
2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:已知气体分压(P分 )=气体总压(P总 )×体积分数,则925℃时,用平衡分压代替平衡浓度表示的化学平衡常数= 。T℃时,若充入等体积的CO2和CO,平衡 (填“正向移动、逆向移动、不移动”)。


(4)如下图是一个二甲醚(CH3OCH3)燃料电池工作时的示意图,
①若乙池为粗铜的电解精炼,电解质为硫酸铜,则N电极材料为 。
②若乙池中M、N为惰性电极,电解质为足量硝酸银溶液,写出乙池中电解的化学方程式 。乙池中某一电极析出金属银2.16g时,溶液的体积为200mL,则常温下乙池中溶液的pH为 。
③通入二甲醚的铂电极的电极反应式为 。若该电池的理论输出电压为1.0V,则该电池的能量密度= kW·h·kg-1(结果保留小数点后一位).(能量密度=电池输出电能/燃料质量,1kW·h=3.6×106J,法拉第常数F=9.65×l04C·mol-1 )。
铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)Fe基态原子核外电子排布式为 。
(2)H、N、O的电负性从小到大的顺序是 。
(3)与NO2+互为等电子体的一种分子为 (填化学式)。氨基(-NH2)中氮原子的杂化类型为 。
(4)1mol苯分子中含有σ键的数目为 。
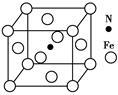
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为 。
已知孔雀石的主要成分为Cu2(OH)2CO3,还含少量FeO、SiO2。现以孔雀石为原料制备CuSO4·5H2O。
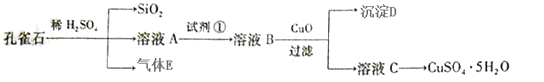
(1)实验步骤中试剂①最佳选择 (填代号);
a.H2O2 b.Cl2 c.KMnO4 d.HNO3
请写出其对应的离子方程式 。
(2)溶液B中加入CuO作用是 。
(3)由溶液C获得CuSO4·5H2O晶体,需要经___________、____________和过滤。
(4)25 ℃,Fe(OH)3的Ksp=1×10-38,若要将溶液中的Fe3+沉淀完全,必需调节溶液pH> 。
(5)实验室用惰性电极电解500ml的CuSO4溶液一段时间后,撤去电源,若加入0.2mol Cu(OH)2恰好使电解液恢复到原来状态,则电解过程中转移电子的物质的量为__________mol,原CuSO4溶液的物质的量浓度为________mol·L-1。
已知2SO2(g)+O2(g) 2SO3(g) ΔH=-a kJ/mol (a>0),在一个装有催化剂的2L的密闭容器中加入2 mol SO2和1 mol O2,在T ℃时充分反应,10s后达平衡状态,测得容器内气体压强为起始压强的5/6,放出热量为b kJ。
2SO3(g) ΔH=-a kJ/mol (a>0),在一个装有催化剂的2L的密闭容器中加入2 mol SO2和1 mol O2,在T ℃时充分反应,10s后达平衡状态,测得容器内气体压强为起始压强的5/6,放出热量为b kJ。
(1)计算:10s内该反应的平均速率v(O2)=______________,平衡常数K=______________。
(2)比较a b(填“>”“=”或“<”,下同),已知T1 ℃时,该反应的平衡常数K=16,由此可推知, T1___________T。
(3)若在原来的容器中,只加入2 mol SO3,T ℃时充分反应达平衡后, 吸收热量为c kJ,则a、b、c之间满足何种关系 (用代数式表示)。
(4)若相同条件下,向上述容器中分别通入x mol SO2 (g)、y mol O2 (g)、z mol SO3 (g),欲使达到新平衡时容器内气体压强仍为起始压强的5/6。
①x、y、z必须满足的关系是 、 ;
②欲使起始时反应表现为向正反应方向进行,则x的取值范围是 。
(5)将上述容器改为恒压容器(反应前体积相同),起始时加入2 mol SO2和1 mol O2,T ℃时充分反应达平衡后,放出热量为d kJ,则d b(填“>”“=”或“<”)。
水溶液中的行为是中学化学的重要内容。
(1)25 ℃时,某溶液中由水电离出c(H+)=1×10-10 mol/L,该溶液pH为_______________。
(2)25 ℃时,测得亚硫酸氢钠溶液的pH<7,解释该溶液显酸性的原因(用离子方程式表示,并作适当解释) 。
(3)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 |
电离常数(25 ℃) |
| HCN |
K=4.9×10-10 |
| HClO |
K=3×10-8 |
| H2CO3 |
K1=4.3×10-7、K2=5.6×10-11 |
25 ℃时,将浓度相同的四种盐溶液:① NaCN ② NaClO ③ Na2CO3 ④ NaHCO3,按pH由大到小的顺序排列 (填序号),向84消毒液中通入少量的CO2,该反应的化学方程式为 。
(4)25 ℃时,将n mol·L-1的氨水与0.2mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_______________性(填“酸”、“碱”或“中”), NH3·H2O的电离常数Kb=_____________(用含n的代数式表示)。
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景。工业生产甲醇的常用方法是CO(g)+2H2(g)===CH3OH(g) ΔH<0。
(1)在25℃、101 kPa下,1 g甲醇(液态)完全燃烧后,恢复到原状态放热Q kJ,则表示甲醇燃烧热的热化学方程式为 。
(2)工业上利用甲醇制备氢气常用的方法之一是甲醇蒸气重整法。此方法当中的一个主要反应为CH3OH(g)===CO(g)+2H2(g),说明该反应能自发进行的原因 。
(3)甲醇燃料电池由于其结构简单、能量转化率高、对环境无污染、可作为常规能源的替代品而越来越受到关注。其工作原理如右图,质子交换膜左右两侧的溶液均为1L 1.5 mol/L H2SO4 溶液。

①通入气体a的电极是电池的______________(填“正”或“负”)极,其电极反应式为_______________;
②当电池中有2 mole-发生转移时,左右两侧溶液的质量之差为__________________(忽略气体的溶解,假设反应物完全耗尽)。
为测定一种复合氧化物材料的组成。称取12.52g样品,将其全部溶于过量稀硝酸后,配成100ml溶液。取其一半,加入过量K2SO4溶液,生成白色沉淀,经过滤、洗涤、烘干后得4.66克固体。在余下的50毫升溶液中加入少许KSCN溶液, 显红色;如果加入过量NaOH溶液,则生成红褐色沉淀,将沉淀过滤、洗涤、灼烧后得3.20克固体。计算确定该材料的化学式为 。
(1)某氯化镁溶液的密度为d g·cm-3,其中镁离子的质量分数为A%,则300 mL该溶液中c (Cl-)= (mol/L)。
(2)无土栽培中,需配制营养液NaH2PO4、Na2HPO4(物质的量之比为4 : 1),已知每升含磷元素0.10mol,现用4.0mol/LH3PO4和固体NaOH配制2 L该营养液需要:
V(H3PO4)= (mL),m(NaOH)= (g)。
(3)甲、乙两烧杯中各成盛有100mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为 甲 : 乙=1 : 2,则加入铝粉的质量为: (g)。