工农业生产和科学实验中常常涉及溶液的酸碱性,人们的生活健康也与溶液的酸碱性有关,因此,测试和控制溶液的pH具有重要意义。
(1)常温下,下列事实一定能证明HA是弱电解质的是 。
①常温下HA溶液的pH小于7
②用HA溶液做导电实验,灯泡很暗
③常温下NaA溶液的pH大于7
④0.1mol/L HA溶液的pH=2.1
⑤将等体积的pH=2的HCl与HA分别与足量的Zn反应,放出的H2体积HA多
⑥pH=1的HA溶液稀释至100倍,pH约为2.8
(2)常温下,①将 pH=3的HA溶液与将 pH=11的NaOH溶液等体积混合后,溶液可能呈 (选填字母:a酸性、b碱性、c中性 )。
②将等物质的量浓度的HA溶液与NaOH溶液等体积混合后,溶液可能呈 (选填字母:a酸性、b碱性、c中性)。用离子方程式解释混合液②呈酸性或碱性的原因 。
(3)甲、乙两烧杯均盛有5 mL pH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4。关于甲、乙烧杯中溶液的描述正确的是( )
A.溶液的体积10V甲≥V乙
B.水电离出的OH―浓度:10c(OH―)甲=c(OH―)乙
C.若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙
D.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙
(4)若HA为弱酸,一定浓度的HA和NaA的混合溶液可作为控制体系pH的缓冲溶液,向缓冲溶液中加入少量的酸或碱,溶液pH 的变化很小,下列体系可作为缓冲溶液的有 。
A.氨水和氯化铵混合溶液 B.硝酸和硝酸钠溶液
C.盐酸和氯化钠混合溶液 D.醋酸和醋酸钠溶液
(5)某二元酸(化学式用H2B表示 )在水中的电离方程式是:H2B=H++HB﹣;HB﹣ H++B2﹣。在0.1mol·L﹣1的Na2B溶液中,c(B2﹣ ) + =0.1mol·L﹣1。
H++B2﹣。在0.1mol·L﹣1的Na2B溶液中,c(B2﹣ ) + =0.1mol·L﹣1。
(6)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中
c(NH4+)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=__________。

 和
和 ,可选用 ▲(填字母)。
,可选用 ▲(填字母)。
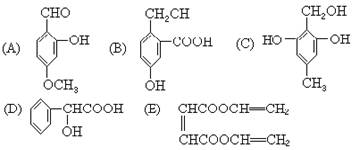

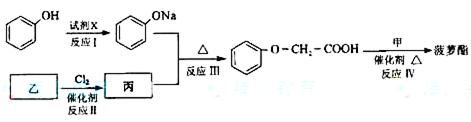
 -O-CH2-COOH发生酯化反应的产物。
-O-CH2-COOH发生酯化反应的产物。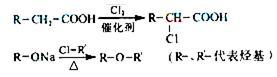
 粤公网安备 44130202000953号
粤公网安备 44130202000953号