配制0.1 mol·L-1的NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是 ( )
| A.称量时,左盘高,右盘低 | B.定容时俯视读取刻度 |
| C.原容量瓶洗净后未干燥 | D.定容时液面超过了刻度线 |
已知某溶液的:①体积;②密度;③溶质和溶剂的质量比;④溶质的摩尔质量,要根据溶质的溶解度计算其饱和溶液的物质的量浓度时,上述条件中必不可少的是( )
| A.①②③④ | B.①②③ | C.②④ | D.①④ |
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是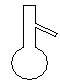
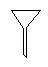


| A.蒸馏、蒸发、萃取、过滤 | B.蒸馏、过滤、萃取、蒸发 |
| C.萃取、过滤、蒸馏、蒸发 | D.过滤、蒸发、萃取、蒸馏 |
下列实验事故的处理方 法正确的是 ( )
法正确的是 ( )
A 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭
B 不 慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦。
慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦。
C 皮肤上溅有较多的浓硫酸,赶紧用水冲洗。
D 衣服沾上大量的浓氢氧化钠溶液,需将此衣服浸泡在盛水的盆中。
下列根据实验现象所得出的结论中,一定正 确的是 ( )
确的是 ( )
| A.无色溶液使红色石蕊试纸变蓝,结论:溶液显碱性 |
| B.无色溶液焰色反应呈黄色,结论:试液是钠盐溶液 |
| C.无色溶液加入Na2CO3溶液产生白色沉淀,结论:试液中含Ca(OH)2 |
| D.无色试液加入氢氧化钠溶液,加热产生的气体使红色石蕊试纸变蓝,结论:试液中含NH3 |
现有下列四种因素:① 温度和压强 ② 所含微粒数 ③ 微粒本身大小 ④ 微粒间的距离,其中对气体物质体积有显著影响的是( )
| A.只②③④ | B.只①②④ | C.只①③④ | D.①②③④全部 |
有关化学实验的下列操作中,一般情况下不能相互接触的是 ( )
| A.过滤操作中,玻璃棒与三层滤纸 |
| B.过滤操作中,漏斗径与烧杯内壁 |
| C.分液操作中,分液漏斗径与烧杯内壁 |
| D.用胶头滴管向试管滴液体时,滴管尖端与试管内壁 |
3月11日的日本大地震使福岛第一核电站受损,泄漏放射性物质131I、132I、和134Cs、137Cs等导致核污染。服用一定剂量的碘片可防放射性碘的伤害。下列说法错误的是
A.131I、132I、134Cs、137Cs是四种不同的核素 |
B.食用碘盐不能防辐射 |
C.碘片的主要成分是I2  |
D.核能仍然是重要能源之一 |
极细的黄金粒子在水中可以形成玫瑰红色胶体金,为了能观察到胶体金颗粒的形态,德国化学家席格蒙迪研制出超显微镜,创立了现代胶体化学研究的基本方法,因而获得1925年的诺贝尔化学奖。用这种超显微镜能分辨的颗粒大小为
| A.10nm | B.200nm | C.1000nm | D.10000nm |
分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
| A.根据纯净物的元素组成,将纯净物分为单质和化合物 |
| B.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
| C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类 |
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。下列实验中所选用的仪器合理的是
①用50 mL量筒量取5.2 mL稀硫酸 ②用分液漏斗分离苯和四氯化碳的混合物 ③用托盘天平称量11.7g氯化钠晶体 ④用碱式滴定管取23.10 mL溴水 ⑤用瓷坩埚灼烧各种钠化合物 ⑥用250 mL容量瓶配制250 mL 0.2 mol/L的NaOH溶液
| A.①②④ | B.③⑥ | C.②③④⑥ | D.③⑤⑥ |
右图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。制造此加热杯可选用的固体碎块是 ( )
| A.硝酸铵 | B.生石灰 | C.氯化镁 | D.食盐 |
已知反应mX(g)+nY(g)  qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( B )
qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( B )
| A.通入稀有气体使压强增大,平衡将正向移动 |
| B.X的正反应速率是Y的逆反应速率的m/n倍 |
| C.降低温度,混合气体的平均相对分子质量变小 |
| D.若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n:m |