选做[化学——选修3:物质结构与性质]已知A、B、C、D、E、F都是元素周期表中前36号的元素,它们的原子序数依次增大。A的一种单质是自然界硬度最大的物质,B是地壳中含量最多的元素,C的单质能从B的一种氢化物中置换出B的一种单质,D是人体骨骼中的常见元素,D的氢氧化物常用来检验A和B形成的一种化合物,F的原子序数比E大1,F是Ⅷ族元素中原子序数最小的一种元素。
(1)E的基态原子电子排布式为 ,比较F和 E的各级电离能后发现,气态E2+再失去一个电子比气态F2+再失去一个电子难,其原因是 。
(2)写出 DA2的电子式 。
(3)DC2的一个晶胞如图所示,则图中实心球表示D还是C?
答: (填元素名称)。该晶体的密度为a g/cm3,则晶胞的体积是 (只要求列出算式)。
(4)AB32- 离子的空间立体构型为 ,AB气体在配合物中常作为配体,如近年来开始使用的一种新型汽油防震剂F(AB)5,该化合物中F元素的化合价为 。
【化学一选修3:物质结构与性质】(15分)
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、 (PAN)等二次污染物。
(PAN)等二次污染物。
①1mol PAN中含有的σ键数目为_______。PAN中除H外其余三种元素的第一电离能由大到小的顺序为_________________。
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为_______,中心离子的核外电子排布式为_______________。
③相同压强下,HCOOH的沸点比CH3OCH3____(填“高”或“低”),其原因是___________________。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间的作用力不涉及___________(填序号)。
a.离子键
b.共价键
c.配位键
d.范德华力
e.氢键
②NH4NO3中阳离子的空间构型为_____,阴离子的中心原子轨道采用_______杂化。
(3)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则m/n=_____(填数字)。
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为24。
(1)F原子基态的核外电子排布式为 。
(2)在A、B、C三种元素中,第一电离能由大到小的顺序是 (用元素符号回答)。
(3)元素B的简单气态氢化物的沸点远高于元素A的简单气态氢化物的沸点,其主要原因是 。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为 。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 。
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 。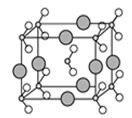
铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。回答下列问题:
(1)铜原子基态电子排布式为 ;
(2)用晶体的X射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00 g·cm-3,则铜晶胞的体积是 cm3、晶胞的质量是 g,阿伏加德罗常数为 (列式计算,已知A1(Cu)=63.6);
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为 。已知其中一种化合物的化学式为KCuCl3,另一种化学式为 ;
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是 ,反应的化学方程式为 。
【化学——物质结构与性质】选做X、Y、Z、L四种元素分别位于周期表中三个紧邻的周期且原子序数依次增大,它们相关信息如下:
X元素原子的价电子构型为nsnnp2n,Y和Z位于同一周期,最外层都有两个未成对电子L元素原子的基态未成对电子数是同周期最多的元素。
请回答如下问题:
(1)L元素在周期表中的位置是 。该原子核外电子排布式是 。其最高正价氧化物对应的水化物的化学式是 和 。
(2)元素X与Y形成的化合物晶体类型是 晶体,1mol该化合物含有的化学键数目为 (用阿伏加德罗常数NA表示)
(3)元素M是周期表中电负性最强的元素,X与M形成的化合物XM2的分子几何构型是 ,该化合物中X原子的杂化轨道类型是 。
(4)X与碳、氢三种元素形成的相对分子质量最小的分子里有 个σ键, 个π键
(5)金属元素N与Z形成的离子化合物的晶胞结构如图,晶胞中Z离子数目为 。
Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+的核外电子排布式是 。
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道接受NH3分子提供的 形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
a.稳定性:甲>乙,沸点:甲>乙
b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙
d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 。
【化学—物质结构与性质】W、X、Y、Z(W、X、Y、Z分别代表元素符号)均为元素周期表中前四周期的元素,其原子序数依次增大,其中W、X、Y为短周期元素,它们的单质在通常状况下均为无色气体。X元素的基态原子在同周期元素基态原子中含有的未成对电子数最多,Y元素的基态原子中s能级上的电子数等于p能级上的电子数,Z为金属元素,其基态原子是具有4s1结构的基态原子中质子数最多的原子,试回答下列各题:
(1)写出X的基态原子的核外电子排布式_________________;
(2)比较X、Y两元素基态原子的第一电离能大小:X_____Y(填“>”、“<”或“=”),理由是___________________;
(3)W、X两元素能形成一种常见气体M,每个M分子中含有l0个电子,M分子中心原子的杂化方式为______;W、X两种元素还能形成一种常见阳离子N,每个N中也含有10个电子,但在N与M中所含化学键的键角大小不同,其原因是______________;
(4)Z2+可与M分子在水溶液中形成[Z(M)4]2+,其中M分子和Z2+通过____________结合;
(5)单质Z的晶胞结构如图所示,则每个晶胞中含有原子Z的个数为______________。
[《物质结构与性质》选考题]现代世界产量最高的金属是Fe、Al、Cu。
(1)Fe、Al、Cu三种元素第一电离能由高到低的排序为 ;Fe2+的电子排布式为 。
(2)Cu(OH)2溶于浓氨水形成 色铜氨溶液;乙二酸( )分子中碳原子杂化类型为 ,分子中σ键比π键多 个。
)分子中碳原子杂化类型为 ,分子中σ键比π键多 个。
(3)以下变化伴随化学键破坏的是 (填下列选项标号)
| A.冰融化 | B.铝气化 | C.AlCl3溶于水 | D.胆矾受热变白 |
(4)二氧化硅晶体结构示意图如下,每个氧原子最近且等距离相邻 个氧原子。
(12分)X、Y、Z、R为短周期元素且原子序数依次增大。X、R原子核外电子层数等于其最外层电子数,Y元素的基态原子中电子分布在3个不同的能级,且每个能级中的电子总数相同;Z的两种同素异形体都存在于大气中,对生命起着重要作用。另有M元素位于周期表的第4周期第6列。请回答下列问题:
(1)上述5种元素中,电负性最大的是(填名称) ,X3Z+的VSEPR模型名称是 。
(2)M基态原子的电子排布式是 ;
(3)R的单质为面心立方最密堆积(见下图),则一个晶胞中R原子数为 ,R的配位数是 。
(4)已知:M2Z3与R2Z3结构和性质相似,则M2Z3溶于强碱时发生反应的离子方程式是 .
、
、
、
为原子序数依次增大的四种元索,
和
具有相同的电子构型;
、
为同周期元索,
核外电子总数是最外层电子数的3倍;
元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是(填元素符号),其中原子的核外电子排布式为。
(2)单质有两种同素异形体,其中沸点高的是(填分子式),原因是;
和
的氢化物所属的晶体类型分别为和。
(3)和
反应可生成组成比为1:3的化合物
,
的立体构型为,中心原子的杂化轨道类型为。
(4)化合物的立体构型为,中心原子的价层电子对数为,单质D与湿润的
反应可制备
,其化学方程式为。
(5)和
能够形成化合物
,其晶胞结构如图所示,晶胞参数,
=0.566
,
的化学式为:晶胞中
原子的配位数为;列式计算晶体F的密度(
)。
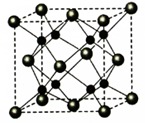
氟在自然界中常以的形式存在。
(1)下列关于的表述正确的是。
a.与
间仅存在静电吸引作用
b.的离子半径小于
,则
的熔点高于
c.阴阳离子比为2:1的物质,均与晶体构型相同
d.中的化学键为离子键,因此
在熔融状态下能导电
(2)难溶于水,但可溶于含
的溶液中,原因是(用离子方程式表示)。
已知在溶液中可稳定存在。
(3)通入稀NaOH溶液中可生成
,
分子构型为,其中氧原子的杂化方式为。
(4)与其他卤素单质反应可以形成卤素互化物,例如
、
等。已知反应
,
键的键能为
,
键的键能为
,则
中
键的平均键能为
。
的熔、沸点比
的(填"高"或"低")。
(12分)【选做题】本题包括A、B两小题,请选定一中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质]下列反应曾用于检测司机是否酒后驾驶:
2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
(1)Cr3+基态核外电子排布式为_________;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是________(填元素符号)。
(2)CH3COOH中C原子轨道杂化类型为______________;1molCH3COOH分子中含有δ键的数目为______。
(3)与H2O互为等电子体的一种阳离子为________(填化学式);H2O与CH3CH3OH可以任意比例互溶,除因为它们都是极性分子外,还因为___________。
选做【化学——物质结构与性质】化学中的某些元素是与生命活动密不可分的元素,请回答下列问题。
(1)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式是 。
(2)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。以下关于维生素C的说法正确的是 。
a.分子中既含有极性键又含有非极性键
b.1 mol 分子中含有4 mol π键
c.该物质的熔点可能高于NaCl
d.分子中所含元素电负性由大到小的顺序为O>C>H
(3)维生素C晶体溶于水的过程中要克服的微粒间作用力有 。
(4)KSCN溶液可用于Fe3+的检验,原因是铁离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物。Fe3+的价电子排布为 ,与之形成配合物的分子或离子中的配位原子应具备的结构特征是 。
(5)1183K以下纯铁晶体的晶胞如图1所示,1183K以上则转变为图2所示晶胞,则图1和图2中,铁原子的配位数之比为 。
【化学—物质结构与性质】前36号元素A、B、C、D的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半充满结构,C最外层电子数是电子层数的三倍。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均全充满。请回答下列问题:
(1)A、B、C第一电离能由小到大的顺序为______;基态D原子的价电子排布式为______。
(2)BC3-的空间构型为_______。
(3)1 molAB-中含有的 键数目为________个。
键数目为________个。
(4)已知镧镍合金LaNin晶胞(结构如图)体积为9.0×10-23cm2,,储氢后形成LaNinH3.5合金(晶胞体积不变,则n=________;氢在合金中的密度为________g/cm2(保留小数点后三位数字)。
[化学——选修3物质结构与性质]氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为______。氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化轨道类型为 。
(2)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气与氧化铝和碳在一定条件下反应生成X和CO,X的晶体结构如图所示,工业制备X的化学方程式为_______。
(3)X晶体中包含的化学键类型为______。(填字母标号)
| A.离子键 | B.共价键 | C.配位键 | D.金属键 |
(4)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,可能的原因是______
(5)若X的密度为pg/cm3,则晶体中最近的两个N原子的距离为______cm(阿伏加德罗常数用NA表示,不必化简)。