(10分)HN3称为叠氮酸,常温下为无色有刺激性气味的液体。N3-也被称为类卤离子。用酸与叠氮化钠反应可制得叠氮酸。而叠氮化钠可从下列反应制得:NaNH2+N2O=NaN3+H2O。HN3、浓盐酸混合液可溶解铜、铂、金等不活泼金属,如溶解铜生成CuCl2-。铜和铂的化合物在超导和医药上有重要应用,Cu的化合物A(晶胞如图,图中小黑球代表氧原子,其余大黑球为Y 、Cu 、Ba原子)即为超导氧化物之一,而化学式为Pt(NH3)2Cl2的化合物有两种异构体,其中异构体B可溶水,可用于治疗癌症。试回答下列问题:
(1)基态氮原子核外电子排布的轨道表示式为 。
(2)元素N、P、S的第一电离能(I1)由大到小的顺序为 。
(3)HN3属于 晶体,与N3-互为等电子体的分子的化学式 (写1种)NH2-的电子式为 ,其中心原子的杂化类型是 。
(4)CuCl2-中的键型为 ,1mol超导氧化物A晶胞中实际占有的氧原子的物质的量为 。
(5)治癌药物B的结构简式为 。
[化学——选修3: 物质结构与性质]Sn是人类最早使用的元素之一,能形成SnCl2,SnCl4两种氯化物,SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而SnCl4常温下为无色液体。白锡和灰锡是Sn的两种同素异形体,白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似。白锡的密度大于灰锡的密度。
(1)Sn元素价层电子排布式为 。
(2)SnCl2的一维链状聚合结构如图所示,在分子结构中标出所含有的配位键。其固体分子及气体分子中Sn的杂化方式为 。
(3)SnCl4分子的空间构型为 ,SnCl4与CCl4中
沸点较高的是 。
(4)锡的某种氧化物的晶胞如图,其化学式为 。
(5)解释白锡分子的密度大于灰锡的密度的原因: 。
(6)若灰锡的晶胞边长为a pm,计算灰锡的密度为 。
过渡元素具有较多的空轨道,所以第四周期的Cr、Fe、Co、Ni、Cu、Zn等多种金属能形成配合物。
(1)铬元素的基态原子的外围电子排布式是 。
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:
图中虚线表示的作用力为______________________;
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是 __,其中心原子的杂化轨道类型是 ___;
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。试推测四羰基镍的晶体类型是 ___,Ni(CO)4易溶于下列 __(用序号作答)。
| A.水 | B.四氯化碳 | C.苯 | D.硫酸镍溶液 |
(5)元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子最外层电子数是其内层的3倍。X与Y所形成化合物晶体的晶胞如图所示,该化合物的化学式为 ____。
【化学选修——3:物质的结构与性质】(15分)氧化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3气体和BN,如图所示:
请回答下列问题:
(1)基态B原子的电子排布式为________;基态N原子价电子排布图为________
(2)在BF3分子中,键角是________,B原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为________
(3)由B2O3制备BF3的化学方程式是_______________
(4)六方氮化硼晶体与石墨晶体结构相似,该晶体层间相互作用力为________
六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似(如下图所示),硬度与金刚石相当,已知立方氮化硼的晶胞边长为361.5 pm,则立方氮化硼的密度是_______g·cm﹣3(列式并计算。阿伏加德罗常数为NA)。
主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为________,W3分子的空间构型为________;
(2)X单质与水发生主要反应的化学方程式为________________;
(3)化合物M的化学式为________,其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是________。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有_____ ___,O—C—O的键角约为________;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X∶Y∶Z=________;
(5)含有元素Z的盐的焰色反应为_____ ___色。许多金属盐都可以发生焰色反应,其原因是___________________。
磁性材料氮化铁镍合金可用Fe(NO3)3、Ni(NO3)2、丁二酮肟、氨气、氮气、氢氧化钠、盐酸等物质在一定条件下反应制得。
(1)基态Ni原子的价电子排布式是 。
(2)丁二酮肟(结构式如图所示)中碳原子的杂化方式为 。
(3)NH3的沸点高于PH3,其主要原因是 。
(4)与N 3- 离子具有相同电子数的三原子分子的空间构型是 。
(5)向Ni(NO3)2溶液中滴加氨水,刚开始时生成绿色Ni(OH)2沉淀,当氨水过量时,沉淀会溶解,生成[Ni(NH3)6]2+的蓝色溶液,则1 mol [Ni(NH3)6]2+含有的σ键为 mol。
(6)下图是一种镍基合金储氢后的晶胞结构示意图。该合金储氢后,含1 mol La的合金可吸附H2的数目为 。
下图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
①B的水溶液呈弱酸性,其主要的电离方程式可表示为_________ ,D的化学式是_____ __。
②A、B、E中均含有的一种元素为___________ (填元素名称) 。
③E电子式为_________________。
④液态B与液态E反应可生成一种气态单质和一种常见液体,1molB参加反应放出热量QkJ,其反应的热化学方程式为_______ _______。
⑤NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl。试写出E与足量盐酸时,发生反应的化学方程式 。
本题包括两道题
(1)下面是s能级p能级的原子轨道图,试回答问题: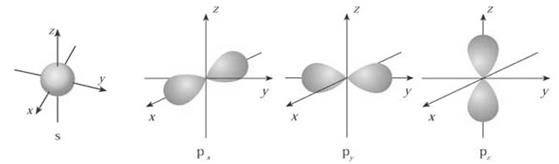
s电子的原子轨道呈 形,每个s能级有 个原子轨道;
p电子的原子轨道呈 形,每个p能级有 个原子轨道。
(2)A、B、C、D、E都是元素周期表中前20号的元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。A和E可组成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子(用“●”表示)位于该正方体的顶点或面心;阴离子(用“○”表示)位于小正方体的中心。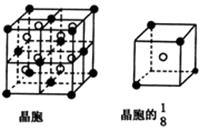
根据以上信息,回答下列问题:A至E的元素名称:
A ;B ;C ;D ;E
(15分)元素周期表第ⅤA族元素包括氮、磷、砷(As)、锑(Sb)等。这些元素无论在研制新型材料,还是在制作传统化肥、农药等方面都发挥了重要的作用。请回答下列问题:
(1)N4分子是一种不稳定的多氮分子,这种物质分解后能产生无毒的氮气并释放出大量能量,能被应用于制造推进剂或炸药。N4是由四个氮原子组成的氮单质,其中氮原子采用的轨道杂化方式为sp3,该分子的空间构型为________,N—N键的键角为________。
(2)基态砷原子的最外层电子排布式为________。
(3)N、P、As原子的第一电离能由大到小的顺序为____________(用元素符号表示)。
(4)叠氮化钠(NaN3)用于汽车安全气囊中氮气的发生剂,写出与N3-互为等电子体的分子的化学式________(任写一种即可)。
(5)天然氨基酸的命名常用俗名(根据来源与性质),例如,最初从蚕丝中得到的氨基酸叫丝氨酸[HOCH2CH(NH2)COOH]。判断丝氨酸是否存在手性异构体?________(填“是”或“否”)
(6)砷化镓为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。已知立方砷化镓晶胞的结构如图所示,其晶胞边长为c pm,则密度为_______g·cm-3(用含c的式子表示,设NA为阿伏加德罗常数的值),a位置As原子与b位置As原子之间的距离为________pm(用含c的式子表示)。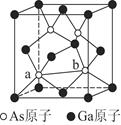
(12分)【化学—物质结构与性质】
(1)下列叙述正确的是________。
a.含有金属阳离子的晶体一定是离子晶体
b.化合物硫氰化铁和氢氧化二氨合银中都存在配位键
c.KCl、HF、CH3CH2OH、SO2都易溶于水,且原因相同
d.MgO的熔点比NaCl的高,主要是因为MgO的晶格能大于NaCl的晶格能
(2)氨基酸是蛋白质的基石,甘氨酸是最简单的氨基酸(结构如图),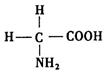
在甘氨酸分子中,N 原子的杂化形式是_____,在甘氨酸分子中C、N、O原子的第一电离能从大到小的顺序是_______;氮可以形成多种离子,如N3-、NH2-、NH4+、N2H5+等,其中,NH4+的空间构型是____。
(3)已知MO与CsCl的结构相似(如图所示),MO晶体的密度为p g·cm-3,NA为阿伏加德罗常数,相邻的两个M2+的核间距为acm。写出Cs基态原子的价电子排布式______,MO的相对分子质量可以表示为_____。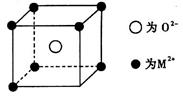
翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅。
(1)Na、Al、Si、O四种元素电负性由大到小的顺序为 。
(2)Cr3+的基态核外电子排布式为 。
(3)Cr可形成配合物K[Cr(C2O4)2(H2O)2],与H2O互为等电子体的一种分子是 (填化学式),草酸根离子(C2O42-)中碳原子的杂化方式为 ,1 mol H2C2O4分子中含有的σ键的数目为 。
(4)Cr和Ca可以形成一种具有特殊导电性的复合氧化物,晶胞如图所示。当该晶体中部分Ca2+被相同数目的La3+替代时,部分铬由+4价转变为+3价。若化合物中La3+和Ca2+的物质的量之比为 (x<0.1),三价铬与四价铬的物质的量之比为 。
(x<0.1),三价铬与四价铬的物质的量之比为 。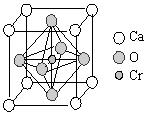
[物质结构]X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;Z基态原子的M层与K层电子数相等;R2+的3d轨道有9个电子。
请回答下列问题:
(1)Y基态原子的电子排布式是 ;
(2)Z所在周期中第一电离能最大的主族元素是 。
(3)XY2—的立体构型是 ;
(4)Z与某元素形成的化合物的晶胞如图所示,晶胞中阴离子与阳离子的个数比是 。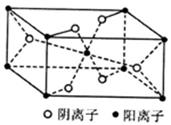
(5)将R单质的粉末加入X气态氢化物的浓溶液中,不断鼓入空气充分反应,得到深蓝色的[R(NH3)4](OH)2溶液,该反应的离子方程式是 ;1mol [R(NH3)4]2+中含有的σ键的数目是 。
选做(12分)【化学——物质结构与性质】X、Y、Z为前四周期元素,且原子序数依次增大。X与氢元素可形成:H2X、H2X2两种化合物,且在常温下均为液态;Y基态原子的M层电子数是K层的3倍;Z2+的3d轨道中有10个电子。请回答下列问题:
(1)X所在周期中第一电离能最大的主族元素是_______(填元素符号);H2X2分子中X原子的杂化方式是_______。
(2)Y与X可形成YX42-。
①YX42-的立体构型是_____________。
②写出一种与YX42-互为等电子体分子的化学式__________。
(3)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为_________。
(4)Y与Z形成化合物晶体的晶胞如图所示。已知该晶体的密度为a g·cm-3,则该晶胞的体积为___________cm3(NA表示阿伏加德罗常数的值)。
氮元素可形成卤化物、叠氮化物及络合物等。
(1)在铜催化作用下F2和过量NH3反应得到NF3,其分子立体构型为_____________;NF3是_________键结合形成的___________分子(填极性或非极性)。固态NF3晶体熔点比冰______________(填高或低)。
(2)氢叠氮酸(HN3)是一种弱酸,它的酸性类似于醋酸,微弱电离出H+和N3-。
①与N3-互为等电子体的分子有: (举2例),由此可推知N3-的立体构型是 型。
②叠氮化物、氰化物能与Fe3+及Cu2+及Co3+等形成络合物,如:[Co(N3)(NH3)5]SO4、Fe(CN)64-。写出钴原子在基态时的电子排布式: ;[Co(N3)(NH3)5]SO4中钴的配位数为 ;配位原子结构特征是________;CN-的电子式是 。
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)=2Na(l)+3N2(g),有关说法正确的是 (选填序号)
| A.NaN3与KN3结构类似,前者晶格能较小 |
| B.第一电离能(I1):N>P>S |
| C.钠晶胞结构如上图,该晶胞分摊2个钠原子 |
| D.氮气常温下很稳定,是因为氮的电负性大 |
(4)化学式为Pt(NH3)2Cl2的化合物有两种异构体,其中一种异构体可溶于水,该种异构体的结构可用示意图表示为 。
(5)三氯化铁常温下为固体,熔点282 ℃,沸点315 ℃,在300 ℃以上易升华。易溶于水,也易溶于醚、丙酮等有机溶剂。据此判断三氯化铁晶体类型为____________;
(6)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为________。
下表是元素周期表的一部分,回答下列问题(答题时用具体元素符号表示)。
| ① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
② |
|
|
|
|
|
|
|
|
|
|
|
③ |
④ |
⑤ |
|
|
| ⑥ |
|
|
|
|
|
|
|
|
|
|
|
⑦ |
|
|
|
⑧ |
|
| |
|
|
|
|
|
|
⑨ |
|
|
⑩ |
|
|
|
|
|
|
|
(1)①、③形成的6原子气态化合物中含 个σ键, 个π键。
(2)元素⑨的原子核外次外层电子数为 个。焊接钢轨时,常利用元素⑨的氧化物与⑦的单质在高温下发生反应,写出其中一种反应的化学方程式 。
(3)④、⑤两元素原子第一电离能较大的是 ,两元素以质量比7:12组成的化合物A是一种高效火箭推进剂,相对分子质量为152,A的分子式为 。
(4)⑥和⑧可形成某离子化合物,下图所示结构 (选填“能”或“不能”)表示该离子化合物的晶胞;下图所示结构中,X离子的堆积方式为 (选填“ABAB…”或“ABCABC…”)。
(5)元素⑩单质的晶胞如图所示,该晶胞中金属原子的配位数为 ,每个晶胞“实际”拥有的原子数是 。