糖类、油脂、蛋白质都是人体必需的营养物质。
(1)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和_____________(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和____________(写结构简式或名称)。人体中共有二十多种氨基酸,其中人体自身_______________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
(3)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:_______________。
(4)蛋白质在一定条件下能发生变性,从而失去生理活性。万一误服硫酸铜溶液,此时应立即作怎样的处理? 。
由葡萄糖发酵可得乳酸,为研究乳酸的分子组成和结构,进行了下述实验:
(1)称取乳酸0.9 g,在某种状况下使其完全气化,相同状况下同体积的H2的质量为0.02 g,则乳酸的相对分子质量为 g。
(2)若将上述乳酸蒸气在氧气中燃烧只生成CO2和H2O(g),当全部被碱石灰吸收时,碱石灰的质量增加1.86 g;若将此产物通入过量石灰水中,则产生3.00 g白色沉淀。则乳酸的分子式为 。
(3)另取0.90 g乳酸,若与足量金属钠反应,生成H2 2240 mL(标准状况),若与足量碳酸氢钠反应,生成224 mL CO2(标准状况),则乳酸的结构简式可能为 或 。
(4)若葡萄糖发酵只生成乳酸,其反应的化学方程式为 。
水解反应是中学化学中的一大类反应。
(1)在 ①酸 ②碱 ③盐 ④不饱和烃 ⑤卤代烃 ⑥醇 ⑦醛 ⑧酯 ⑨低聚糖 ⑩蛋白质等物质中,能发生水解的物质有 (填编号)。蔗糖水解的产物名称为 。
(2)写出二甲基二氯硅烷[(CH3)2SiCl2 ]水解得到二甲基硅二醇的化学方程式: 。
(3)溴乙烷水解实验的操作为:取一支试管,加入0.5 mL溴乙烷,再加入2 mL 5% 的NaOH溶液,充分振荡后静置,待液体分层后,用滴管小心吸取10滴上层水溶液,转入另一盛有10 mL稀HNO3溶液的试管中,然后加入3滴2 % 的AgNO3溶液,观察反应现象。
请根据上述操作回答以下问题:
①本实验中涉及溴乙烷的物理性质主要有 ,稀HNO3的作用是 。
②甲同学在盛溴乙烷和NaOH溶液的试管口塞紧带长玻璃管的单孔橡皮塞,然后水浴加热数分钟,最后液体不再分层。反应的化学方程式为 。
③乙同学认为:要证明上述实验中溴乙烷发生了水解反应,需要先做一个对比实验证明溴乙烷自身不能电离出溴离子,此实验操作步骤和现象是 。
糖尿病是由于人体内胰岛素紊乱导致的代谢紊乱综合征,以高血糖为主要标志。长期摄入高热量食品或缺少运动,都会导致糖尿病。
(1)血糖是指血液中的葡萄糖,下列有关说法正确的是___________。
A.葡萄糖分子可表示为C6(H2O)6,则每个葡萄糖分子含有6个H2O分子
B.葡萄糖与果糖互为同分异构体
C.糖尿病人尿糖较高,可用新制的氢氧化铜来检测人尿液中的葡萄糖
D.淀粉水解的最终产物是氨基酸
(2)糖尿病人不可过量饮酒,将会一定程度上造成胰岛细胞损伤。但酒精在肝脏内可转化成有机物A。A的实验结果如下:
① 通过实验测得A的相对分子质量为60;
② A由C、H、O三种元素组成,分子中只存在两种类型的氢原子,且这两种类型的氢原子个数比为1∶3
③ A可与酒精在一定条件下生成有芳香气味的物质。
纯净的A又称为______________,结构简式为____________________。
A的主要化学性质有(用化学方程式表示):a____________________________________,
b___________________________________________。
Ⅰ.充分燃烧1.4 g某有机物A生成4.4 gCO2和1.8 g H2O,该有机物蒸气的密度是相同条件下H2密度的28倍。
(1)该有机物的分子式为________。
(2)A的链状同分异构体共________种。
(3)A的链状同分异构体中含有支链的同分异构体的结构简式为________,其系统命名为________。
(4)B是A的某种同分异构体,B的磁共振氢谱中只有4个信号峰(即只有4种氢原子),B通入Br2的CCl4溶液褪色,生成化合物C。则由B生成C的化学方程式为________。
Ⅱ.油脂是高级脂肪酸甘油酯,在工业上用途广泛。
(1)以硬脂酸甘油酯为例写出油脂的皂化反应方程式为
(2)从皂化反应后的溶液中提取肥皂和甘油的过程如下:
加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是 。
食品安全关系国计民生,影响食品安全的因素很多。
(1)聚偏二氯乙烯( )具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
)具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
(2)劣质植物油中的亚油酸[CH3(CH2)4—CH===CH—CH2—CH===CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是_________。
| A.分子式为C18H34O2 |
| B.一定条件下能与乙酸发生酯化反应 |
| C.能和NaOH溶液反应 |
| D.能使酸性KMnO4溶液褪色 |
(3)假酒中甲醇(CH3OH)含量超标,请写出Na和甲醇反应的化学方程式:_________________。
(4)三类营养物质之一的淀粉最终的水解产物是葡萄糖。请设计实验证明淀粉已经全部水解,写出操作、现象和结论:______________________________________________。
A、B、C、X是中学化学常见物质,它们在一定条件下具有如下转化关系:
A + X → B + C + H2O
(1)若X是淀粉水解的最终产物,B为砖红色难溶于水的氧化物。
①X的化学式为 。
②A溶于硝酸的离子方程式为 。
③将淀粉水解液中和后,与A的悬浊液(含NaOH)共热至沸腾,产生砖红色沉淀则证明淀粉已经水解。若要进一步探究淀粉是否完全水解,还需用到的试剂是 。
(2)若A是由M+和R-构成的盐,X为二元强碱,B为气体。
①B与氧气一定条件下可以发生置换反应,当生成18g液态水时,放出能量Q kJ,该反应的热化学方程式为 ;若将该反应设计成燃料电池(以硫酸溶液为电解质溶液),其负极反应式为 。
②室温时,20mL 0.10mol·L-1的B溶液用0.050mol·L-1的硫酸溶液滴定,所得滴定曲线如图所示。曲线上a点,c(M+) c(SO42-)(填“>”、“<”或“=”)。曲线上b点,溶液中c(H+)≈ (只保留一位有效数字)。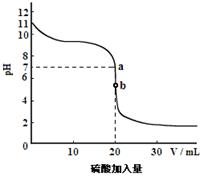
(9分)I.按要求完成下列问题
(1) 系统命名为 ,
系统命名为 ,
(2)写出间﹣甲基苯乙烯的结构简式 ,
(3)2,2二甲基丙烷的习惯命名为 ,
(4)写出4﹣甲基﹣2﹣乙基﹣1﹣戊烯的键线式 。
II.糖类、油脂、蛋白质都是人体必需的营养物质。
(1)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和A,举一例说明A物质的用途 。
(2)氨基酸是组成蛋白质的基本结构单元,甘氨酸的结构简式为:NH2CH2COOH,丙氨酸的结构简式为: CH3CH(NH2)COOH。甘氨酸和丙氨酸混合发生缩合,能生成 种二肽化合物。
(3)淀粉的水解产物为葡萄糖(C6H12O6),检验水解产物是葡萄糖的实验过程为:
①在淀粉中加入硫酸后加热一段时间,②加入 ,③加入新制Cu(OH)2溶液,煮沸。写出③的化学方程式 。
油脂是高级脂肪酸的甘油酯,在工业上用途广泛。
实验一:用地沟油制肥皂(高级脂肪酸钠盐)和甘油(常压下甘油的沸点为290℃)。
32将约6g地沟油、10mL 40%的烧碱溶液、5mL液体A混合后在烧杯中加热约0.5小时。A可以增大反应物间的接触,则A可以是 _____(选填编号)。
a.四氯化碳 b.汽油 c.乙醇
33.从皂化反应后的溶液中提取肥皂和甘油的过程如下:

加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是 。操作②必须用到的玻璃仪器是_____(选填编号)。
a.漏斗 b.分液漏斗 c.蒸馏烧瓶
34.若甘油的产率明显低于高级脂肪酸钠盐的产率,可能的原因是_____(选填编号)。
a.油脂水解不充分 b.部分甘油挥发 c.甘油中混有水
实验二:测定油脂的碘值。碘值是指100g油脂中所能吸收(加成)碘的克数。
称取a g某油脂,加入含bmol I2的溶液(韦氏液),充分振荡;过量的I2用cmol/L Na2S2O3溶液滴定(以淀粉为指示剂):2Na2S2O3+ I2 =Na2S4O6+ 2NaI用去vmL。
35.配制韦氏液,溶剂选用冰醋酸而不选用水的原因是 。
滴定终点时颜色的变化是 。
36.该油脂的碘值为(用相关字母表示) 。
37.冰醋酸也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏_____(选填“高”或“低”)。
F是新型降压药替米沙坦的中间体,可由下列路线合成:
F
(1)A→B的反应类型是________,D→E的反应类型是________,E→F的反应类型是________。
(2)写出满足下列条件的B的一种同分异构体_____________________________(写结构简式)。
①含有苯环 ②含有酯基 ③能与新制Cu(OH)2悬浊液反应
(3)C中含有的官能团名称是________。已知固体C在加热条件下溶于甲醇,下列C→D的有关说法正确的是________。
a.使用过量的甲醇是为了提高D的产量
b.浓硫酸的吸水性可能会导致溶液变黑
c.甲醇既是反应物,又是溶剂
d.D的化学式为C9H9NO4
(4)E的同分异构体苯丙氨酸经缩合反应形成的高聚物是____________________(写结构简式)。
(5)已知 在一定条件下可水解为
在一定条件下可水解为 ,F在强酸和长时间加热条件下发生水解反应的化学方程式是
,F在强酸和长时间加热条件下发生水解反应的化学方程式是
________________________________________________________________________
________________________________________________________________________。
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,机动车废气排放已成为城市大气污染的重要来源。
(1)设汽油成分为C8H18,若在气缸中汽油高温裂解产生丁烷和丁烯,写出该反应的化学方程
。
(2)气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g) △H >0
2NO(g) △H >0
①汽车启动后,气缸内温度越高,单位时间内NO排放量越大,原因是 。
②1mol空气中含有0.8molN2和0.2molO2,1300℃时在含1mol空气的密闭容器内反应达到平衡。测得NO为8×10-4mol。计算该温度下的平衡常数K≈ 。
(3)尾气中的CO主要来自于汽油不完全燃烧。
①有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g) △H=+221kJ·mol-1, 简述该设想能否实现的依据: 。
②测量汽车尾气的浓度常用电化学气敏传感器,其中CO传感器可用下图简单表示,则阳极发生的电极反应为 。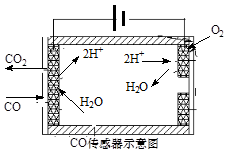
(4)在汽车尾气系统中安装催化转换器,可有效减少尾气中的CO、NOx 和碳氢化合物等废气。
已知:N2(g)+O2(g)=2NO(g) △H1=+180kJ/mol
CO(g) +1/2O2(g)= CO2(g) △H2=-283kJ/mol
2NO(g)+ 2CO(g) = 2CO2(g) + N2(g) △H3
则△H3 = kJ·mol-1。
(5)光化学烟雾(含臭氧、醛类、过氧乙酰硝酸酯等)是汽车尾气在紫外线作用下发生光化学反应生成的二次污染物。写出2-丁烯与臭氧按物质的量之比为1:2反应生成乙醛及氧气的化学方程式 。
现有通式为(CH2O)n的六种有机物,性质如下:
①甲是无色有刺激性气味的气体,可以发生银镜反应;
②乙、丙、丁的相对分子质量均为甲的2倍,戊的相对分子质量是甲的3倍,己的相对分子质量是甲的6倍;
③乙、戊的水溶液可使紫色石蕊试液变红,还可以与乙醇在一定条件下酯化,乙和戊之间也能酯化;
④戊结构中含有—CH3,两分子戊可形成环状酯;
⑤丙不溶于水;丁、己两种物质的水溶液均呈中性;丙既能水解,又能发生银镜反应;丁能与钠反应放出H2,且能与新制Cu(OH)2悬浊液加热反应产生红色沉淀;己能发生银镜反应,它可由淀粉水解制得。
(1)推断各物质的结构,写出其结构简式。
甲________,乙________,丙________,
丁________,戊________,己________。
(2)甲~己中能与NaOH溶液反应的是________,(填序号,下同)能发生酯化反应的是________,能被H2还原为醇的是________,能发生银镜反应的是________。
糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志。长期摄入高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖(C6H12O6)。下列说法正确的是________。
A.葡萄糖属于碳水化合物,其分子式可表示为C6(H2O)6,则每个葡萄糖分子中含6个H2O
B.糖尿病人尿糖高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C.葡萄糖为人体提供能量
D.淀粉水解的最终产物是葡萄糖
(2)木糖醇[CH2OH(CHOH)3CH2OH]是一种甜味剂,糖尿病人食用后血糖不会升高。请预测木糖醇的一种化学性质:___________________。
(3)糖尿病人不可饮酒,酒精在肝脏内可被转化成有机物A。
A的有关性质实验结果如下:
Ⅰ.通过样品的质谱测得A的相对分子质量为60。
Ⅱ.核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:乙醇(CH3CH2OH)有三种氢原子(图甲)。经测定,有机物A的核磁共振氢谱示意图如图乙所示。
Ⅲ.将A溶于水,滴入石蕊试液,发现溶液变红。
试写出A的结构简式:________________________________。
(4)糖尿病人宜多吃蔬菜和豆类食品。蔬莱中富含纤维素,豆类食品中富含蛋白质。下列说法错误的是________(填序号)。
A.蛋白质都属于天然有机高分子化合物,且都不溶于水
B.用灼烧闻气味的方法可以区别合成纤维和羊毛
C.人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
D.紫外线、医用酒精能杀菌消毒,是因为它们能使细菌的蛋白质变性
E.用天然彩棉制成贴身衣物可减少染料对人体的副作用
(5)香蕉属于高糖水果,糖尿病人不宜食用。乙烯是香蕉的催熟剂,它可使溴的四氯化碳溶液褪色,试写出该反应的化学方程式:__________________。
葡萄糖是一种重要的营养物质,应用范围十分广泛。
I.在某些酶的催化下,人体内葡萄糖的代谢有如下过程:
(1)过程①是_______反应,过程②是_______ 反应,过程③是_______反应(填写反应类型的名称)。
(2)上述物质中_______和_______互为同分异构体(填写字母代号)。
Ⅱ.葡萄糖被氧化后生成葡萄糖酸,形成内酯(具有六元环酯结构)。葡萄糖酸内酯简称GDL,是一种食品添加剂,超市中见到的内脂豆腐就是用它点成的。方法是把GDL和CaSO4(或其他凝固剂)按1:3~2:3配比混合使用。用它点出的豆腐更加细嫩,营养价值也高。
(3)葡萄糖酸的分子式为_______。
(4)葡萄糖酸内酯的结构简式为 _______。
成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成份的存在,请你参与并协助他们完成相关实验。
(1)用小试管取少量的苹果汁,加入 ,溶液变蓝,则苹果中含有淀粉。
(2)用小试管取少量的苹果汁,加入新制Cu(OH)2悬浊液,并加热,产生砖红色的沉淀,则苹果中含有 (写分子式)。
(3)葡萄糖在一定条件下可以得到化学式为C2H6O的化合物A。
A + CH3COOH→有香味的产物
① 含A的体积分数为75%的水溶液可以用做 。
②写出化合物A与CH3COOH反应的化学方程式为 ,该反应的类型为 。
(4)苹果中含有苹果酸,测得其相对分子质量为134。取0.02mol苹果酸,使其完全燃烧,将燃烧后的产物先后通过足量的无水CaCl2和碱石灰,两者分别增重1.08g 和 3.52g。则分子中C、H原子的个数比 。苹果酸的分子式是 。