铁制自来水管与下列材料做成的水龙头连接,锈蚀最快的铁水管所连接的是
| A.塑料水龙头 | B.铁水龙头 | C.铜水龙头 | D.陶瓷水龙头 |
用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是
| A.溶液pH≤2时,生铁发生析氢腐蚀 |
| B.在酸性溶液中生铁可能发生吸氧腐蚀 |
| C.析氢腐蚀和吸氧腐蚀的速率一样快 |
| D.两溶液中负极反应均为:Fe﹣2e﹣=Fe2+ |
有关金属的腐蚀与防护的叙述正确的是
| A.金属的化学腐蚀比电化学发生普遍 |
| B.上图装置的原理是“牺牲阳极的阴极保护法” |
| C.金属腐蚀的本质是M-ne-→Mn+而被损耗 |
| D.用铝制铆钉来接铁板,铁板易被腐蚀 |
有一合金由X、Y、Z、W四种金属组成,若将合金放入盐酸中只有Z、Y能溶解;若将合金置于潮湿空气中,表面只出现Z的化合物;若将该合金做阳极,用X盐溶液作电解液,通电时四种金属都以离子形式进入溶液中,但在阴极上只析出X。这四种金属的活动性顺序是( )
| A.Y>Z>W>X | B.Z>Y>W>X |
| C.W>Z>Y>X | D.X>Y>Z>W |
以下现象与电化学腐蚀无关的是:
| A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B.生铁比纯铁更易生锈 |
| C.铁质配件附有铜质配件,在接触处易生铁锈 |
| D.银质物品久置表面变暗 |
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
| A.4Fe(OH)2+2H2O+O2=4Fe(OH)3↓ | B.2Fe+2H2O+O2=2Fe(OH)2↓ |
| C.2H2O+O2+4e-=4OH- | D.Fe-3e-=Fe3+ |
下列有关金属腐蚀与防护的说法正确的是( )
| A.纯银器表面在空气中会因化学腐蚀渐渐变暗 |
| B.地下输油钢管与外加直流电源的正极相连可保护其不受腐蚀 |
| C.海轮外壳连接锌块是采用牺牲阴极的阳极保护法保护外壳不受腐蚀 |
| D.当镀锡铁制品的镀层破损时,锡镀层仍能对铁制品起保护作用 |
下列与金属腐蚀有关的说法正确的是
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池放电腐蚀主要是由MnO2的氧化作用引起的 |
24.(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》
(4分)性能各异的各种材料的广泛应用大大提高了人们的生活水平。回答问题:
(1)家庭中“钢精锅”是由铝合金做成的,在烧菜时能否放大量醋炖煮? 。(填能或否)
(2)下列关于铁制品保护措施的说法中不正确的有 (填序号)。
A.在自行车钢圈上镀上一层金属铬,摩擦部位加上机油或黄油
B.相同条件下,马口铁(表层镀锡)与白铁(表层镀锌)相比,马口铁更为耐用
C.在海轮的外壳上常焊有锌块,且定期更新
D.将不锈钢制成刀具和餐具,有的刀具还进行烤蓝处理
(3)在快中子反应堆中得以广泛应用的钠钾合金,这个事实说明合金的熔点比其成分金属的熔点 (填字母)。
a.高 b.低 c.可能高也可能低
(4)轨道交通建设需要大量金属材料。下列金属材料最容易发生腐蚀的是 (填字母)
a、铝合金 b、钢铁 c、纯度很高的铁
(12分)铁在地壳中的含量约占 5 %左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是 Fe2O3)等。
(1)红热的铁能跟水蒸气反应,一种产物与磁铁矿的主要成分相同,另一种产物是可燃性气体,则其反应的化学方程式为 。该可燃气体在酸性条件下,可制成燃料电池,写出该气体发生的电极反应式 。
(2)在常温下,铁跟水不起反应。但在潮湿的空气中,铁很容易生锈(铁锈的主要成分是 Fe2O3)而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。铁生锈的化学原理如下,请你用离子方程式和化学方程式补充完整。
①原电池反应:
负极:2Fe-4e-=2Fe2+、正极: ;
②氢氧化物的形成: Fe2 + + 2OH-= Fe(OH)2↓ 。
③氢氧化物的分解: 2Fe(OH)3 =Fe2O3+3H2O。
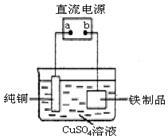
(3)为了防止铁生锈,可在铁制品表面镀上一层铜(如图装置),a为 (填“正极”或“负极”),铁制品表面发生的电极反应式 为 。
下列叙述与电化学腐蚀无关的是
| A.切过咸菜的菜刀不及时清洗易生锈 |
| B.线路连接时,有经验的电工从不把铝导线和铜导线接在一起 |
| C.银质奖章久置后表面逐渐变暗 |
| D.在轮船的尾部和船壳的水线以下,常装有一定数量的锌块 |
将一根生铁棒垂直浸入水中,由于深水处溶解氧气量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是
| A.铁棒AB段发生反应为O2 + 4e- + 2H2O = 4OH- |
| B.腐蚀过程中在铁棒上会产生微电流 |
| C.向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响 |
| D.产生这种现象是因为铁棒发生了电化学腐蚀 |
下列叙述不正确的是
| A.锌跟稀硫酸反应制取氢气,加入少量的硫酸铜能加快反应速率 |
| B.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀 |
| C.为保护海轮的船壳,常在船壳外面镶上锌块 |
| D.钢铁在发生析氢腐蚀和吸氧腐蚀时,负极反应是相同的 |
下列叙述,其中正确的是
①电解池是将化学能转变成电能的装置
②原电池是将电能转变成化学能的装置
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤电镀过程相当于金属的“迁移”,可视为物理变化
| A.①②③④ | B.③④ | C.③④⑤ | D.④ |