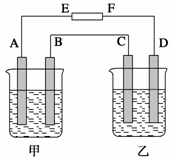
下图为相互串联的甲、乙两电解池试回答:

(1)若甲池利用电解原理在铁上镀银,则A是 (填电极材料),电极反应式是 ;B是 (填电极材料),电极反应式是 ,应选用的电解质溶液是 。
(2)乙池滴入少量酚酞试液,电解一段时间, (填“C”或“Fe”)极附近呈红色。
(3)若甲槽阴极增重43.2g,则乙槽中阳极上放出的气体在标况下的体积是 _________L。
如图装置,A、B中电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极。若在A、B中充满KOH溶液后倒立于KOH溶液的水槽中,切断K1,闭合K2、K3,通直流电,则:
(1)标出电源的正、负极,a为______________极。
(2)在湿的Na2SO4滤纸条中心滴KMnO4溶液,现象为___________________。
(3)写出电极反应式:A中____________________B中__________________。
(4)若电解一段时间,A、B中均有气体包围电极。此时切断K2、K3,闭合K1。电流表的指针偏转,则此时A极电极反应式为_________________________。
如图为相互串联的甲乙两个电解池,甲池若为电解精炼铜的装置,请回答:

(1)A极材料和B极材料分别是
a.石墨、精铜 b.石墨、粗铜 c.粗铜、精铜 d.精铜、粗铜
(2)电解质溶液为 。
(3)若甲槽阴极增重12.8g,则乙槽阴极放出气体在标准状况下的体积为 。
(4)若乙槽剩余液体为400mL,求电解后得到碱液的物质的量浓度 。
(9分)如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)B极是电源的 ,一段时间后,甲中溶液颜色 ,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 ,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 。
(3)现用丙装置给铜件镀银,则H应该是 (填“镀层金属”或“镀件”),电镀液是 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 ,甲中溶液的pH (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是 。
(10分) (1)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的________腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的________极(填“正”或“负”)相连。
(2)基态Fe原子有 个未成对电子,Fe2+的电子排布式为 。可用铁氰化钾溶液检验 Fe2+,发生反应的离子方程式为 。
(3)用惰性电极电解200mL一定浓度的硫酸铜溶液(不考虑电解过程中溶液体积变化),通电一段时间后,若向所得的溶液中加入0.1molCu (OH)2,溶液恰好恢复到电解前的浓度和pH,则电解过程中转移电子的物质的量为________ mol。
(4)用铂作电极电解AlCl3溶液的总反应离子方程式为 。
据报道,苹果公司开发了一种以液态甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.下图是一个电化学过程的示意图.

已知甲池的总反应式为:2CH3OH+3O2+4KOH K2CO3+6H2O 请填空:
K2CO3+6H2O 请填空:
(1)充电时:①原电池的负极与电源______极相连,②阳极的电极反应为________.
(2)在此过程中若完全反应,乙池中B极的质量增加648g,则甲池中理论上消耗O2____L(标准状况下).
(3)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为 。
在如图中,甲烧杯中盛有100 mL 0.50 mol/L AgNO3 溶液,乙烧杯中盛有100 mL 0.25 mol/L CuCl2溶液,A、B、C、D均为 质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9 g。
(1)电源E为________极
(2)A极的电极反应式为______________,析出物质______ mol。
(3)B极的电极反应式为______________,析出气体______ mL(标准状况)。
(4)D极的电极反应式为______________,析出气体______ mL(标准状况)。
(5)甲烧杯中滴入石蕊试液,________极附近变红,如果继续电离,在甲烧杯中最终得到______溶液。
如图所示3套实验装置,分别回答下列问题: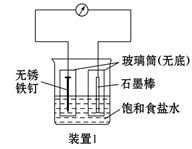
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入KSCN溶液呈无色,再滴入氯水即可观察到铁钉附近的溶液变红色,表明铁被_______;向插入碳棒的玻璃筒内滴入酚酞试液,可观察到碳棒附近的溶液变红,该电极反应为_______________。
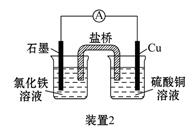
(2)装置2中的石墨是_________极(填“正”或“负”),该装置发生的总反应的离子方程式为__________。
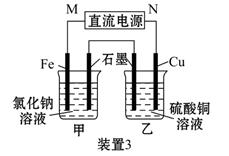
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨电极附近首先变红。
①电源的M端为_________极,甲烧杯中铁电极的电极反应为________________;
②乙烧杯中电解反应的离子方程式为______________;
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,则甲烧杯中产生的气体在标准状况下为________ mL。
某化学研究性学习小组的同学在学习了电化学相关知识后,将所学知识整合得到如图所示装置,用于电解饱和食盐水。
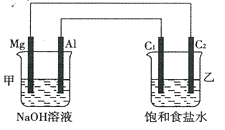
请回答下列问题:
(1)甲池中Al极为 极,乙池中C2极为 极;
(2)甲池中发生反应的总化学方程式为 ;
(3)若向乙池中滴加酚酞试液,则C1极附近观察到的现象为 ,C2极的电极反应式为 ;
(4)当C1极析出224mL气体(标准状况)时,转移电子的物质的量为 。
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
 (1)该电池的负极材料是_________。电池工作时,电子流向____________(填“正极”或“负极”)。
(1)该电池的负极材料是_________。电池工作时,电子流向____________(填“正极”或“负极”)。
 (2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是__________。欲除去Cu2+,最好选用下列试剂中的__________(填代号)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是__________。欲除去Cu2+,最好选用下列试剂中的__________(填代号)。
 a.NaOH b.Zn c.Fe d.NH3·H2O
a.NaOH b.Zn c.Fe d.NH3·H2O
 (3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 __________。若电解电路中通过2 mol电子,MnO2的理论产量为_______g。
__________。若电解电路中通过2 mol电子,MnO2的理论产量为_______g。
如下图所示,甲、乙为相互串联的两电解池。

试回答:
(1)乙池中Fe电极为 极。若在乙池中滴入少量酚酞试液,开始电解一段时间后,铁电极附近呈 色。
(2)甲池若为精炼铜(假设粗铜的组成是均匀的,且其中活泼和不活泼的成份均存在)的装置,则电解质溶液可以是 ;通过一段时间后,A电极增重12.8g,则甲池溶液原溶质的浓度 (填“增大”、“减小”、“不变”或“无法确定”),乙池石墨电极放出的气体在标准状况下的体积为 。
如图所示装置,X、Y为电源的两极,a、b均为石墨电极,c为铜电极,d为铁电极,A槽中盛装饱和食盐水,B槽中盛装CuCl2溶液。通电一段时间后,发现d电极上覆盖一层红色物质。
根据以上实验事实,回答下列问题:
(1)c极的电极反应式为 ;
(2)A槽中发生反应的离子方程式为 ;
(3)A槽中溶液的pH (填“变大”、“变小”或“不变”)。
(12分)(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式: 。若1g水蒸气转化成液态水放热2.5kJ,则氢气的燃烧热为△H= kJ/mol。
(2)近年来已经研制出甲烷(CH4)燃料电池,该电池的电解质溶液为H2SO4溶液,写出该电池负极的电极反应式:____________________。该电池总反应式:________________________。
(3)用惰性电极电解AgNO3溶液,写出该电解反应的化学方程式 ;若在阳极收集到0.32 g O2,中和电解生成的酸需0.4 mol·L-1 NaOH溶液 mL。
金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是 。
| A.Fe2O3 | B.NaCl | C.Cu2S | D.Al2O3 |
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2=4CuSO4+2 H2O,该反应的还原剂是 ,当1mol O2发生反应时,还原剂所失电子的物质的量为 mol。
(3)下图为电解精炼银的示意图, (填a或b)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成的该气体为 ,电极反应为 。