(10分)如图所示:已知甲池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称。甲池是 装置,乙池是 装置。
(2)B(石墨)电极的名称是 。在图中标明电子移动的方向。
(3)通入O2的电极的电极反应式是 。
(4)乙池中反应的化学方程式为 。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下)
(5)现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;③把A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向为A→导线→C。根绝上述情况,回答下列问题:
(1)在①中,金属片 发生氧化反应
(2)在②中,金属片 作负极
(3)如果把B、D用导线连接后同时浸入稀硫酸溶液,则金属片 上有气泡产生
(4)上述四种金属的活动顺序是
某小组同学在实验室中组装如下图所示装置,a为铁片,b为石墨,请回答:
(1)从能量转化的角度看,该装置是将 (填能量转化的形式),符合该装置的化学反应类型一定是 反应。
(2)若容器内盛有H2SO4溶液,则b极的电极反应式是 ,b极附近观察到的现象是 ;导线中电子流动的方向是 (用“a→b”或“b→a”表示)。
(3)若容器内盛有NaCl溶液,则a为 极(填电极名称);b极的电极反应式是 。溶液中的阳离子向 (填“a”或“b”)极方向移动。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 。(填字母)
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2CO(g)+O2(g)=2CO2(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极的电极反应式为 。
(3)利用右图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应该置于 处,此时溶液中的阴离子向 极(填X或铁)移动。
(10分) A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸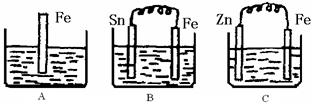
(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A ;B ; C 。
(2)一段时间后,B中Sn(锡)极附近溶液的pH (填“增大”、“减小”、“不变”)。
(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度为 mol·L-1。
(8分)已知在250C、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
(1)若2 mol氢气完全燃烧生成水蒸气,则放出的热量 ___ (填“>”、“<”或“=”)570 kJ
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:A、B两个电极均由多孔的碳块组成。该电池的正极为:__________(填A或B)。若该电池工作时增加了1mol H2O,电路中转移电子的物质的量为 ____________ mol 。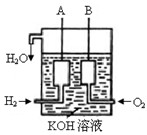
(3)写出电极反应式A: ; B: ;
为节省药品和时间.甲、乙、丙三位同学用铜片、锌片、稀硫酸、直流电源、导线、烧杯、试管等中学化学常见的药品和仪器(用品),以巧妙的构思,“接力”的方式,设计了比较铜与锌金属活动性相对强弱的系列实验。试填写下列空白:
(1)甲同学将铜片和锌片插入盛有稀硫酸的烧杯中(铜与锌不接触),观察到的现象是 。
(2)乙同学接着甲同学的实验,用导线将铜片和锌片连接起来组成原电池,此时在正极上观察到的现象是 ,负极的电极反应式为 。
(3)丙同学接着乙同学的实验,去掉连接铜片和锌片的导线,将铜片和锌片分别与同一直流电源的正极和负极连接,再向烧杯中加入一定量的CuSO4溶液进行电解。此时阴极的电极反应式为 ,电解过程中溶液的pH (填“增大”、“减小”或“不变”)。
(4)甲、乙、丙3位同学能达到比较铜和锌的金属活动性相对强弱的目的的是 。
| A.只有甲同学 | B.甲和乙同学 |
| C.乙和丙同学 | D.甲、乙和丙同学 |
如下图所示,烧杯中都盛有稀硫酸。
(1)中反应的离子方程式为 。
(2)中的电极反应:Fe: ,Sn: 。
(3)中被腐蚀的金属是 ,其电极反应式为 。
比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是 。
依据氧化还原反应:2Ag+(aq) + Cu(s) = Cu2+(aq) + 2Ag(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
Ⅰ.依据氧化还原反应:2Ag+(aq)+Cu(s) ===Cu2+(aq) +2Ag(s)设计原电池,请回答下列问题:
(1)负极材料是____________;电解质溶液是____________;
(2)正极发生的电极反应为________________________;
(3)电解质溶液中Ag+向_________极移动。
Ⅱ.一定温度下在某定容容器中发生反应:2A(g) +3B(g) ===2C(g),开始时,A的浓度为2 mol·L -1,B的浓度是4 mol·L-1,2 min后,A的浓度减少0.8 mol·L-1,则
(1)v(B) =___________,v(C) =____________。
(2)在2min末,C的浓度是____________,B的浓度是____________。
在以铁、铜为两电极的原电池中,如图所示:
(1)若电解质溶液为稀硫酸,则铜电极上的电极反应式为: ;原电池总反应的离子方程式: ;
(2)若电解质溶液为浓硝酸, 则铁电极上的电极反应式为: ;当电路中通过了1mol的电子时,则在某极上生成了标准状况下的气体体积为: L。
天然气是一种洁净环保的优质能源,天然气主要成分是烷烃,其中甲烷占绝大多数。
(1)甲烷分子具有____________结构,其结构式是___________。
(2)天然气是一种高效、低耗、污染小的清洁能源,已知1mol甲烷完全燃烧生成CO2气体和水蒸气放出802KJ热量,则在相同条件下,1mol甲烷完全燃烧生成CO2气体和液态水,放出的热量________802KJ(填“>”、“=”或“<”)。
(3)通常情况下,甲烷比较稳定,但在特定条件下,甲烷也会发生某些反应,请写出甲烷在光照条件下与氯气反应生成一氯甲烷的化学方程式__________________该反应属于______________(填反应类型)。
(4)在一定条件下甲烷也可用于燃料电池。下图是甲烷燃料电池的原理示意图:
若正极的反应式为O2+4e-+4H+=2H2O,则负极反应式为___________________;该电池工作过程中,H+的移动方向为从_____到_____(填“左”或“右”)。
如图所示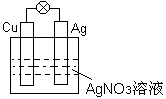
(1)负极材料是 ,
(2)正极的电极反应式为 ,
(3)电池工作时总反应的离子方程式是
(4)电子的流向
(5)阳离子的移动方向___________________________
有如下两个反应
A:2HCl+Ba(OH)2=BaCl2+2H2O B:2Fe3++Cu=2Fe2++Cu2+
(1)根据两反应的本质,判断能否设计成原电池:A ,B ,(填“能”或“不能”)不能设计成原电池的原因是 ;
(2)根据能设计成原电池的反应选择适合的材料和试剂设计一个原电池
①负极材料是 ,正极材料是 ,电解质溶液是 ;
②写出负极的电极反应式 ;
③若导线上转移电子0.2 mol,则负极质量减少 。
某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若电解质溶液为0.5mol/L硫酸,电极为铜片和铝片,则电流计指针偏向 (填“铝”或“铜”)。铝片上的电极的反应式为 ;
(2)若用浓硝酸作电解质溶液,电极为铜片和铝片,则电流计指针偏向 (填“铝”或“铜”),铝片为 极(填“正”或“负”)。铜极上电极反应式为: ,正极上发生的电极反应式为 ;
(3)若电解质溶液为0.5mol/L氢氧化钠溶液,电极为镁片和铝片,则正极发生的电极反应为 。
通过上述实验探究,你受到的启示是 。