如下图所示,烧杯中都盛有稀硫酸。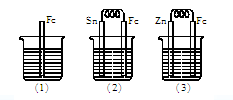
(1)中反应的离子方程式为 。
(2)中的电极反应:Fe: ,Sn: 。
(3)中被腐蚀的金属是 ,其电极反应式为 。
比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是 。
如下图所示,烧杯中都盛有稀硫酸。
(1)中反应的离子方程式为 。
(2)中的电极反应:Fe: ,Sn: 。
(3)中被腐蚀的金属是 ,其电极反应式为 。
比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是 。