如图所示,电流表G发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的哪一组( )

A.A是Zn、B是Cu、C为稀H2SO4溶液
B.A是Cu、B是Zn、C为稀H2SO4溶液
C.A是Fe、B是Ag、C为AgNO3溶液
D.A是Ag、B是Fe、C为AgNO3溶液
将纯锌片和纯铜片按图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中的铜片是正极,乙中的铜片是负极 |
| C.两烧杯中溶液的PH值均增大 |
| D.产生气泡的速度甲比乙慢 |
下列反应中,在原理上可以设计成原电池的是( )
| A.Ba(OH)2·8H2O 与NH4Cl的反应 | B.铝与盐酸的反应 |
| C.石灰石的分解 | D.甲烷与氧气的反应 |
关于下图所示的装置叙述正确的是( )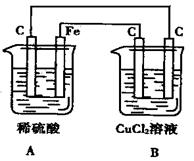
| A.装置A 是电解池,装置B是原电池 |
| B.装置A 是原电池,装置B是电解池 |
| C.电子由装置A中碳棒流向B 装置中碳棒 |
| D.工作一段时间后,A 装置中稀H2SO4溶液质量减轻,B装置中CuCl2溶液质量减轻 |
(08青岛统一检测,13)工业上利用氢气在氯气中燃烧,所得产物再溶于水的方法制得盐酸,流程复杂且造成能量浪费。有人设想利用原电池原理直接制备盐酸的同时,获取电能,假设这种想法可行,下列说法肯定错误的是( )
| A.两极材料都用石墨,用稀盐酸做电解质溶液 |
| B.通入氢气的电极为原电池的负极 |
| C.电解质溶液中的阴离子向通氯气的电极移动 |
| D.通氯气的电极反应为Cl2+2e—=2Cl— |
右图中,两电极上发生的电极反应如下:a极: ↑,
↑, 
b极: -2
-2 =
= 。则以下说法不正确的是( )
。则以下说法不正确的是( )
| A.该装置可能是电解池 |
| B.该装置中电解质溶液pH可能等于7 |
| C.a、b可能是同种电极材料 |
| D.该过程中能量的转换一定是化学能转化为电能 |
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应
“AsO43-+2I-+2H+ AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
下列叙述中正确的是( )
| A.甲组操作时,微安表(G)指针发生偏转 |
| B.甲组操作时,溶液颜色变深 |
| C.乙组操作时,C2做正极 |
| D.乙组操作时,C1上发生的电极反应为I2+2e-=2I- |
“神舟六号”宇宙飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池。该电池可同时供应电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾。已知该电池的总反应为2H2+O2 ="==" 2H2O,负极反应为H2+CO2—3→CO2↑+H2O+2e—,则下列推断中,正确的是( )
| A.电池工作时,CO2—3向负极移动 |
| B.电池放电时,外电路电子由通氧气的正极流向通氢气的负极 |
| C.正极的电极反应为:4OH—→O2↑+2H2O+2e— |
| D.通氧气的电极为阳极,发生氧化反应 |
(2008广东四校水平测试,13)如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是

| A.产生气体的体积:①>② |
| B.溶液的pH变化:①减小,②增大 |
| C.电极上析出物质的质量:①>② |
| D.电极反应式:①中阳极 2Cl--2e-Cl2 ↑ ②中负极 2H++2e-H2↑ |
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙慢 |
钢铁发生腐蚀时,正极上发生的反应是
| A.2Fe-4e- = 2Fe2+ | B.2Fe2++4e- = 2Fe |
| C.2H2O+O2+4e-= 4OH- | D.Fe3++e-= Fe2+ |
市场上出售的“热敷带”的主要成分是铁屑、碳粉、木屑、少量的氯化钠、水等。“热敷带”启用之前用塑料袋密封,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完后,会产生大量铁锈。
(1)“热敷带”放热的原理是:______________________________________________
(2)碳粉的作用是: 氯化钠的作用是:_____________________________
(3)有关电极反应是:________________________________________________________
随后反应为:_____________________________________________________________
硫一钠原电池具有输出功率较高、循环寿命长等优点。其工作原理可表示为: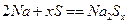 。但工作温度过高是这种高性能电池的缺陷。科学家研究发现,采用多硫化合物[如
。但工作温度过高是这种高性能电池的缺陷。科学家研究发现,采用多硫化合物[如 ]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列关于此种多硫化合物的叙述正确的是
]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列关于此种多硫化合物的叙述正确的是
| A.这是一种新型无机非金属材料 |
| B.此化合物可能发生加成反应 |
C.原电池的负极反应将是单体 转化为 转化为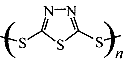 t的过程 t的过程 |
| D.当电路中转移0.02mol电子时,将消耗原电池的正极反应材料1.48g |
有人设计将两根铂丝做电极插入到KOH溶液中,然后在两极上分别通过甲烷和氧气而构成燃料电池。该电池中反应的化学方程式为:CH4+2O2+2KOH====K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是(1个电子所带电量为1.6×10-19C)
A.通过甲烷的电极为电池的负极,通过氧气的电极为正极
B.在标准状况下,每消耗5.6 L O2,可向外提供2.4×104 C的电量
C.通过甲烷电极的电极反应为:CH4+10OH--8e-==CO32-+7H2O
D.放电一段时间后,溶液的pH升高