【改编】下列说法中,不正确的是
| A.反应热指的是反应过程中放出或吸收的热量 |
| B.原电池的正极发生氧化反应 |
| C.化学变化一定伴随能量变化 |
| D.升温反应速率一定加快 |
原电池的正极__________(填“得到”或“失去”)电子,发生__________(填“氧化”或“还原”)反应;负极__________(填“得到”或“失去”)电子,发生__________(填“氧化”或“还原”)反应。
下图为番茄电池,下列说法正确的是
| A.一段时间后,锌片质量会变小 |
| B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 |
| D.锌电极是该电池的正极 |
某原电池的总反应为:Cu + 2Fe3+ = Cu2+ + 2Fe2+
| |
A |
B |
C |
D |
| 电极材料 |
Cu、Zn |
Cu、Ag |
Fe、Zn |
Cu、C |
| 插入溶液 |
FeCl3 |
Fe(NO3) 2 |
CuSO4 |
Fe2(SO4)3 |
下列说法正确的是
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.一个化学反应是吸热还是放热,取决于反应物和生成物总能量的相对大小 |
| C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D.在原电池的负极和电解池的阴极上都发生失电子的氧化反应 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是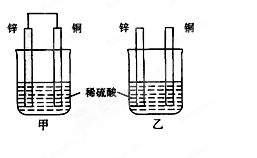
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙慢 |
下图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是

下列叙述的原因不是由于原电池造成的是
| A.运输液氯的铁管被腐蚀 | B.金属在潮湿空气中更容易腐蚀 |
| C.铁与酸反应滴加硫酸铜后反应加快 | D.含杂质的锌比纯锌与酸反应快 |
下列述叙正确的是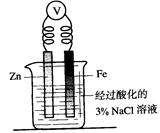
| A.要除去氯化镁酸性溶液里少量的氯化铁,可以选用氢氧化钠 |
| B.镀锡铁表面有划痕是,仍然能阻止铁被氧化 |
| C.向上图烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,一段时间后可看到Fe电极附近有蓝色沉淀生成 |
| D.各种原生铜的硫化物经氧化、淋滤作用变成硫酸铜,遇到深层的ZnS和PbS,便慢慢地使之转变为CuS |
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是
| A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动 |
| B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O |
| C.由Fe、Cu、NaCl溶液组成原电池,其负极反应式为:Cu - 2e-= Cu2+ |
| D.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗Cu电极32g |
利用下图装置可以模拟铁的电化学防护。下列说法不正确的是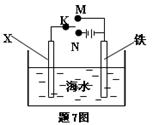
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M处,铁极发生氧化反应 |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀 |
| D.若X为碳棒,开关K置于N处,X极发生氧化反应 |
在常温常压下,某实验小组按下图做完实验后,实验报告记录如下。其中描述合理的是
| A.①②③ | B.②③④ | C.②⑤⑥ | D.③④⑥ |
如图所示,由锌片、铜片和稀硫酸溶液构成的原电池中,下列叙述正确的是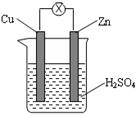
| A.锌片为负极,发生还原反应 |
| B.电流从锌片流向铜片 |
| C.一段时间后,铜片质量减轻 |
| D.一段时间后,溶液pH值变大 |