北京市朝阳区高三上学期期末考试化学试卷
下列有关物质的叙述不正确的是
| A.淀粉水解可以制得葡萄糖 |
| B.碘酒可使细菌、病毒的蛋白质变性而死亡 |
| C.氨基酸是两性化合物,能与酸或碱反应生成盐 |
| D.光导纤维遇盐酸和氢氧化钠溶液都不会被损坏 |
下列生产、生活中的事实不能用金属活动性顺序表解释的是
| A.铝制器皿不宜盛放酸性食物 |
| B.电解食盐水时阴极产生氢气 |
| C.可用铁制容器盛放和运输浓硫酸 |
| D.镀锌铁桶镀层破损后铁仍不易被腐蚀 |
下列有关化学用语正确的是
| A.聚丙烯的链节:—CH2—CH2—CH2— |
B.NH4Cl的电子式: |
C.F-结构示意图: |
D.中子数为20的氯原子: Cl Cl |
下图显示的是生锈的铁桥,有关钢铁生锈说法不正确的是
| A.铁桥生锈是电化学腐蚀 |
| B.建在海边的铁桥更易生锈 |
| C.钢铁生锈的负极反应是:Fe-3e-=Fe3+ |
| D.吸氧腐蚀的正极反应是:O2+4e-+2H2O=4OH- |
下列实验对应的离子方程式正确的是
| A.铝溶解在NaOH溶液中:2Al+2OH-=2AlO2-+3H2↑ |
| B.醋酸溶液滴入NaHCO3溶液中: H+ +HCO3-= CO2↑+H2O |
| C.SO2通入溴水中:SO2+Br2+H2O = SO42-+2Br- + 2H+ |
| D.少量铁溶于过量稀硝酸中:Fe+4H++ NO3- =Fe3++NO↑+2H2O |
下列推测或结论不合理的是
| A.X2-和Y+核外电子层结构相同,原子序数:X<Y |
| B.气态氢化物的稳定性HCl>HBr,还原性:Cl->Br- |
| C.硅、锗都位于金属与非金属的交界处,用途:都可以做半导体材料 |
| D.铷(37Rb)和锶(38Sr)分别位于第五周期IA和IIA族,碱性:RbOH >Sr(OH)2 |
下列实验操作不能达到实验目的的是
| |
实验操作 |
实验目的 |
| A |
将SO2通入品红溶液中 |
证明SO2具有漂白性 |
| B |
用pH试纸测定NaHSO3溶液的pH |
比较HSO3- 电离程度和水解程度的大小 |
| C |
溴乙烷与NaOH乙醇溶液共热,将得到的气体通入KMnO4酸性溶液 |
证明反应得到的气体是乙烯 |
| D |
向含酚酞的Na2CO3溶液中加入BaC12溶液 |
证明Na2CO3溶液中存在水解平衡 |
下列装置不能完成相应实验的是
| A.甲装置可用于制备氨气 |
| B.乙装置可除去CO2中少量的SO2杂质 |
| C.丙装置可用于粗盐提纯 |
| D.丁装置可分离CCl4萃取碘水后的分层液体 |
下列除杂方案不正确的是
| |
被提纯的物质[括号内物质是杂质] |
除杂试剂 |
除杂方法 |
| A |
CO(g) [CO2(g)] |
NaOH溶液、 浓H2SO4 |
洗气 |
| B |
NH4Cl(aq) [Fe3+(aq)] |
NaOH溶液 |
过滤 |
| C |
Cl2(g) [HCl(g)] |
饱和食盐水、浓H2SO4 |
洗气 |
| D |
Na2CO3(s) [NaHCO3(s)] |
— |
加热 |
下列叙述和推论都正确的是
| |
叙述 |
推论 |
| A |
酸性:HCl >H2CO3>H2SiO3 |
非金属性:Cl >C>Si |
| B |
组成原电池时,通常是还原性较强的物质做负极 |
镁和铝在氢氧化钠溶液中组成原电池时,镁做负极 |
| C |
—OH是亲水基,含有—OH的有机物都易溶于水 |
常温时,C2H5OH和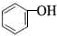 都易溶于水 都易溶于水 |
| D |
溶解度小的沉淀可转化成溶解 度更小的沉淀 |
向AgCl悬浊液中滴加KI溶液可以得到AgI沉淀 |
碘盐中添加的碘酸钾在工业上可用电解KI溶液制取,电极材料是石墨和不锈钢,化学方程式是:KI+3H2O KIO3+3H2↑,有关说法不正确的是
KIO3+3H2↑,有关说法不正确的是
| A.石墨作阳极,不锈钢作阴极 |
| B.I-在阳极放电,H+在阴极放电 |
| C.电解过程中电解质溶液的pH变小 |
| D.电解转移3 mol e-时,理论上可制得KIO3 107 g |
常温下,浓度均为0.1 mol/L的4种钠盐溶液pH如下:
| 溶质 |
Na2CO3 |
NaHCO3 |
NaClO |
NaHSO3 |
| pH |
11.6 |
9.7 |
10.3 |
5.2 |
下列说法不正确的是
A.四种溶液中,Na2CO3溶液中水的电离程度最大
B.NaHSO3溶液显酸性的原因是: NaHSO3 =Na+ + H+ + SO32-
C.向氯水中加入少量NaHCO3(s),可以增大氯水中次氯酸的浓度
D.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3
H2和I2在一定条件下能发生反应:H2(g) +I2(g) 2HI(g) △H= —a kJ/mol
2HI(g) △H= —a kJ/mol
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法正确的是
| A.H2、I2和HI分子中的化学键都是非极性共价键 |
| B.断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ |
| C.相同条件下,1 mol H2 (g)和1mol I2 (g)总能量小于2 mol HI (g)的总能量 |
| D.向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ |
制作软质隐形眼镜高分子材料(M)和聚酯PET的合成路线如下:
已知酯与醇可发生如下酯交换反应:
(R、R′、R″代表有机基团)
(1)A的相对分子质量是28,A、B分子中含有的官能团分别是 。
(2)B的名称是 。
(3)反应I的反应类型是_______(选填字母)。
a.加聚反应 b.缩聚反应
(4)有关B、C、D的说法正确的是 。
a.1mol B最多可以和1 mol C反应
b.C、D都能使Br2的CCl4溶液褪色
c.D与NaOH溶液共热后可以得到B和C
(5)B→D的化学方程式是 。
(6)C有多种同分异构体,其中一种是合成纤维维尼纶的单体,该分子在酸性环境下水解得到两种产物,它们的相对分子质量相差16,该同分异构体的结构简式是 。
(7)反应II的化学方程式是 。
甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物。工业上可用CO和H2制取甲醇,化学方程式为:CO(g)+2H2(g) CH3OH(g) △H="a" kJ/mol
CH3OH(g) △H="a" kJ/mol
为研究平衡时CO的转化率与反应物投料比( )及温度的关系,研究小组在10 L的密闭容器中进行模拟反应,并绘出下图:
)及温度的关系,研究小组在10 L的密闭容器中进行模拟反应,并绘出下图:
(1)反应热a 0 (填“>”或“<”),判断依据是 。
(2)若其它条件相同,Ⅰ、Ⅱ曲线分别表示投料比不同时的反应过程。
①投料比:Ⅰ Ⅱ (填“>”或“<”)。
②若Ⅱ反应的n(CO)起始 ="10" mol、投料比为0.5,
A点的平衡常数KA= ,
B点的平衡常数KB KA (填“>”或“<”或“=”)。
(3)为提高CO转化率可采取的措施是 (至少答出两条)。
电解铝厂的实验室为测定铝土矿(主要成分是Al2O3,杂质是Fe2O3 、SiO2)样品中Al2O3的质量分数,操作如下:
Ⅰ.将铝土矿样品粉碎后加入足量稀H2SO4溶液,充分反应后过滤,得滤液a
Ⅱ.向滤液a中加入足量NaOH溶液,充分反应后过滤,得滤液b
Ⅲ.向滤液b中通入足量CO2,充分反应后过滤、洗涤,得Al(OH)3沉淀
Ⅳ.……
(1)滤液a中阳离子有 (写离子符号)。
(2)操作Ⅱ中反应的离子方程式是 。
(3)操作Ⅳ是 。
(4)要测定铝土矿样品中Al2O3的质量分数,所需数据是 (质量数据用x、y…表示,单位是g);铝土矿样品中Al2O3质量分数表达式是 (用含x、y…的式子表示)。
高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是 价,Na2FeO4具有较强的 (填“氧化性”或“还原性”)。
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是 (用离子方程式表示)。
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 + 10NaOH + 3NaClO = 2 + 5 + 9 。
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4 。
① 若电解所需的浓NaOH溶液为16 mol/L,则在实验室配制500 mL该浓度的溶液需NaOH g,配制过程所需玻璃仪器是 。
② 电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:
阳极的电极反应式是 ;可循环使用的物质是 ,理由是 。
SO2是常见的大气污染物,燃煤是产生SO2的主要原因。工业上有多种方法可以减少SO2的排放。
(1)往煤中添加一些石灰石,可使燃煤过程中产生的SO2转化成硫酸钙。该反应的化学方程式是 。
(2)可用多种溶液做燃煤烟气中SO2的吸收液。
①分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHSO3时,两种吸收液体积比V(Na2SO3): V(NaOH)= 。
②NaOH溶液吸收了足量的SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式是 。
(3)甲同学认为BaCl2溶液可以做SO2的吸收液。为此甲同学设计如下实验(夹持装置和加热装置略,气密性已检验):
已知:Na2SO3(固体) + H2SO4(浓) Na2SO4 + SO2↑+ H2O
Na2SO4 + SO2↑+ H2O
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B中有白色沉淀。甲同学认为B中白色沉淀是SO2与BaCl2溶液反应生成的BaSO3,所以BaCl2溶液可做SO2吸收液。
乙同学认为B中的白色沉淀是BaSO4,产生BaSO4的原因是:
①A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀。
② 。
为证明SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略,气密性已检验):
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其它现象;D中红色褪去。
③试管B中试剂是 溶液;滴加浓硫酸之前的操作是 。
④通过甲乙两位同学的实验,得出的结论是 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号