某温度下,FeB(s) Fe2+(aq)+B2-(aq)的平衡常数表达式为Ksp= c(Fe2+)·c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )
Fe2+(aq)+B2-(aq)的平衡常数表达式为Ksp= c(Fe2+)·c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )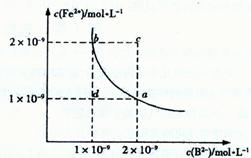
| A.a点对应的Ksp等于b点对应的Ksp |
| B.d点无沉淀生成 |
| C.可以通过升温实现由c点变到a点 |
| D.此温度下,FeB的Ksp=2×l0-18mol2·L-2[ |
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图。下列说法正确的是( )
| A.常温下,向100mL CaSO4饱和溶液中,加入400mL 0.01mol/L Na2SO4溶液后,溶液中无沉淀析出 |
| B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3 mol/L |
| C.d点溶液通过蒸发可以变到c点 |
D.a 点对应的Ksp等于c点对应的Ksp 点对应的Ksp等于c点对应的Ksp |
下列有关沉淀溶解平衡的说法中,正确的是( )
A. Ksp(AB2)小于Ksp(CD),说明AB2的溶解度小于CD的溶解度
B.在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp增大
C.在碳酸钙的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动
D.向氯化银沉淀溶解平衡体系中加人碘化钾固体,氯化银沉淀可转化为碘化银沉淀
(1)粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质。在提纯时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是___________。
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
(2)己知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,㏒2=0.3。通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全。试计算
①将溶液的pH调至PH=__________时Fe3+转化为Fe(OH)3而沉淀完全。
②若CuSO4溶液的浓度为2.2mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为__________。
(3)调整溶液的pH可选用下列中的____________。
A.NaOH(aq) B.NH3·H2O C.CuO粉末 D.Cu(OH)2悬浊液 E.Cu2(OH)2CO3(s)
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀中滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是
| A.白色沉淀为ZnS,黑色沉淀为CuS |
| B.上述现象说明ZnS的Ksp小于CuS的Ksp |
| C.利用该原理可实现一种沉淀转化为更难溶的沉淀 |
| D.该过程破坏了ZnS的溶解平衡 |
下列说法正确的是( )
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;
③对于Al(OH)3(s) Al(OH)3(aq)
Al(OH)3(aq) Al3++3OH-,前者为溶解平衡,后者为电离平衡;
Al3++3OH-,前者为溶解平衡,后者为电离平衡;
④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小
⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全。
| A.①②③④⑤ | B.② | C.①③④⑤ | D.①②⑤ |
在溶液中有浓度均为0.01mol·L—1的Fe3+、Cr3+、Mg2+等离子,已知:
Ksp[Fe(OH)3]=2.6×10—39mol4·L—4;Ksp[Cr(OH)3]=7.0×10—31mol4·L—4
Ksp[Zn(OH)2]=1.0×10—17mol3·L—3;Ksp[Mg(OH)2]=1.8×10—11mol3·L—3
当氢氧化物开始沉淀时,下列哪一种离子所需溶液的pH最小
| A.F3+ | B.Cr3+ | C.Zn2+ | D.Mg2+ |
已知,Fe2+结合S2—的能力大于结合OH—的能力,而Al3+则正好相反,I2的氧化性比S强。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是( )
| A.FeS、Al(OH)3和S | B.Fe(OH)3和Al(OH)3 |
| C.Fe2S3和 Al(OH)3 | D.Al2S3、FeS和S |
有关AgCl沉淀的溶解平衡说法正确的是( )
| A.AgCl沉淀生成和沉淀溶解不断进行并且速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升高温度,AgCl沉淀的溶解度减小 |
| D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解平衡不移动 |
在平衡体系Ca(OH)2(s) Ca2+(aq)+2OH-(aq)中,能使c(Ca2+)减小,而使c(OH-)增大的是( )
Ca2+(aq)+2OH-(aq)中,能使c(Ca2+)减小,而使c(OH-)增大的是( )
| A.加入少量MgCl2固体 | B.加入少量Na2CO3固体 |
| C.加入少量KCl固体 | D.加入少量Ba(OH)2固体 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线 如右图所示。下列说法正确的是
如右图所示。下列说法正确的是 (提示:BaSO4(s)
(提示:BaSO4(s) Ba2+(aq)+SO42-(aq)的平衡
Ba2+(aq)+SO42-(aq)的平衡 常数Ksp=c(Ba2+)·c(SO42-),称为溶积常数)
常数Ksp=c(Ba2+)·c(SO42-),称为溶积常数)
A. 加入Na2SO4可以使溶液由a点变到c点 加入Na2SO4可以使溶液由a点变到c点 |
B. 通过蒸发可以使溶液由d 通过蒸发可以使溶液由d 点变到c点 点变到c点 |
C. d点有BaSO4沉淀生成 d点有BaSO4沉淀生成 |
D. a点对应的Ksp大于c点对应的Ksp a点对应的Ksp大于c点对应的Ksp |
已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11。下列说法正确的是( )
A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+) 大 大 |
| B.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
| C.25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1NH4Cl溶液中的Ksp小 |
| D.25℃时,在Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 |
下列说法正确的是
| A.汽油燃烧时将全部的化学能转化为热能 |
| B.饱和石灰水中加入一定量生石灰,所得溶液的pH增大 |
| C.向AgCl悬浊液中加入KI溶液,白色沉淀转化为黄色沉淀,说明溶解度AgCl<AgI |
| D.向AgCl悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀中滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是
| A.白色沉淀为ZnS,黑色沉淀为CuS | B.上述现象说明ZnS的Ksp小于CuS的Ksp |
| C.利用该原理可实现一种沉淀转化为更难溶的沉淀 | D.该过程破坏了ZnS的溶解平衡 |