下列叙述正确的是  ( )
( )
| A.0.1 mol/LCH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 |
| D.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 |
向饱和的BaSO4溶液中加水,下列叙述正确的是( )
| A.BaSO4溶解度增大,Ksp不变 |
| B.BaSO4溶解度、Ksp均增大 |
| C.BaSO4溶解度不变,Ksp增大 |
| D.BaSO4溶解度、Ksp均不变 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的BaSO4的Ksp大于c点对应的Ksp |
已知:Ksp(AgCl)=1×10-10,Ksp(AgI)=1×10-16,Ksp(Ag2CrO4)=8.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
| A.AgCl>AgI>Ag2CrO4 | B.AgCl> Ag2CrO4>AgI |
| C.Ag2CrO4> AgCl> >AgI | D.Ag2CrO4> AgI> AgCl |
下列化学原理的应用,主要用沉淀溶解平衡原理来解释的是( )
①热纯碱溶液洗涤油污的能力强 ②误将钡盐〔BaCl2、Ba(NO3)2〕当作食盐混用后,常用0.5%的Na2SO4溶液解毒 ③溶洞、珊瑚的形成④碳酸钡不能做“钡餐”而硫酸钡则能 ⑤泡沫灭火器灭火的原理
| A.②③④ | B.①②③ | C.③④⑤ | D.①②③④⑤ |
(1)用水稀释0.1mol/L氨水,溶液中随着水量的增加而减小的是_______(填字母)
(2)已知25℃时,Ksp(CaSO4)==7.10×10-5.向0.100L含CaSO4固体的溶液中加入2.22gCaCl2粉末充分搅拌,若溶液的体积变化忽略不计,则溶液中CaSO4固体的质量将______ (填“增大”、“减小”或“不变”,下同), Ksp(CaSO 4)将________。
4)将________。
相同温度下,将足量的AgCl分别放入下列溶液中:
①20mL0.1mol/L(NH4)2CO3溶液 ②40mL0.02 mol/LBaCl2溶液
③40mL0.03 mol/L盐酸 ④10 mL蒸馏水
⑤50 mL0.05mol/LAgNO3溶液。则AgCl的溶解度大小顺序为:
| A.①=②=③=④=⑤ | B.①>④>③>②>⑤ |
| C.⑤>④>①>③>② | D.④>③>⑤>①>② |
有关难溶盐的溶度积及溶解度,以下叙述中正确的是
| A.将难溶电解质放入纯水中,溶解达到平衡时,电解质离子浓度的乘积就是该物质的Ksp |
| B.两种难溶电解质,其中Ksp小的溶解度也一定小 |
| C.加入与原电解质具有相同离子的物质,可使难溶盐电解质的溶解度变小,也使Ksp变小 |
| D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变 |
已知:Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=7.8×10-13。现将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,发生的反应为
| A.只有AgBr沉淀 |
| B.AgCl和AgBr沉淀等量生成 |
| C.AgCl和AgBr沉淀都有,AgCl沉淀比AgBr多 |
| D.AgCl和AgBr沉淀都有,AgBr沉淀比AgBr多 |
下列说法中正确的是
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 |
B.AgCl悬浊液中存在平衡:AgCl(s)  Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 |
| C.为减小洗涤过程中固体的损失,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀 |
| D.硬水中含有较多的Ca2+、Mg2+、HCO3-、SO42-,加热煮沸可以完全除去其中的 Ca2+、Mg2+ |
在重铬酸钾(K2Cr2O7)溶液中存在如下平衡:

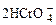

 , 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
, 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
| A.Ag2O | B.Ag2CrO4 | C.AgHCrO4 | D.Ag2Cr2O7 |
(4分)向100mL 0.018mol/L的AgNO3溶液中加入100mL 0.02mol/L的盐酸,生成沉淀。已知AgCl(s) 的溶度积常数Ksp=c(Ag+)×c(Cl-)=1×10-10。(混合后溶液的体积变化忽略不计)。试计算:
的溶度积常数Ksp=c(Ag+)×c(Cl-)=1×10-10。(混合后溶液的体积变化忽略不计)。试计算:
(1)沉淀生成后溶液中Cl-的浓度。
(2)沉淀生成后溶液中Ag+的浓度。
把Ca(OH)2放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s)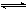 Ca2++2OH-
Ca2++2OH-
当向悬浊液中加入少量生石灰后,若温度保持不变,下列说法正确的是( )
| A.溶液中Ca2+数目增多 | B.溶液中Ca2+数目不变 |
| C.c(Ca2+)增大 | D.c(Ca2+)不变 |
下列说法正确的是
| A.AgCl的水溶液中,Ag+和Cl-浓度的乘积是一个常数; |
| B.AgCl的Ksp=1.8×10-10,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10; |
| C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液; |
| D.向饱和AgCl水溶液中加入盐酸,Ksp值变大。 |
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。
下列说法正确的是
| A.CaSO4在稀硫酸中的溶解性比在纯水中的溶解性强 |
| B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3 mol/L |
C.d点溶液通过蒸发 可以变到c点 可以变到c点 |
| D.a点对应的Ksp等于c点对应的Ksp |