在N2+3H2 2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol·L-1,在此时间内用H2表示的反应速率为0.45mol·L-1·s-1,则该反应所经历的时间是( )
2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol·L-1,在此时间内用H2表示的反应速率为0.45mol·L-1·s-1,则该反应所经历的时间是( )
| A.0.44s | B.1s | C.1.33s | D.2s |
在不同条件下分别测得反应2SO2+O2 2SO3的化学反应速率,其中表示该反应进行最快的是( )
2SO3的化学反应速率,其中表示该反应进行最快的是( )
| A.v(SO2)=4 mol·L-1·min-1 | B.v (O2)=3 mol·L-1·min-1 |
| C.v (SO3)="0.1" mol·L-1·s-1 | D.v (O2)=0.1mol·L-1·s-1 |
反应速率v和反应物浓度的关系是用实验方法测定的,化学反应H2+Cl2=2HCl的反应速率v可表示为v=K[c(H2)]m[c(Cl2)]n,式中K为常数,m、n值可用下表中数据确定之。
| c(H2)(mol·L-1) |
c(Cl2)(mol·L-1) |
v(mol·L-1·s-1) |
| 1.0 |
1.0 |
1.0K |
| 2.0 |
1.0 |
2.0K |
| 2.0 |
4.0 |
4.0K |
由此可推得,m、n值正确的是
A.m=1,n=1 B.m= ,n=
,n= C.m=
C.m= ,n=1 D.m=1,n=
,n=1 D.m=1,n=
在四个不同的容器中,在不同的条件下进行合成氨反应:N2 + 3H2 2NH3,根据下列在相同时间内测得的结果判断,生成氨的反应速度最快的是:
2NH3,根据下列在相同时间内测得的结果判断,生成氨的反应速度最快的是:
| A.V(NH3) =" 0.1" mol/(L﹒min) | B.V(N2) =" 0.1" mol/(L﹒min) |
| C.V(N2) =" 0.2" mol/(L﹒min) | D.V(H2) =" 0.3" mol/(L﹒min) |
)将等物质的量的A、B混合于2L密闭容器中发生如下反应:
3A(g)+B(g)=xC(g)+2D(g) 经5分钟后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L·min) 求:
(1)此时A的浓度及反应开始前容器中A、B的物质的量分别为 、 、
(2)B的平均反应速率
(3)x=
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+ Y(g) Z(g) Z(g) |
将N2、H2的混合气体分别充入甲、乙、丙三个容器中,进行合成氨反应,经过相同的一段时间后,测得反应速率分别为:甲:v(H2)=3 mol·L-1·min-1;乙:v(N2)=2 mol·L-1·min-1;丙:v(NH3)= 1 mol·L-1·min-1。则三个容器中合成氨的反应速率
| A.v(甲)>v(乙)>v(丙) | B.v(乙)>v(丙)>v(甲) |
| C.v(丙)>v(甲)>v(乙) | D.v(乙)>v(甲)>v(丙) |
在一定条件下,向体积为2 L的容器中加入2 mol O2和3 mol SO2使之反应生成SO3气体:2SO2+ O2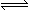 2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
(1)2min内,平均反应速率v(SO3)=
(2)2min时,SO2的浓度为
⑴20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如题图⑴所示是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是 (填“吸热”或“放热”)反应,NO2和CO的总能量 (填“>”、“<”或“=”)CO2和NO的总能量。
⑵某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质物质的量随时间的变化曲线如图⑵所示。根据图中数据,试填写下列空白:
①该反应在 min时达到平衡状态;
②该反应的化学方程式为: ;
⑶一定温度下,对于反应2A(g) + B(g) 2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图⑶所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则:
2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图⑶所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则:
①p点时反应的v正 v逆(填“>”、“<”或“=”);
②a,b两点的正反应速率va vb(填“>”、“<”或“=”)
在某一化学反应中,反应物A的浓度在20 s内从1.0 mol/L变为0.2 mol/L,则在这20 s内以A浓度的变化表示的平均反应速率为( )
| A.0.04 mol / (L·s) | B.0.04 mol / L | C.0.08 mol / (L·s) | D.0.08 mol / L |
(1)在CH4、H2S、NH4+、H2O、OH—、HCl、Na、Mg2+八种粒子中,选择符合下列要求的粒子填空:
①上述粒子中与K+质子数不同,电子数相同的有 ;
②上述粒子中与NH3质子数相同,电子数也相同的有 ;
③上述粒子中电子数大于质子数的有 。
(2)用锌片、铜片和稀硫酸组成的原电池,该电池的负极材料是 ,正极的电极反应式为 ,电池工作时电子流向 (填“正极”或“负极”)。
(3)将6molA气体和2molB气体在2L密闭容器中混合并在一定条件下发生反应:3A(g)+B(g) xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L•min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L•min),请填写下列空白:
①x的数值为 ;
②A的平均反应速率为 ;
③5min时B的转化率为 。
反应4A(s)+3B(g)=2C(g)+ D(g),经2 min,B的浓度减少了0.6 mol/L。对此反应速率的表示正确的是
A.用A表示的反应速率是0.3 mol·L−1·min−1
B.分别用B、C、D表示的反应速率的比值是3﹕2﹕1
C.在2 min末的反应速率,用B表示是0.3 mol·L−1·s−1
D.B和C的反应速率分别表示2 min内各自的消耗量
在2A+B 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.υ(A)=0.5 mol·L−1·s−1 B.υ(B)=0.5 mol·L−1·s−1
C.υ(C)=0.8 mol·L−1·s−1 D.υ(D)=1 mol·L−1·s−1
把0.2molX气体和0.5molY气体混合于1L密闭容器中,使它们发生如下反应:2X(g)+3Y(g)=nZ(g)+4W(g)。2min末已生成0.2molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L•min),试计算:
(1)前2min内用W的浓度变化表示的平均反应速率;
(2)2min末时Y的浓度;
(3)化学反应方程式中n的值是多少?
用实验确定某酸HB的弱电解质。两同学的方案是:
甲:①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质。
乙:①用已知物质的量浓度的HB溶液、盐酸,分别配制pH = 1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HB是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HB是弱电解质的现象是 (多选扣分)
A.HCl溶液的试管中放出H2的速率快;
B.装HB溶液的试管中放出H2的速率快;
C.两个试管中产生气体速率一样快。
(3)请你评价:乙方案中两个难以实现之处
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表达。