设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1 mol苯分子中含有C=C双键数目为3NA |
| B.标准状况下,11.2 L CCl4中含有的共价键数目为2NA |
| C.1 mol乙烯和乙醇的混合物完全燃烧时消耗O2的分子数为3NA |
| D.常温常压下,17 g羟基含有的电子总数为10NA |
某实验需要使用大约480mL 1mol/L的稀H2SO4,现若要你用18.4mol/L的浓H2SO4配制,则你需量取浓H2SO4的体积是
| A.26.1mL | B.27.2mL | C.26.0m L | D.27.0mL |
下列关于1.5 mol 氢气的叙述中,正确的是
| A.质量是 4 g | B.体积是 33.6 L |
| C.电子数是 3 | D.分子数是 1.5×6.02 ×1023个 |
某Mg、Al混合物共7.8克,加入足量盐酸,生成标准状况下的气体8.96升。再向此溶液中加入适量NaOH溶液,恰好使Mg2+、Al3+完全沉淀,求:
(1)混合物中Mg、Al的物质的量各为多少?
(2)生成沉淀的质量是多少?
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为 mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取溶液体积的多少而变化的是 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取 mL上述浓盐酸进行配制。
②配制过程中,需要使用的仪器除了烧杯,玻璃棒,还包括 。
③在配制过程中下列实验操作会使所配制的稀盐酸的物质的量浓度偏高的是 。
A.用量筒量取浓盐酸后用蒸馏水洗涤量筒,并把洗涤液转移入容量瓶中
B.配制过程动作过慢,浓盐酸中HCl挥发
C.溶液注入容量瓶前没有恢复到室温就进行定容
D.定容时俯视刻度线
E.定容时仰视刻度线
F.定容时不小心加水超过刻度线,立即用胶头滴管吸出使凹液面最低点与刻度线相切
300mlAl2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1mol/l Ba(OH)2溶液100ml,反应后溶液中SO42-的物质的量浓度为( 忽略溶液体积的变化)( )
| A.0.2mol/L | B.0.1mol/L | C.0.3mol/L | D.0.4mol/L |
两种金属混合粉末15g,与足量的盐酸反应时生成11.2L氢气(标准状况),符合上述情况的金属混合物的是( )
| A.Mg和Al | B.Mg和Ag | C.Na和Zn | D.Fe和Zn |
在标准状况下①6.72L CH4 ②3.01×1023个HCl分子③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达不正确的是( )
| A.物质的量②>③>①>④ | B.体积②>③>①>④ |
| C.质量②>③>①>④ | D.氢原子个数②>③>①>④ |
用NA表示阿伏加德罗常数值。下列叙述正确的是( )
| A.64gSO2含有氧原子数为NA |
| B.物质的量浓度为0.5mol/LMgCl2溶液,含有Cl-离子数为NA |
| C.0.5NA个O2的质量为32g |
| D.常温常压下,14gN2含有分子数为0.5NA |
与30mL 1mol/L的MgCl2溶液中Cl-浓度相同的是( )
| A.150mL 0.2mol/L FeCl2溶液 | B.90mL 2mol/L NaCl溶液 |
| C.60mL 1mol/L AlCl3溶液 | D.30mL 0.5mol/L CaCl2溶液 |
下列叙述中正确的是( )
| A.摩尔是把物质的质量和微观粒子数联系起来的一个基本物理量 |
| B.1摩尔H2SO4的质量为98g/mol |
| C.国际上规定,0.012 kg 碳原子所含有的碳原子数目为 1 mol |
| D.1摩尔氢气分子可以表示为1mol H2 |
某化学小组欲以CO2主要为原料,采用下图所示装置模拟“侯氏制碱法”制取NaHCO3,并对CO2与NaOH的反应进行探究。请你参与并完成对有关问题的解答。
【资料获悉】
1、“侯氏制碱法”原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,然后再将NaHCO3制成Na2CO3。
2、Na2CO3与盐酸反应是分步进行:Na2CO3先与盐酸反应生成NaHCO3;然后再发生NaHCO3+HCl=NaCl+H2O +CO2↑
【实验设计】
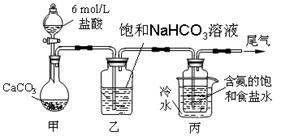
【实验探究】
(1)装置乙的作用是 。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、洗涤、灼烧。NaHCO3转化为Na2CO3的化学方程式为 。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。
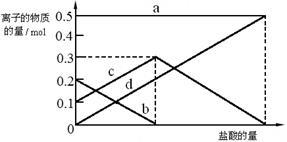
则曲线c对应的溶液中的离子是 (填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是 。
(4)若将装置甲产生的纯净的CO22.24L(标准状况下)通入100mLNaOH溶液中,充分反应后,将溶液小心蒸干,得到不含结晶水的固体W,其质量为10.16g,则W的成分为 (填化学式),原NaOH溶液的物质的量浓度为 。
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。 向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是( )。
A. |
B. |
| C.n=m+0.017Vc | D.n=p+ ×2 ×2 |
将NO2、NH3、O2混合气22.4L通过稀硫酸后,溶液质量增加了26.7g,气体体积缩小为4.48L。(气体体积均在标况下测定)剩余气体能使带火星的木条着火,则混合气体的平均相对分子质量为(4NO2+O2+2H2O=4HNO3)( )
| A.28.1 | B.30.2 | C.33.1 | D.34.0 |