已知反应I2(g)+H2(g) 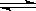 2HI(g) ΔH<0,下列说法正确的是( )
2HI(g) ΔH<0,下列说法正确的是( )
| A.降低温度,正向反应速率减小倍数大于逆向反应速率减小倍数 |
| B.升高温度将缩短达到平衡的时间 |
| C.达到平衡后,保持温度和容积不变,充入氩气,正、逆反应速率同等倍数增大 |
| D.达到平衡后,保持温度和压强不变,充入氩气,HI的质量将减小 |
可以充分说明反应P(g)+Q(g) R(g)+S(g)在恒温下已达到平衡的是( )
R(g)+S(g)在恒温下已达到平衡的是( )
| A.反应容器内的压强不随时间改变 |
| B.反应容器内P、Q、R、S四者浓度之比为1:1:1:1 |
| C.P的生成速率和S的生成速率相等 |
| D.反应容器内的气体总物质的量不随时间变化 |
在一密闭容器中充入1molNO2气体,建立如下平衡2NO2  N2O4,测得NO2转化率为a%。在温度、体积不变时,再通入1molNO2,待新平衡建立时,测得NO2的转化率为b%, a与b比较
N2O4,测得NO2转化率为a%。在温度、体积不变时,再通入1molNO2,待新平衡建立时,测得NO2的转化率为b%, a与b比较
| A.a>b | B.b>a | C.a=b | D.无法比较 |
下列对各种平衡体系的叙述中,完全正确的一组是
① 在醋酸溶液中存在的电离平衡:CH3COOH CH3COO-+ H+,加水稀释后,溶液中所有离子浓度均减小
CH3COO-+ H+,加水稀释后,溶液中所有离子浓度均减小
② 常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡逆向移动
③ 某温度下,容积一定的密闭容器中进行可逆反应:X(g)+Y(g)  2Z(g) +W(s); △H>0平衡后,升高温度,该化学平衡正向移动
2Z(g) +W(s); △H>0平衡后,升高温度,该化学平衡正向移动
④在上述③的可逆反应中,当容器中气体压强不变时,反应达到平衡
⑤一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡
CH3COO-+ H2O CH3COOH + OH-使得溶液中的c (OH-)>c(H+)
CH3COOH + OH-使得溶液中的c (OH-)>c(H+)
⑥在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动
⑦在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
| A.①②③④⑤ | B.②③④⑤⑥ | C.②③⑤⑥⑦ | D.①②⑤⑥⑦ |
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发达水平的一种标志。目前主要生产方法是“接触法”,有关2SO2+O2 2SO3的说法中,不正确的是
2SO3的说法中,不正确的是
| A.该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻之后,正、逆反应速率相等 |
| D.平衡时SO2、O2、SO3的分子数之比不再改变 |
在一定温度下,下列叙述说明可逆反应A(g)+2B(g)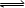
 2C(g) 达到平衡的( )
2C(g) 达到平衡的( )
A.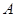 、 、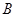 、 、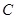 的浓度之比为1:2:2 的浓度之比为1:2:2 |
B.单位时间内消耗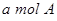 ,同时生成2a mol C ,同时生成2a mol C |
C.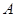 的浓度不再变化 的浓度不再变化 |
| D.混合气体总物质的量为2a mol |
高温下,某反应达平衡,平衡常数K= 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A 升高温度,逆反应速率减小
B.恒温恒容下,增大压强,H2浓度一定减小
C.反应的焓变为正值
D.该反应化学方程式为CO + H2O CO2+ H2
CO2+ H2
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说法正确的是
CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说法正确的是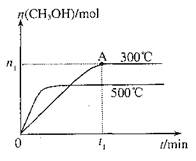
| A.该反应的△H<0 |
| B.其他条件不变,升高温度反应的平衡常数增大 |
C.300℃时,0–t1 min内CH3OH的平均生成速率为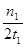 mol•L-1 min-1 mol•L-1 min-1 |
D.A点的反应体系从300℃升高到500℃,达到平衡时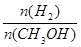 减小 减小 |
I2在KI溶液中存在下列平衡:I2(aq) + I-(aq) I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)。
I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)。
下列说法不正确的是
| A.状态a与状态b相比,状态b时I2的转化率更高 |
B.反应I2(aq)+I-(aq) I3-(aq)△H<0 I3-(aq)△H<0 |
| C.若T1时,反应进行到状态d时,一定有υ正>υ逆 |
| D.温度为T1时,向该平衡体系中加入KI固体,平衡正向移动 |
在刚性密闭容器中加入P、Q发生下列反应,P(g)+2Q(g)  2S(g)+R(s)下列说法可以说明反应已达平衡的是
2S(g)+R(s)下列说法可以说明反应已达平衡的是
| A.反应容器中压强不随时间变化而变化 |
| B.反应容器中P、Q、R、S四者共存 |
| C.P和R的生成速率相等 |
| D.反应容器中物质的总物质的量保持不变 |
在一定条件下,对于反应mA(g)+nB(g)  pC(g)+qD(g),C物质的质量分数[w(C)]与温度、压强的关系如图所示,下列判断正确的是( )
pC(g)+qD(g),C物质的质量分数[w(C)]与温度、压强的关系如图所示,下列判断正确的是( )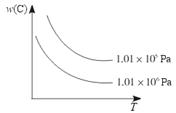
A.ΔH<0,m+n<p+q B.ΔH>0,m+n>p+q
C.ΔH>0,m+n<p+q D.ΔH<0,m+n>p+q
当反应COCl2(g) CO(g)+Cl2(g) ΔH>0达到平衡时,下列措施:
CO(g)+Cl2(g) ΔH>0达到平衡时,下列措施:
①升温 ②恒容通入惰性气体 ③增加CO的浓度
④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
某一反应物在一定条件下的平衡转化率为25.3%,当使用了催化剂时,其转化率为
| A.大于25.3% | B.小于25.3% | C.等于25.3% | D.不能确定 |
某温度下,反应SO2(g)+ O2(g)  SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)
SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)  2SO2(g) + O2(g)的平衡常数K2的值为
2SO2(g) + O2(g)的平衡常数K2的值为
| A.2500 | B.100 | C.4×10-4 | D.2×10-2 |