[山东]2012-2013学年山东省高一暑假作业(四)化学试卷
下面有关离子化合物的说法正确是
| A.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物。 |
| B.离子键只存在于离子化合物中,离子化合物中一定含有离子键 |
| C.离子化合物中不可能含有共价键 |
| D.离子化合物受热融化破坏化学键,吸收能量,属于化学变化 |
下列情况会破坏共价键的是
| A.氯化纳加热融化 | B.氢氧化钠溶于水 |
| C.氯化氢气体溶于水 | D.酒精溶于水 |
下列各数值表示有关元素的原子序数,其所表示的各原子组中能以共价键相互结合成稳定化合物的是
| A.8与11 | B.9与9 | C.2与19 | D.6与8 |
XY2是离子化合物,X和Y的离子的电子层结构与氖原子的相同,则X、Y为
| A.Na和Cl | B.K和S | C.Ca和F | D.Mg和F |
下列事实中,能够证明HCl是共价化合物的是
| A.HCl易溶于水 | B.液态的HCl不导电 |
| C.HCl不易分解 | D.HCl溶于水能电离,呈酸性 |
下列变化中,既有共价键和离子键断裂,又有共价键和离子键形成的是
| A.2Na2O2+2CO2=2Na2CO3+O2 | B.2Na+2H2O=2NaOH+H2↑ |
| C.Cl2+H2O=HCl+HclO | D.Na2CO3+BaCl2=BaCO3↓+2NaCl |
下列说法中正确的是
| A.化学反应中的能量变化,表现形式除热量外还可以是光能和电能等 |
| B.化学反应中的能量变化不一定服从能量守恒定律 |
| C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量可能相同 |
| D.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.反应物X和Y的总能量一定小于生成物M和N的总能量 |
过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是
| A.升高温度 | B.加入适量的水 |
| C.加入少量CuSO4溶液 | D.加入浓度较大的盐酸 |
下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是
| A.10℃ 20mL 3mol/L的盐酸溶液 | B.20℃ 30mL 2mol/L的盐酸溶液 |
| C.20℃ 20mL 2mol/L的盐酸溶液 | D.20℃ 10mL 4mol/L的盐酸溶液 |
可逆反应2NO2 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2,NO,O2表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②③⑤⑦ | C.①③④⑤ | D.全部 |
下列说法正确的是
| A.一定条件下,增加反应物的量,必定加快反应速率 |
| B.升高温度正反应速率增大,则逆反应速率也一定增大 |
| C.可逆反应的特征是正反应速率总是和逆反应速率相等 |
| D.使用催化剂一定会加快反应速率 |
下列反应体系中,不属于可逆反应的是
| A.Cl2溶解于水 |
| B.氨气溶解于水 |
| C.工业合成氨 |
| D.水电解生成H2和O2与H2在O2中燃烧生成H2O |
下图是可逆反应X2+3Y2 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是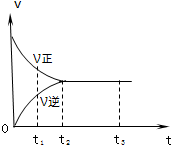
| A.t1时,只有正方向反应 | B.t1~t2时,X2的物质的量越来越多 |
| C.t2~t3,反应不再发生 | D.t2~t3,各物质的浓度不再发生变化 |
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发达水平的一种标志。目前主要生产方法是“接触法”,有关2SO2+O2 2SO3的说法中,不正确的是
2SO3的说法中,不正确的是
| A.该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻之后,正、逆反应速率相等 |
| D.平衡时SO2、O2、SO3的分子数之比不再改变 |
下列叙述中可以说明反应2HI(g)  H2(g)+I2(g)已达平衡状态的是
H2(g)+I2(g)已达平衡状态的是
①单位时间内生成n mol H2的同时生成n mol HI ②一个H—H键断裂的同时有两个H—I键断裂 ③百分组成HI%=I2% ④反应速率v(H2)=v(I2)=1/2v(HI) ⑤[HI]∶[H2]∶[I2]=2∶1∶1 ⑥v(HI)分解=v(HI)生成 ⑦压强不变
| A.①③⑤ | B.②⑥ | C.④⑤ | D.④⑥⑦ |
分类法是化学学习的一种十分有效的方法,它可以使我们从不同角度对同一知识做更加深入的了解,人们根据不同的标准,即使同一物质也可能被划在不同的类别中。现有如下物质①MgCl2②HCl ③SO2 ④ NO2 ⑤K2CO3 ⑥ Cl2⑦CaO ⑧ NaOH请根据下列标准,对上述物质进行分类:
(1)既含离子键又含共价键的物质是 (填代号,下同)。
(2)只含共价键且为非电解质的是 。
(3)含有共价键的化合物是 。
有H、C、O、Cl、Na五种元素。
(1)在由两种元素组成的化合物里,其中离子化合物有(写2种)______________________,共价化合物有(写2种)______________________。
(2)在由三种元素组成的化合物里,其中离子化合物有(写2种)______________________,共价化合物有(写2种)______________________。
W、X、Y、Z为短周期内除稀有气体元素外的四种元素。它们的原子序数依次增大,其中只有Y是金属元素,Y的最外层电子数和W的最外层电子数相等,X、Z为同一主族,Y、Z两种元素的质子数之和为W、X两种元素质子之和的3倍。由此可知元素W为 ,X为 ,Y为 ,Z 。上述元素中任意三种元素组成的既含有离子键又含有共价键的化合物化学式为 (至少写三种)。能形成共价化合物的化学式有 、 、 、 。
如图所示,把试管放入盛有25 ℃的饱和澄清石灰水的烧杯中,试管开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中,试回答下列问题:
Ⅰ.(1)实验中观察到的现象是
________________________________________________________________________
________________________________________________________________________
(2)产生上述现象的原因是
________________________________________________________________________
________________________________________________________________________
(3)写出有关反应的离子方程式
________________________________________________________________________
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
Ⅱ.已知断开1mol H—H键,1mol N—H键、1 molNN键分别需要吸收的能量为436kJ、391kJ、946kJ。一定条件下由氢气和氮气反应生成1mol NH3需要________(填“放出”或“吸收”)________kJ的热量。
在一体积为10 L的容器中,通过一定量的CO和H2O,850 ℃时发生反应:
CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
(1)CO和H2O浓度变化如图,则0~4 min的平均反应速率v(CO)=______mol·L-1·min-1。
(2)如图中4~5min之间该反应________(填“是”或“否”)处于平衡状态,判断理由________________________________________________________________________。
在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |

(1)A点处,v(正)________v(逆),A点正反应速率________B点正反应速率(用“大于”、“小于”或“等于”填空)。
(2)如图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________________。
(3)能说明该反应已经达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
(4)能使该反应的反应速率增大的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
 粤公网安备 44130202000953号
粤公网安备 44130202000953号