可逆反应:3A 3B+C △H>0,已知反应物A为气态物质,随着温度的升高,反应体系中气体的平均相对分子质量有变小趋势,则下列判断中,正确的是
3B+C △H>0,已知反应物A为气态物质,随着温度的升高,反应体系中气体的平均相对分子质量有变小趋势,则下列判断中,正确的是
①若C为固体,则B一定是气体 ②B和C一定都是气体
③B和C可能都是固体 ④B和C可能都是气体
| A.①② | B.②③ | C.①④ | D.③④ |
下列事实,其中不能用平衡移动原理解释的是
| A.向0.1mol/L的CH3COOH溶液中加入少量CH3COONa固体,溶液pH增大 |
B.在密闭容器中充入一定量NO2建立2NO2(g)  N2O4(g)平衡后,增大压强,体系颜色加深 N2O4(g)平衡后,增大压强,体系颜色加深 |
| C.向水中投入金属Na,最终溶液呈碱性 |
| D.在滴有酚酞的Na2CO3溶液中,慢慢滴入BaCl2溶液,溶液的红色逐渐褪去 |
一定温度下,能说明反应A(g)+2B(g) 3C(g)已达到平衡状态的是( )
3C(g)已达到平衡状态的是( )
| A.C的生成速率与C的分解速率相等 |
| B.单位时间内消耗amolA,同时生成3amolC |
| C.容器内压强不再变化 |
| D.混合气体的物质的量不再变化 |
对于固定体积的密闭容器中进行的气体反应A(g)+B(g)  C(s)+2D(g),可以说明在恒温下已达到平衡状态的是
C(s)+2D(g),可以说明在恒温下已达到平衡状态的是
①反应容器中压强不随时间而变化;②A气体和B气体的生成速率相等;③混合气体的平均摩尔质量不随时间变化而变化;④反应混合气体的密度不随时间而变化
| A.①④ | B.①③ | C.③④ | D.②③ |
下列情况不能用勒夏特列原理解释的是
| A.生活中,用饱和碳酸钠溶液洗去锅碗瓢盆上的油污,且热溶液的效果更好 |
| B.常温下,铁、铝在浓硝酸中钝化 |
| C.侯氏制碱中,降温析出副产品NH4Cl之前,向溶液中既洒NaCl固体又通入足量NH3 |
| D.夏天,打开冰镇汽水瓶,立即冒出大量泡沫 |
下列事实中,不能用勒夏特列原理解释的是( )
| A.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 |
| B.实验室中常用排饱和食盐水的方式收集氯气 |
| C.打开汽水瓶,有气泡从溶液中冒出 |
| D.对熟石灰的悬浊液加热,悬浊液中固体质量增加 |
NO和CO都是汽车尾气中的有害物质,它们能缓慢地起反应,反应的化学方程式为:
2CO+2NO=N2+2CO2,为了控制大气污染,下列措施切实可行的是( )
| A.改变压强 | B.提高温度 |
| C.使用催化剂 | D.用耐高压储气罐收集尾气,集中处理 |
升高温度,下列数据不一定增大的是
A.化学反应速率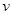 |
B.弱酸的电离平衡常数Ka |
| C.化学平衡常数K | D.水的离子积常数KW |
图像能直观地反映有关物理量的变化及规律,下列各图像与描述相符的是




图1 图2 图3 图4
| A.图1表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图2表示0.1 mol MgCl2·6H2O在空气中充分加热时固体质量随时间的变化 |
| C.图3表示分别稀释1 mL pH=2的盐酸和醋酸时溶液pH的变化,图中b>100mL |
D.图4表示平衡2NO2(g) N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
下列事实不能用勒夏特列原理解释的是
| A.用排饱和食盐水的方法收集氯气 |
| B.在沸腾的蒸馏水中滴加FeCl3溶液,制Fe(OH)3胶体 |
| C.在FeCl3溶液中加AgNO3溶液,产生白色沉淀 |
| D.向AgCl 和水的悬浊液中加入足量的Na2S溶液并振荡,白色固体转化为黑色固体 |
下列有关说法错误的是
| A.室温下的某NaF溶液中,c(H+)=1×10-10 mol∙L-1,说明NaF使水的电离减弱 |
| B.Mg在空气中燃烧时发出耀眼的白光,一部分化学能转化为光能 |
| C.纯碱溶于热水中去污效果增强,说明纯碱的水解是吸热反应 |
| D.反应 N2(g)+3H2(g)=2NH3(g)(△H<0)达平衡后,降低温度,正、逆反应速率都减小,平衡向正反应方向移动 |
下列变化不能用勒夏特列原理解释的是
| A.向H2S水溶液中加入NaOH有利于S2-增多 |
| B.H2、I2、HI 混合气体加压后颜色变深 |
| C.合成氨时将氨液化分离,可提高原料的利用率 |
| D.新制氯水久置后颜色变浅 |
将2molA与2molB混合于2L的密闭容器中发生如下反应:2A(g)+3B(g) 2C(g)+zD(g),2s后A的转化率为50%,测得v(D)=0.25mol•L-1•s-1,下列推断不正确的是( )
2C(g)+zD(g),2s后A的转化率为50%,测得v(D)=0.25mol•L-1•s-1,下列推断不正确的是( )
A.v(C)=v(D)=0.25mol•L-1•s-1 B.z=2
C.C的体积分数为28.6% D.B的转化率为25%
下列事实不能用勒夏特列原理来解释的是( )
| A.加压有利于SO2与O2反应生成SO3 |
| B.用过量氮气与氢气反应可以提高氢气的转化率 |
| C.将混合气中的氨气液化分离,有利于合成氨的反应 |
D.密闭容器中发生反应H2(g)+I2(g)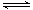 2HI (g),增大压强时容器中颜色加深 2HI (g),增大压强时容器中颜色加深 |
在其他条件不变时,下列说法正确的是( )
| A.增大压强一定会破坏气体反应的平衡状态 |
| B.升高温度可使化学平衡向放热的方向移动 |
| C.使用催化剂只能改变反应速率,不能改变化学平衡状态 |
| D.增大反应物浓度或减小生成物浓度,平衡向逆反应方向移动 |