将1 mol SO2和1 mol O2通入一容积不变的密闭容器中,在一定温度和催化剂作用下,发生反应:2SO2(g)+O2(g) 2SO3(g)。反应达到平衡时SO3为0.3 mol。若此时移走0.5 mol O2和0.5 mol SO2,则重新达到平衡后,SO3的物质的量
2SO3(g)。反应达到平衡时SO3为0.3 mol。若此时移走0.5 mol O2和0.5 mol SO2,则重新达到平衡后,SO3的物质的量
| A.等于0.3 mol | B.等于0.15 mol |
| C.小于0.15 mol | D.大于0.15 mol,小于0.3 mol |
下列事实不能用勒夏特列原理解释的是
| A.棕红色NO2加压后颜色先变深后变浅 |
| B.钢铁在潮湿的空气中容易生锈 |
| C.实验室可用排饱和食盐水的方法收集氯气 |
| D.常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5 |
对于可逆反应A(g)+2B(g) 2C(g) △H>0,下列图象中正确的是
2C(g) △H>0,下列图象中正确的是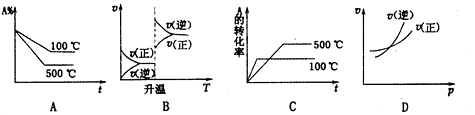
根据下列实验现象,所得结论错误的是
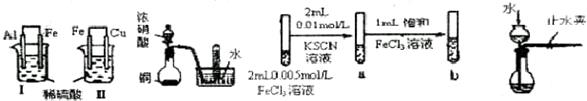
| 实验 |
实验现象 |
结论 |
| A |
Ⅰ烧杯中铁片表面有气泡,Ⅱ烧杯中铜片表面有气泡 |
活动性Al>Fe>Cu |
| B |
试管中收集到无色气体 |
铜与浓硝酸反应产物是NO |
| C |
试管b比试管a中溶液的红色深 |
增大反应物浓度,平衡向正反应方向移动 |
| D |
长颈漏斗内液面高于烧瓶内液面且保持不变 |
装置气密性良好 |
向某恒容密闭容器中充入一定量C02和H2,发生反应: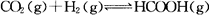 测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量 中,a点大于b点的是
测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量 中,a点大于b点的是

①:正反应速率 ②逆反应速率 ③HCOOH(g)的浓度 ④对应温度时的平衡常数
| A.①② | B.①③ | C.②④ | D.③④ |
合成氨反应:N2(g)+3H2(g) 2NH3(g)ΔH="-92.4" kJ·mol-1,在反应过程中,正反应速率的变化如图所示:
2NH3(g)ΔH="-92.4" kJ·mol-1,在反应过程中,正反应速率的变化如图所示:
下列说法正确的是
| A.t1时升高了温度 | B.t2时使用了催化剂 |
| C.t3时增大了压强 | D.t4时降低了温度 |
在一定温度下的定容容器中,发生反应:2A(g)+B(s) C(g)+D(g),下列描述中能表明反应已达到平衡状态的是
C(g)+D(g),下列描述中能表明反应已达到平衡状态的是
①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内A、C、D三种气体的浓度之比为2:1:1
⑤单位时间内生成n molD,同时生成2n mol A.
⑥单位时间内生成n molC,同时消耗n mol D.
A.①②③ B.③④⑥ C.②③⑤⑥ D.只有 ③
现有下列两个图象:下列反应中符合上述图象的是
A.N2(g)+3H2(g) 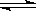 2NH3(g) ΔH<0 2NH3(g) ΔH<0 |
B.2SO3(g) 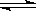 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
C.4NH3(g)+5O2(g) 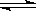 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
D.H2(g)+CO(g) 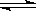 C(s)+H2O(g) ΔH>0 C(s)+H2O(g) ΔH>0 |
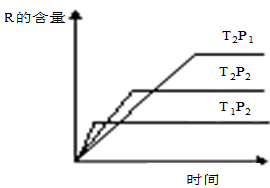
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+ 3B2(g)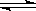 2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
A.若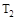 > >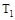 ,则正反应是放热反应 ,则正反应是放热反应 |
B.达到平衡时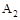 的转化率大小为:b>a>c 的转化率大小为:b>a>c |
C.若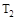 > >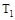 ,达到平衡时b、d点的反应速率为 ,达到平衡时b、d点的反应速率为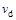 > >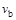 |
D.在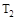 和 和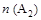 不变时达到平衡, 不变时达到平衡,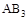 的物质的量大小为:c>b>a 的物质的量大小为:c>b>a |
只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是
| A.K值不变,平衡可能移动 | B.K值变化,平衡一定移动 |
| C.平衡移动,K值可能不变 | D.平衡移动,K值一定变化 |
在密闭容器中进行下列反应:M (g)+N (g)  R (g)+2 L此反应符合下面图像。下列叙述正确的是
R (g)+2 L此反应符合下面图像。下列叙述正确的是
| A.正反应放热,L是气体 |
| B.正反应吸热,L是固体 |
| C.正反应吸热,L是气体 |
| D.正反应放热,L是液体 |
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮(甲)和空气(乙),现分别进行下列两项实验:
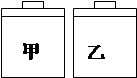
(N2O4 2NO2 △H> 0)
2NO2 △H> 0)
(a)将两容器置于沸水中加热 (b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是
| A.(a)甲>乙,(b)甲>乙 | B.(a)甲>乙,(b)甲=乙 |
| C.(a)甲<乙,(b)甲>乙 | D.(a)甲>乙,(b)甲<乙 |
下列叙述中,不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成SO3的反应 |
| C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D.黄绿色的氯水光照后颜色变浅 |