计算:
(1)同温同压下的两个相同容器中分别装有O2和O3气体,则两瓶气体中分子数之比是 ,质量之比是 ,密度之比是
(2)下列所给出的几组物质中:含有分子数最多的是 ;含有原子数最多的是 ;标准状况下体积最大的是 。(填序号)
①1gH2; ②2.408×1023个CH4;③10.8gH2O; ④ 标准状况下6.72LCO2
(3)设NA表示阿伏加德罗常数,如果ag某气体含有的分子数是b,则cg该气体在标准状况下的体积是 (用含NA的式子表示)。
(4)工业上,向500—600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行试验。

回答下列问题:
①制取无水氯化铁的实验中,装置B中加入的试剂是 。
②制取无水氯化亚铁的实验中若操作不当,制得的FeCl2会含有少量FeCl3,欲制得纯净的FeCl2,在实验操作中应先 ,再 。
MnO2是一种重要的无机功能材料。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯净MnO2的实验,其流程如下:
请回答下列问题:
(1)第①步加稀硫酸时,粗MnO2样品中的MnO和MnCO3转化为(填化学式)_______________。
(2)第①步反应中的硫酸能否用盐酸代替?____________(填“能”或“否”),理由是____________。
(3)第②步发生反应的离子方程式为:___________________________。
(4)取17.4gMnO2与200g36.5%的浓盐酸(足量)反应,将反应后剩余的溶液用水稀释至500mL,计算稀释后溶液中Cl-的物质的量浓度(写出计算过程)。
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意图如下:

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3+ + Fe ="===" 3Fe2+ 2TiO2+(无色)+ Fe + 4H+="===" 2Ti3+(紫色)+ Fe2++2 H2O
Ti3+(紫色)+ Fe3++ H2O ====TiO2+(无色)+ Fe2++2H+
加入铁屑的作用是 。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在_________范围。
(3)写出④中TiO2和焦炭、氯气反应的化学方程式:______________________________。
(4)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是 (只要求写出一项 )。
(5)依据表格信息,要精制含少量SiCl 4杂质的TiCl 4,可采用 方法。
| |
TiCl4 |
SiCl4 |
| 熔点/℃ |
-25.0 |
-68.8 |
| 沸点/℃ |
136.4 |
57.6 |
孔雀石主要含Cu2(OH)2CO3,还含少量FeO、SiO2。以孔雀石为原料可制备CuSO4·5H2O步骤如下:

(1).写出孔雀石与稀硫酸反应的化学方程式:____________ ,
为了提高原料浸出速率,可采取的措施有______________________(写出两条)。
(2). 溶液A的金属离子有Cu2+、Fe2+。实验步骤中试剂①最佳选 (填代号)。
a.KMnO4 b.Cl2 c.H2O2 d.HNO3
(3)溶液B中加入CuO作用是__________________ _______________。
(4)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10—3mol/L,必需将溶液pH调节至 。
(5)由溶液C获得CuSO4·5H2O晶体,需要经_____________、___________和过滤。
(6)可用KMnO4标准溶液测定溶液A中Fe2+的浓度,量取A溶液20.00ml,用0.010mol/L酸性KMnO4标准溶液滴定,消耗KMnO4 10.00ml, A溶液中Fe2+的物质的量浓度_________mol/L.
(反应原理:MnO4- + 5Fe2++8H+=Mn2++5Fe3++4H2O)
以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:



 (1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
(1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
| A.锌粉 | B.铁屑 | C.KI溶液 | D.H2 |
 (2)反应Ⅰ需控制反应温度低于35℃,其目的是 。
(2)反应Ⅰ需控制反应温度低于35℃,其目的是 。 (3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是 。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是 。 (4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为 。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为 。
制取氨气并完成喷泉实验(图中夹持装置均已略去)。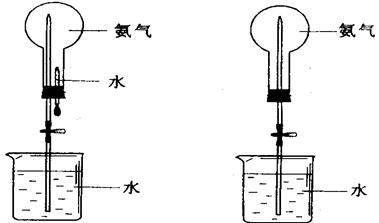
(1)写出实验室制取氨气的化学方程式:___________________________ 。
(2)收集氨气应使用 法,要得到干燥的氨气可选用 做干燥剂。用______方法检验氨气是否已收集满。
(3)用左上图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是 。
硫酸锌是制备荧光粉的原料之一。工业上由锌白矿(主要成分是ZnO,还含有Fe2O3、CuO、SiO2等杂质)制备ZnSO4•7H2O的流程如下。
已知:常温下,溶液中的Fe3+、Zn2+、Fe2+以氢氧化物形式完全沉淀的pH分别为:3.7,6.5,9.7。
(1)浸取过程中提高浸出效率可采用的措施有 (任答一条),ZnO和硫酸反应的化学方程式为 。
(2)加入适量锌粉的作用为:①使溶液中的Fe3+转化为Fe2+;② 。
(3)氧化过程中H2O2发生反应的离子方程式为 。
(4)加入适量Ca(OH)2调节溶液pH,促进Fe3+水解,Fe3+水解反应的平衡常数表达式K= ,Ca(OH)2不能过量的原因是 。
(12分)高氯酸钠可用于制备高氯酸。以精制盐水等为原料制备高氯酸钠晶体(NaClO4·H2O)的流程如下: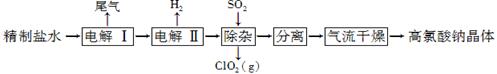
(1)由粗盐(含Ca2+、Mg2+、SO42-、Br-等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。Na2CO3的作用是____________;除去盐水中的Br-可以节省电解过程中的电能,其原因是____________。
(2)“电解Ⅰ”的目的是制备NaClO3溶液,产生的尾气除H2外,还含有________(填化学式)。“电解Ⅱ”的化学方程式为__________________________________________。
(3)“除杂”的目的是除去少量的NaClO3杂质,该反应的离子方程式为______________。
“气流干燥”时,温度控制在80~100 ℃的原因是________________________。
七铝十二钙(12·7
)是新型的超导材料和发光材料,用白云石(主要含
和
)和废
片制备七铝十二钙的工艺如下:

(1)煅粉主要含和,用适量的
溶液浸取煅粉后,镁化合物几乎不溶, 若溶液I中
(
)小于5×10-6
,则溶液
大于(
的
=5×10-12);该工艺中不能用
代替
,原因是。
(2)滤液I中的阴离子有(忽略杂质成分的影响);若滤液I中仅通入,会生成,从而导致
产率降低。
(3)用溶液可除去废
片表面的氧化膜,反应的离子方程式为。
(4)电解制备时,电极分别为
片和石墨,电解总反应方程式为。
(5)一种可超快充电的新型铝电池,充放电时和
两种离子在
电极上相互转化,其它离子不参与电极反应,放电时负极
的电极反应式为。
[化学——选修2:化学与技术](15分)最近的研究发现,复合氧化物铁酸锰(MnFe2O4)可以用于热化学循环分解水制氢,因而受到许多发达国家的青睐。MnFe2O4的制备流程如下: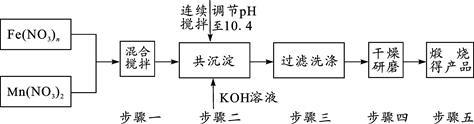
(1)原料Fe(NO3)n中n=____,投入原料Fe(NO3)n和Mn(NO3)2的质量之比应为______。
(2)步骤二中“连续搅拌”的目的是___________________________________________;
步骤三中洗涤干净的标准_____________________________________________。
(3)利用MnFe2O4热化学循环制氢的反应可表示为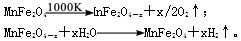
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中x=0.6,则MnFe2O4-x中Fe2+占全部铁元素的百分率为_______。
②该热化学循环新氢法的优点有____________________________(答两点即可)。
③该热化学循环法制氢尚有不足之处,进一步改进的研究方向是_____________。
“烂版液”是制印刷锌板时,用稀硝酸腐蚀锌板后得到的“废液”(含有少量的Cl-、Fe3+),某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下:
已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的固体产物具有两性。
(1)若稀硝酸腐蚀锌板产生的气体N2O,写出稀硝酸腐蚀锌板反应的主要化学方程式 。
(2)在操作①中保持pH=8的目的是 。
(3)沉淀I的主要成分是 。
(4)操作③中加热、煮沸的目的是 ;
此步骤操作的理论依据是 。
(5)操作④保持pH=2的目的是 ;
此步骤操作中所用的仪器有带铁圈铁架台、酒精灯、 、 。
(1)配制0.5mol/L的NaOH溶液,定容时向容量瓶中加蒸馏水超过刻度线,其结果 (填“偏大”、“偏小”、或“不变”)。
(2)从石油中分离出汽油、煤油和柴油等,所采用的方法是__________(填“干馏”或“分馏”)。
(3)除去二氧化碳气体中的氯化氢杂质,选用的试剂是_______ __(填“NaOH溶液”或“饱和NaHCO3溶液”)。
(4)下图是实验室制取氨气的装置,回答下列问题:
①收集氨气的方法是 排空气法。
②验证氨气是否收集满的方法是 (写一种)。
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:

根据题意回答下列问题:
(1)实验中需用1 mol·L-1的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有 。
(2)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式: 。
(3)在调节pH=5~6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为: 。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法 。
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) |
40 |
50 |
60 |
70 |
| MgSO4 |
30.9 |
33.4 |
35.6 |
36.9 |
| CaSO4 |
0.210 |
0.207 |
0.201 |
0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明主要操作步骤 、 。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的产率为 。
下图中的实验装置可以用于实验室制取乙炔。请填空: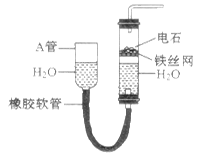
(1)图中A管的作用是 ,制取乙炔的化学反应方程式为 。
(2)乙炔通入酸性KMnO4溶液中,发生 反应,可以观察到的现象为 ,
若通入溴水中,发生 反应,反应方程式为 。
(3)乙炔燃烧的化学方程式为 ,燃烧时的现象为 ,
为了安全,点燃乙炔前应该先 。
镁橄榄石主要成分是Mg2SiO4,电解法促进镁橄榄石固定CO2的工艺流程如下图所示:
已知:Mg2SiO4(s)+4HCl(aq) 2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
固碳时主要反应的方程式为NaOH(aq)+CO2(g)=NaHCO3(aq)。
(1)上图方框里的操作名称是 ,横线上的物质有(填化学式) 。
(2)下列物质中也可用作“固碳”的是(填字母序号) 。
| A.CaCl2 | B.NH3·H2O |
| C.Na2CO3 | D.H2O |
(3)由下图可知,90 ℃后曲线A溶解效率下降,分析其原因 。
(4)经分析,所得碱式碳酸镁沉淀中含有少量NaCl。为提纯,可采取的方法是 。本流程中可循环利用的物质是(填化学式) 。
(5)另一种橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为 。