榴石矿石可以看作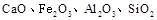 组成,由榴石矿石制取氯化钙和氧化铝的实验步骤如下:
组成,由榴石矿石制取氯化钙和氧化铝的实验步骤如下: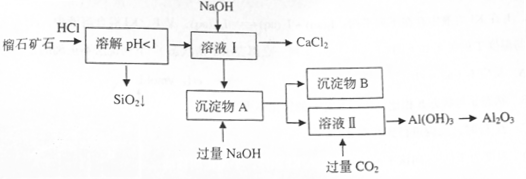
(1)榴石矿加盐酸溶解后,溶液里除了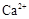 外,还含有的金属离子是 。
外,还含有的金属离子是 。
(2)对溶液I进行操作时,控制溶液PH=9~10(有关氢氧化物沉淀的PH见下表)
NaOH不能过量,若NaOH过量可能会导致 溶解, 沉淀。
(3)写出向沉淀物A中加入过量氢氧化钠溶液的离子方程式 。
(4)①某同学在实验室中用图I装置制取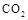 气体并通入溶液II中,结果没有沉淀产生,可能的原是 ;为了能产生沉淀该同学对图I装置进行了改进,改进的方法为 。
气体并通入溶液II中,结果没有沉淀产生,可能的原是 ;为了能产生沉淀该同学对图I装置进行了改进,改进的方法为 。
②若将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系 。
草酸晶体的化学式可表示为H2C2O4·xH2O,为测定x值进行下列实验:
(1)称取W g草酸晶体,配成100.00 mL溶液。
(2)取25.00 mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为a mol·L-1KMnO4溶液滴定。
KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O(未配平)
回答下列问题:
①实验(1)中,为配制准确的草酸溶液,必须使用的仪器有_____________________________;
②实验(2)中,滴定时,KMnO4溶液应盛在___________中(填酸式或碱式滴定管);
③若滴定用的KMnO4溶液因放置而变质,浓度偏低,则根据实验求出的x值______(填偏高、偏低、无影响);
④滴定终点时,锥形瓶内溶液颜色变化是__________________________________;
⑤若滴定终点时,共用去KMnO4溶液V mL,求草酸溶液的物质的量浓度及x的值:
, .
在下图所示的实验装置中,A中盛有品红溶液,B 中盛有NaOH溶液。
请回答下列问题:
(1) 若向A中通入足量的二氧化硫气体,A中的现象是 。
(2) 若向A中通入足量的氯气后,再加热A,A中的溶液
(填“能”或“不能”)恢复到原来的颜色。
应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
(1)写出该反应的化学方程式  ,其中氧化剂是 , 8.4g铁粉参加反应,转移电子 mol。
,其中氧化剂是 , 8.4g铁粉参加反应,转移电子 mol。
(2)干燥管内使用的干燥剂可以是下列物质中的 (填序号)。
①浓硫酸 ②碳酸钠 ③碱石灰 ④过氧化钠
(3)硬质玻璃管中石棉绒的作用是 ,圆底烧瓶中盛装水和 ,加入后者的作用是 。
(4)实验开始时应先点燃 ,实验结束时应先熄灭 ,检验生成的气体 的方法是 。
的方法是 。
实验室制取下列气体时,应选用下列哪种酸:(填入相应的字母。)
| A.浓盐酸 | B.稀盐酸 | C.稀硫酸 | D.浓硫酸 |
⑴用大理石和 制CO2 ; ⑵用MnO2和 制Cl2;
⑶用锌粒和 制H2 ; ⑷用食盐和 制HCl。
“烂板液”是制印刷锌板时,用稀HNO3腐蚀锌板后得到的废液,主要含Zn(NO3)2和由自来水带进的Cl-、Fe3+等杂质离子。在实验室中由“烂板液”制取ZnSO4·7H2O的过程如下:
已知有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe3+ |
1.9 |
3.2 |
| Zn2+ |
6.4 |
8.0 |
(1)沉淀B的主要成分是 。
(2)第②步操作中需要的玻璃仪器有 。
(3)第④步中pH应保持在 范围内。
(4)第⑥步调节溶液pH=2的目的是 。
(5)操作⑦包含3个基本实验操作,它们是蒸发浓缩、 和过滤。
实验室制取乙烯的装置如右图所示,请回答:
(1)反应中浓硫酸起 剂和 剂的作用。
(2)该实验可能产生的主要有机副产物是 。(写名称)
(3)制取乙烯的反应的化学方程式是: 。
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置制取乙酸乙酯。回答下列问题:
⑴写出制取乙酸乙酯的化学反应方程式:
。
⑵饱和碳酸钠溶液的主要作用是: 。
。
⑶装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑷做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
利用以下装置探究氯气的性质。
(1)写出实验室制取C12的化学方程式 ;
实验室制取氯气需要用到的仪器有 (填写序号)。
①分液漏斗②碱式滴定管⑧酒精灯④圆底烧瓶⑤长颈漏斗
(2)若E中的干燥有色布条:不褪色,则D中盛有的试剂是 。
(3)G中盛有NaOH溶液,写出发生反应的离子方程式 。
(4)F中盛有蒸馏水,C12通过后可观察到溶液的颜色变为 色,说明溶液中存在 ;将该溶液加入含有酚酞的氢氧化钠溶液中,溶液红色褪去。设计实验探究红色褪去的原因
。
(5)若F中盛有的是溴化亚铁溶液,通入过量C12后,写出可能发生反应的离子 方程式 。
方程式 。
实验室中所用少量氯气用下列方法制取:4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O试回答下列问题:
Cl2↑+MnCl2+2H2O试回答下列问题:
(1)该反应中 是氧化剂,氧化剂和还原剂的物质的量之比为 。写出该反应的离子方程式 。
(2)若用右图装置收集氯气,气体应从 口进入。
(3)氯气有毒、且氯气溶入水显酸性,请写出氯气溶于水的离子方程式
,若吸入大量氯气,可中毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用NaOH溶液来吸收有毒的氯气,化学方程式为 。
海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
(1)指出提取碘的过程中有关的实验操作名称:① ,③ ;
(2)提取碘的过程中,可选择的有机试剂是 。
A.酒精 B.四氯化碳 C.苯
(3)实验操作③中,实验室已有烧杯、玻璃棒以及必要的夹持仪器,尚缺少的玻璃仪器是 。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
① ;
② ;
③ 。
(5)进行上述蒸馏操作时,使用水浴加热的原因是:
,
最后晶态碘在 里聚集(填仪器名称)。
验需要0.1mol/LNaOH溶液450mL,根据溶液配制中情况回答下列问题:
⑴ 实验中不需要的仪器有:
A.托盘天平 B. 烧杯 C. 500 mL容量瓶 D.玻璃棒 E.滴管 F.铁架台 G.烧瓶 H.酒精灯
⑵ 根据计算得知,所需NaOH的质量为 g
⑶ 下列操作对所配浓度有何影响(填写字母)
偏大的有 ;偏小的有 ;无影响的有 。
A、称量时用了生锈的砝码;
B、将NaOH放在纸张上称量;
C、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
D、往容量瓶转移时,有少量液体溅出
E、未洗涤溶解NaOH的烧杯
F、定容时仰视刻度线
G、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,不再加水。
H、容量瓶底部未干燥即用来配制溶液
某次实验需用480 mL、0.5 mol/L 的稀H2SO4溶液,某同学用98%的浓H2SO4 (ρ="1.84" g/cm3)进行配制,请回答下列问题:
(1)98%的浓H2SO4(ρ="1.84" g/cm3)的物质的量浓度为
(2)将下列步骤中的空格内将所用仪器补充填写完整
①用20 mL量筒量取所需的浓硫酸
②将烧杯中的溶液转移到 mL的容量瓶中
③将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
④将溶液冷却,恢复室温
⑤向容量瓶中加入蒸馏水,在距离刻度1~2 cm时,改用 加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦洗涤烧杯2~3次,洗涤液也注入容量瓶中。轻轻摇动容量瓶,使溶液混合均匀。
(3)实验中上述步骤的正确顺序为 (填序号)。
(4)在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”)。
①所用的浓硫酸长时间放置在密封不好的容器中
②量取浓硫酸所用量筒有蒸馏水
③定容时,俯视液面
某废液中主要含有NaCl、NaI,实验室从该废液中回收I2和NaCl的流程如下:
回答下列问题:
(1)在步骤①中通入的Cl2与NaI发生置换反应生成I2,其反应的化学方程式为
__________________________________________________________________________。
(2)步骤②操作名称是 ,用到的玻璃仪器有________________________。
(3)下层液体Z的颜色是 ,步骤④操作的名称是 。
(4)要从上层液体Y中得到NaCl晶体,步骤③操作中需要的实验仪器有_______________。
| A.试管 | B.蒸发皿 | C.漏斗 | D.玻璃棒 E.坩埚 F.酒精灯 G.烧瓶 |
制备氢氧化铁胶体的方法是
,可通过 来区别溶液和胶体。