25 ℃时,x mol·L-1氢氟酸水溶液中,加入KOH固体调节溶液的pH(忽略加入固体引起的溶液体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示。下列说法正确的是 ( )。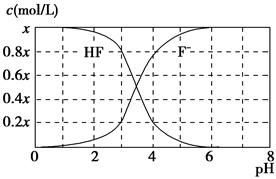
| A.当c(F-)>c(HF)时,溶液呈碱性 |
| B.当pH=2时,c(F-)<c(K+) |
| C.25 ℃时,氢氟酸的电离平衡常数为4×10-6 |
| D.当pH=5时,c(HF)+c(K+)+c(H+)-c(OH-)=x mol·L-1 |
25℃时,下列关于分别由等体积0.1 mo1/L的2种溶液混合而成的溶液的说法中,不正确的是 ( )
| A.Ba(OH)2溶液与Na2SO4溶液:pH=13 |
| B.醋酸与CH3COONa溶液:c(Na+)+c(H+)=c(CH3COO一)+c(OH一) |
C.Na2CO3溶液与NaOH溶液:c(Na+)>c( CO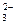 )>c(OH一)>c(H+) )>c(OH一)>c(H+) |
D.Na2CO3溶液与NaHCO3溶液:2c(Na+)= 3c(CO 3c(CO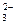 )+3c(HCO )+3c(HCO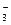 )+3c(H2CO3) )+3c(H2CO3) |
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看做是化学平衡的一种。请根据所学化学知识回答下列问题:
Ⅰ、已知0.01mol/L的NaHCO3溶液呈碱性。
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:
① ② ③ 。
(2)溶液中共有 种不同的粒子(指分子和离子)。
(3)该溶液中的离子浓度由大到小的顺序是: 。
(4)向该溶液中加入AlCl3溶液,有白色胶状沉淀生成,同时产生一种无色无味并能使澄清石灰水变浑浊的气体,写出该反应的离子方程式: 。
已知2Fe2+ +Br2=2Fe3++2Br-。向10mL0.1mol·L-1的FeBr2溶液中通入0.001mol Cl2,反应后的溶液中,除含有Cl—外还一定( )
| A.含Fe2+,不含Fe3+ | B.含Fe3+,不含Br- |
| C.含Fe3+,含有Br- | D.含Fe2+,含有Fe3+ |
常温下,将少量水加入下列物质中,相关量变化正确的是
| A.AgCl悬浊液中 c(Cl-)变小 | B.0.1mol/LCH3COOH溶液中 c(H+)变小 |
| C.0.1mol/LNa2CO3 c(HCO3-)变大 | D.0.1mol/LNH4Cl溶液中 n(OH-)变小 |
25 ℃时,在25 mL 0.1 mol/L的NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,混合溶液pH的变化曲线如图所示,下列分析结论正确的是
| A.a=12.5,且混合溶液pH=7 |
| B.对应曲线上E、F之间的任何一点,溶液中都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C.P点时,c(CH3COO-)>c(Na+)>c(H+)=c(OH-) |
| D.K点时,c(CH3COO-)+c(CH3COOH)=2c(Na+) |
常温下,有物质的量浓度均为0.1mol·L—1的CH3COOH溶液和NaOH溶液,下列说法正确的是
| A.CH3COOH溶液的pH=1 |
| B.往醋酸溶液中加水,c(OH—) 和c(H+)均增大 |
| C.两溶液等体积混合, c(Na+)﹥c(CH3COO—) |
| D.两溶液按一定体积比混合,可能存在:c(CH3COO—) ﹥c(Na+) |
水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与 碱性悬浊液(含有 )混合,反应生成 ,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化, 被 还原为 ,在暗处静置 ,然后用标准 溶液滴定生成的 ( )。
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_____________。
(2)"氧的固定"中发生反应的化学方程式为_______________。
(3) 溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和____________;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除____及二氧化碳。
(4)取 水样经固氧、酸化后,用 溶液滴定,以淀粉溶液作指示剂,终点现象为________________;若消耗 溶液的体积为 ,则水样中溶解氧的含量为_________mg·L − 1。
(5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测量结果偏___________。(填"高"或"低")
下列实验操作能达到实验目的的是( )
| A. |
用长颈漏斗分离出乙酸与乙醇反应的产物 |
| B. |
用向上排空气法收集铜粉与稀硝酸反应产生的 NO |
| C. |
配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 |
| D. |
将 与 混合气体通过饱和食盐水可得到纯净的 |
下列有关说法正确的是
A.一定条件下反应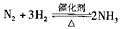 ,达到平衡时, ,达到平衡时,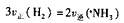 |
| B.10mL浓度为1mol/L的盐酸与过量的Zn粉反应,若加入适量的CH3COONa溶液,既能减慢反应这率,又不影响H2的生成 |
C.将PH=a十l的氨水稀释为pH=a的过程中,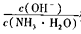 变小 变小 |
| D.常温下,向浓度为0.1 mol/L的CH3COONa溶液中加入等体积等浓度的CH3COOH,混合溶液的pH=7 |
下列叙述正确的是
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 |
| B. |
25℃时,等体积等浓度的硝酸与氨水混合后,溶液
|
| C. |
25℃时,0.1
|
| D. |
0.1
|
下列说法正确的是( )
| A.pH=4的溶液中水电离出的H+一定是1×10-4mol/L |
| B.25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH |
| C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D.AgCl沉淀易转化为AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)<K(AgCl) |
下列说法中,正确的是
| A.25℃时,1L pH=3的盐酸和醋酸能消耗等质量的镁粉 |
| B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)将增大 |
| C.V1L pH=12的NaOH溶液与V2L pH=2的HA溶液混合,若混合液显中性,则V1≤V2 |
| D.在0.1mol·L-1 NaHCO3溶液中,加入少量NaOH固体,Na+和CO32―离子浓度均增大 |
25℃时,浓度均为0.2 mol/L的NaHCO3溶液中,下列判断不正确的是 ( )
A.存在电离平衡HCO H++CO32— H++CO32— |
B.存在水解平衡HCO+H2O H2CO3+OH- H2CO3+OH- |
| C.将溶液加热蒸干、灼烧得Na2O2固体 |
| D.加入NaOH固体,恢复到原温度,c(OH-)、c(CO32—)均增大 |