2015年全国统一高考理综试卷(重庆卷)化学部分
中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是()
| A. | 用胆矾炼铜 | B. | 用铁矿石炼铁 |
| C. | 烧结粘土制陶瓷 | D. | 打磨磁石制指南针 |
下列说法正确的是
下列叙述正确的是
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 |
| B. | 25℃时,等体积等浓度的硝酸与氨水混合后,溶液 =7 |
| C. | 25℃时,0.1 的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 |
| D. | 0.1 和0.1 混合后加入1 水中,所得溶液中 |
某化妆品的组分具有美白功效,原从杨树中提取,现可用如下反应制备:
 下列叙述错误的是()
下列叙述错误的是()
| A. | 、 和 均能使溴水褪色 |
| B. | 和 均能与 溶液反应放出 |
| C. | 既能发生取代反应,也能发生加成反应 |
| D. | 可作加聚反应单体,X可作缩聚反应单体 |
羰基硫()可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将和混合加热并达到下列平衡:
 =0.1
=0.1
反应前物质的量为10,平衡后物质的量为8。下列说法正确的是
| A. | 升高温度, 浓度增加,表明该反应是吸热反应 |
| B. | 通入 后,正反应速率逐渐增大 |
| C. | 反应前 物质的量为7 |
| D. | 的平衡转化率为80% |
某汽车安全气囊的产气药剂主要含有、、、等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)是气体发生剂,受热分解产生和,的电子式为。
(2)是主氧化剂,与反应生成的还原产物为(已知该反应为置换反应).
(3)是助氧化剂,反应过程中与作用生成和。含有化学键的类型为,的原子结构示意图为。
(4)是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为。
(5)100上述产气药剂产生的气体通过碱石灰后得到 33.6(标准状况)。
①用碱石灰除去的物质为;
②该产气药剂中的质量分数为。
与的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
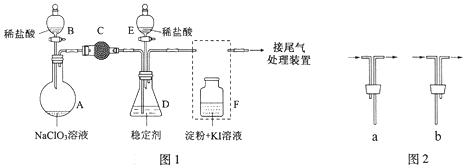
(1)仪器的名称是。安装中导管时,应选用图2中的。
(2)打开的活塞,A中发生反应:+=↑+↑++。
为使在中被稳定剂充分吸收,滴加稀盐酸的速度宜 (填"快"或"慢")。
(3)关闭的活塞,在中被稳定剂完全吸收生成,此时中溶液的颜色不变,则装置的作用是。
(4)已知在酸性条件下NaClO2可发生反应生成并释放出,该反应的离子方程式为,在释放实验中,打开的活塞,中发生反应,则装置的作用是 。
(5)已吸收气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是,原因是 。

某"化学鸡尾酒"通过模拟臭虫散发的聚集信息素可高效诱捕臭虫,其中一种组分可通过下列反应路线合成(部分反应条件略)。

(1)的化学名称是,新生成的官能团是;
(2)的核磁共振氢谱显示峰的组数为 。
(3)的化学方程式为。
(4)与新制的发生反应,所得有机物的结构简式为。
(5)可由与发生加成反应而得,已知,则的结构简式为。
(6)已知
 ,则的结构简式为。
,则的结构简式为。
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)原子序数为29的铜元素位于元素周期表中第周期。
(2)某青铜器中、的质量分别为119、20.7,则该青铜器中和原子的数目之比为。
(3)研究发现,腐蚀严重的青铜器表面大都存在。关于在青铜器腐蚀过程中的催化作用,下列叙述正确的是。
| A. | 降低了反应的活化能 | B. | 增大了反应的速率 |
| C. | 降低了反应的焓变 | D. | 增大了反应的平衡常数 |
(4)采用"局部封闭法"可以防止青铜器进一步被腐蚀。如将糊状涂在被腐蚀部位,与有害组分发生复分解反应,该化学方程式为。
(5)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是(填图中字母""或""或"");
②环境中的扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈,其离子方程式为;
③若生成4.29 ,则理论上耗氧体积为(标准状况)。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号