有Fe2+﹑NO3-﹑Fe3+、NH4+﹑H2O和H+六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是
| A.氧化剂与还原剂的物质的量之比为8∶1 |
| B.还原产物为NH4+ |
| C.若有1 mol NO3-参加还原反应,则转移8mol e- |
| D.若把该反应设计为原电池,则负极反应为Fe2+—e-= Fe3+ |
已知下列物质都能氧化H2S,它们氧化H2S时自身分别发生下列变化:Fe3+→Fe2+,Cr2O72-→2Cr3+,Br2→2Br-,HNO3→NO。如要氧化等物质的量的H2S气体得到S单质,需要上述离子或物质的物质的量最小的是
| A.Fe3+ | B.Br2 | C.Cr2O72— | D.HNO3 |
对于氧化还原反应8Fe(NO3)2+10HNO3=8Fe(NO3)3+NH4NO3+3H2O,以下叙述错误的是 ( )
| A.还原产物为NH4NO3 |
| B.氧化剂与还原剂的物质的量之比为8:1 |
| C.若有1 mol NO3-参加还原反应,则转移8mol电子 |
| D.若应用该反应设计原电池,原电池的负极反应可表示为Fe2+-e-=Fe3+ |
在反应5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,氧化剂是__________,还原剂是__________;氧化剂具有__________性;被氧化和被还原的原子数之比是__________。
在2KMnO4 +16HCl ="==" 2KCl +2MnCl2 + 5Cl2↑+8 反应中
| A.Cl2是还原产物 |
| B.处对应的物质为H2O |
| C.氧化剂与还原剂物质的量之比为1∶8 |
| D.若1mol KMnO4参加反应,转移的电子的物质的量是5mol |
在KClO3+6HCl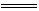 KCl+3Cl2↑+3H2O的反应中,被氧化的氯原子与被还原的氯原子的原子个数比是( )
KCl+3Cl2↑+3H2O的反应中,被氧化的氯原子与被还原的氯原子的原子个数比是( )
| A.1:6 | B.1:5 | C.6:1 | D.5:1 |
已知OCN-中每种元素都满足8电子稳定结构,在反应OCN-+OH-+C12→CO2+N2+C1-+H2O(未配平)中,如果有6 mol C12完全反应,则被氧化的OCN-的物质的量是
| A.2 mol | B.3 mol | C.4 mol | D.6 mol |
在5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,被氧化的氯元素与被还原的氯元素的质量比为:
| A.1:1 | B.5:1 | C.1:5 | D. 3:1 3:1 |
关于反应K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O的叙述中,正确的是
| A.KCl中含有35Cl | B.生成物Cl2的相对分子质量为73.3 |
| C.该反应转移的电子数为6e- | D.氧化剂和还原剂的物质的量之比为1:6 |
多硫化钠Na2Sx(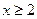 )在结构上与Na2O2,FeS2等有相似之处,Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的量之比为1:16,则x值是
)在结构上与Na2O2,FeS2等有相似之处,Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的量之比为1:16,则x值是
| A.5 | B.4 | C.3 | D.2 |
工业上冶炼铁有化学方程式如下:Fe2O3+3CO 2Fe+3CO2,在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为( )
2Fe+3CO2,在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为( )
| A.3︰1 | B.2︰3 | C.1︰3 | D.3︰5 |
在3Cl2 + 6KOH = KClO3 + 5KCl + 3H2O的反应中,氧化剂和还原剂的质量比为( )
| A.2:1 | B.5:1 | C.1:1 | D.1:5 |
在xR2+ +yH+ +O2=mR3+ +nH2O的离子方程式中,
(1)m=________(填数字)
(2)R3+是___________(填氧化产物、还原产物)
(3)用双线桥法表示电子转移的方向和数目___________
(4)若氧化等量的R2+,消耗的高锰酸钾与氧气的物质的量之比为___________,