(1)KClO3与浓盐酸发生反应:KClO3+6HCl(浓)= KCl+3Cl2↑+3H2O,该反应中被氧化的元素和被还原的元素的质量之比为__________。转移1 mol电子时,产生标准状况下的Cl2__________ L。
(2)与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上用亚氯酸钠和稀盐酸为原料制备ClO2反应: NaClO2+HCl→ClO2↑+NaCl+H2O
写出配平的化学方程式________________。生成0.2 mol ClO2转移电子的物质的量为________ mol。
(3)取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为__________________。如果向FeBr2溶液中通入等物质的量的Cl2,该反应的离子方程式为___________________________。
草酸晶体的化学式可表示为H2C2O4·xH2O,为测定x值进行下列实验:
(1)称取wg草酸晶体,配成100.00 mL溶液。
(2)取25.00mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为a mol/LKMnO4溶液滴定。KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O(未配平)
回答下列问题:
①滴定时,KMnO4溶液应盛在__________(填酸式或碱式)滴定管中;
②若滴定用的KMnO4溶液因放置而变质,浓度偏低,则根据实验求出的x值______(填偏高、偏低或无影响);
③滴定终点时,锥形瓶内溶液颜色变化是_____________________;
④若滴定终点时,共用去KMnO4溶液V mL,求x的值为________________。
下图所示为含Cr化合物在一定条件下的转化: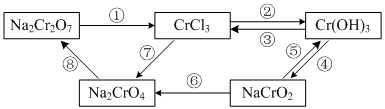
(1)①~⑧所示转化中,需要加入氧化剂才能实现的是_______(填写序号)。
(2)在上述转化中,既能与强酸反应又能与强碱反应的两性物质是______(填化学式)。
(3)转化①可通过下列反应实现:
①完成并配平的化学方程式:
__Na2Cr2O7+__KI+__H2SO4——__Cr2(SO4)3+__Na2SO4+__K2SO4+__I2+__H2O
②用单线桥表示电子转移的方向和数目
③反应中每转移0.4mol电子,生成I2的物质的量为______mol。
Cl2、Br2、I2都具有氧化性,其氧化性Cl2>Br2>I2,Cl2能把溴从溴化物中置换出来,其余类推。
(1)实验室用MnO2制备Cl2的反应中氧化剂是 ,氧化产物是 。将17.4g MnO2与足量的浓盐酸反应,则被氧化的HCl的物质的量为 。
(2)将溴水滴入KI溶液中的化学方程式为 。
(1)已知:2Fe3++2I-===2Fe2++I2, 2Fe2++Br2===2Fe3++2Br-。
①根据以上方程式比较Fe2+、Br-、I-还原性的强弱
②含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是________
(2)在硫酸铝、硫酸钾和明矾的1 L混合溶液中,如果SO42-浓度为0.4 mol/L,当加入等体积0.4 mol/L KOH溶液时,生成的沉淀恰好完全溶解,反应后混合溶液中K+的浓度为_______mol/L
(1)2015年8月12日天津港危化品爆炸,教训极为深刻。其中化学品之一是氰化钠(NaCN):白色固体,可溶于水,剧毒,致死量50~250mg。氰化钠遇水或酸生成剧毒易燃的氰化氢(HCN)气体。处理氰化物可用碱性氯化法,该方法发生三步反应,写出其离子方程式。
①氯气与氢氧化钠溶液反应生成次氯酸盐(ClO-): 。
②次氯酸盐氧化氰化物(CN-)生成氰酸盐(CNO-):ClO-+CN-=CNO-+2Cl-
③过量的次氯酸盐氧化氰酸盐生成CO32-和N2: 。
(2) 用ClO2处理泄漏的氰化钠(NaCN),得到无毒的NaCl、N2和CO2。若处理含NaCN 4×10-5mol·L-1的废水 1000L,至少需要ClO2的质量为___________g。
(3)化学是一门以实验为基础的科学,下列叙述正确的是______(填写序号).
①将0.2mol•L-1FeCl3溶液滴加到沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体.
②分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出。
③用NaOH固体配制100g 10%的氢氧化钠溶液时,用到的玻璃仪器主要有玻璃棒、烧杯、量筒和胶头滴管。
④托盘天平、容量瓶、量筒、滴定管等定量仪器均标有0刻度线。
⑤除去CO2中HCl,可将混合气体通过盛有饱和Na2CO3溶液的洗气瓶。
⑥纯净的氢气在氯气中安静地燃烧,产生苍白色火焰,瓶口伴有白雾。
⑦加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有 。
。
(4)化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是
| A.定性检验SO32-,可用HNO3酸化的BaCl2溶液 |
| B.配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度 |
| C.检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液 |
| D.检验氧化铁中的氧化亚铁,先用硫酸溶液溶解,然后加入盐酸酸化的高锰酸钾溶液 |
用KMnO4氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl 2+5Cl 2↑+8H2O
(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为 。
(2)用双线桥法表示电子的转移情况 。
(3)此反应中氧化剂与还原剂的物质的量的比为 。
(4)15.8g KMnO4完全反应,产生标准状况下Cl2的体积为 ,反应中转移电子的数目为 。(用NA表示阿伏加德罗常数的值)
氧化还原反应在生产、生活中具有广泛的用途、贯穿古今。

(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。试写出有水参加的符合反应类型Ⅳ的一个化学方程式: ,其中水为__ _剂。
(2)过氧化氢的水溶液俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
①下列反应中,H2O2既体现氧化性又体现还原性的反应是( )
| A.Na2O2+2HCl ═ 2NaCl+H2O2 |
| B.Ag2O+H2O2 ═ 2Ag+O2↑+H2O |
| C.2H2O2 ═ 2H2O+O2↑ |
| D.3H2O2+Cr2(SO4)3+10KOH ═K2CrO4+3K2SO4+8H2O |
②保存过氧化氢的试剂瓶上最适合贴上的一个标签是( )(填序号)

(3)焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:
4CuO+2NH4Cl △ 3Cu+CuCl2+N2↑+4H2O
①用双线桥标明电子转移的方向和数目。
。
②该反应中,被氧化的元素是 ,氧化剂是 。
③还原剂与氧化产物的物质的量之比为 。
④反应中若产生0.2 mol的氮气,则有 mol的电子转移。
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且 的值与温度高低有关.当n(KOH)="a" mol时,
的值与温度高低有关.当n(KOH)="a" mol时,
(1)标准状况下,参加反应的氯气的体积等于 L
(2)若某温度下,反应后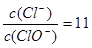 ,则溶液中
,则溶液中 = ,此时反应总离子方程式为 .
= ,此时反应总离子方程式为 .
(3)改变温度,产物中KClO3的最大理论产量为 mol.
在一定条件下,Fe2O3 + 3CO 2Fe + 3CO2反应中, (填名称)是氧化剂, (填化学式)发生氧化反应, (填元素符号)元素被氧化,生成42g Fe时转移的电子的物质的量是 mol .
2Fe + 3CO2反应中, (填名称)是氧化剂, (填化学式)发生氧化反应, (填元素符号)元素被氧化,生成42g Fe时转移的电子的物质的量是 mol .
难溶于水的二硫化亚铁(FeS2)是黄铁矿的主要成分,它溶于稀硝酸的反应为:FeS2 +4HNO3="Fe(NO3)3+2S" + NO↑+2H2O
(1)将反应改写成离子反应方程式_________________________。
(2)用标出电子转移方向和数目:
FeS2 +4HNO3="Fe(NO3)3+2S" +NO↑+2H2O
(3)反应中氧化剂是_______;还原剂是_______。
(4)当反应中转移0.3mol电子,被还原的硝酸的物质的量为_______;可产生标态下NO气体的体积是_______L。
(每空2分,共6分)储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为: C+
C+ K2Cr2O7+
K2Cr2O7+ H2SO4→
H2SO4→ CO2↑+
CO2↑+ K2SO4+
K2SO4+ Cr2(SO4)3+
Cr2(SO4)3+ H2O
H2O
(1)完成并配平上述反应的化学方程式并标出电子转移方向与数目(单线桥法);
___
(2)此反应的氧化产物是__ __;
(3)上述反应中若产生0.1 mol CO2气体,则转移电子的物质的量是__0.4__ mol。
按要求回答下列问题。
(1)把2.3 g钠溶于73.8 g水后所得溶液中Na+与H2O分子的个数比是 。
(2)在甲、乙、丙、丁四个烧杯内分别放入0.1 mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100 mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁中溶液的质量分数由小到大的顺序是 。(填甲、乙、丙、丁,中间以<或=连接)
(3)将钠、镁、铝各0.4 mol分别放入100 mL 1mol/L的盐酸中,同温同压下产生的气体体积比为 。
(4)将物质的量之比为2:3:4的N2、O2、CO2混合气体通过Na2O2后,气体体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为 。
(5)从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4 + 5FeS2 + 12H2O ="=" 7Cu2S + 5FeSO4 + 12H2SO4。(已知FeS2中Fe显+2价),还原剂是 (填化学式),Cu2S是 (选填“还原剂、氧化剂、还原产物、氧化产物或非氧化还原产物”),当有5 mol FeS2发生反应时,有 mol电子转移;1.4 mol硫酸铜可以氧化 mol的硫。
葡萄酒常用Na2S2O5做抗氧化剂。
(1)1.90g Na2S2O5最多能还原 mLO2(标准状况)。
(2)0.5mol Na2S2O5溶解于水配成1L溶液,该溶液pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。
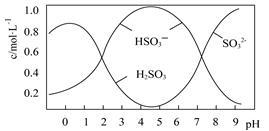
写出Na2S2O5溶解于水的化学方程式 ;当溶液pH小于1后,溶液中H2SO3的浓度变小,其原因可能是 。
已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液pH调为10,向溶液中滴加BaCl2使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤ mol·L-1。
(3)葡萄酒样品中抗氧化剂的残留量测定(已知:SO2+I2+2H2O=H2SO4+2HI):准确量取100.00mL葡萄酒样品,加酸蒸馏出抗氧化剂成分。取馏分于锥形瓶中,滴加少量淀粉溶液,用物质的量浓度为0.0225mol·L-1标准I2溶液滴定至终点,消耗标准I2溶液16.02mL。重复以上操作,消耗标准I2溶液15.98mL。计算葡萄酒样品中抗氧化剂的残留量 (单位:mg·L-1,以SO2计算,请给出计算过程。)
某一反应体系有反应物和生成物共五种物质:
O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是 → 。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目 。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
(5)已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:
H2O2→H2O IO3-→I2 MnO4-→Mn2+ HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
| A.H2O2 | B.IO3- | C.MnO4- | D.HNO2 |