工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。在该反应中
| A.硫元素既被氧化又被还原 |
| B.氧化剂与还原剂的物质的量之比为1:2 |
| C.每生成1molNa2S2O3,转移4mol电子 |
| D.相同条件下,每吸收10m3SO2就会放2.5m3CO2 |
24 mL浓度为0.05 mol·L-1的Na2SO3溶液,恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液完全反应,则元素Cr在被还原的产物中的化合价是
| A.+6 | B.+3 | C.+2 | D.0 |
一定条件下硝酸铵受热分解的未配平化学方程式为:NH4NO3——HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为
| A.5∶3 | B.5∶4 |
| C.1∶1 | D.3∶5 |
如图所示,6个编号分别代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应(已知高温下氨能还原氧化铁):a. Al; b.Fe2O3; c.NaOH溶液; d. HI溶液;e.NH3;f.Cl2 。图中⑤表示的物质是( )

| A.a或b | B.c | C.d | D.e或f |
根据碘与氢气反应的热化学方程式,下列判断正确的是
① I2(g)+ H2(g)  2HI(g) △H=-9.48 kJ/mol
2HI(g) △H=-9.48 kJ/mol
② I2(s)+ H2(g)  2HI(g) △H="+26.48" kJ/mol
2HI(g) △H="+26.48" kJ/mol
| A.254g I2(g)中通入2g H2(g),反应放热9.48 kJ |
| B.当反应②吸收52.96kJ热量时转移2mole一 |
| C.反应②的反应物总能量比反应①的反应物总能量低 |
| D.1 mol固态碘与1 mol气态碘所含能量相差17.00 kJ |
某同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和KCl溶液。下列说法正确的是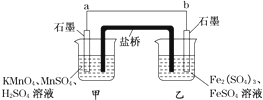
| A.b电极上发生还原反应 |
| B.外电路电子的流向是从a到b |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.a电极上发生的反应为:MnO4-+8H++5e-=Mn2++4H2O |
Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x值是
| A.2 | B.3 | C.4 | D.5 |
在反应KClO3 + 6HCl="=" KCl +3Cl2↑+3H2O中,被氧化与被还原的氯原子个数比为( )
| A.1:6 | B.6:1 | C.1:5 | D.5:1 |
亚硝酸(HNO2)参加反应时,既可作氧化剂,也可作还原剂。当它作还原剂时,可能生成的产物是
| A.NH3 | B.N2 | C.N2O3 | D.HNO3 |
现有等物质的量的铜和银的混合物17.2克,与50.0mL的浓硝酸恰好完全反应,产生气体4.48L(标准状况),则下列说法正确的是
| A.产生的气体是0.2molNO2 |
| B.硝酸的物质的量浓度为12mol/L |
| C.反应中被还原和未被还原的硝酸物质的量之比为3:2 |
| D.要使产生的气体恰好完全被水吸收需要通入氧气0.075mol |
24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
| A.+2价 | B.+3价 | C.+4价 | D.+5价 |
Na2S2O3可作为脱氧剂,已知25.0mL0.100mol·L-1Na2S2O3溶液恰好与224mL(标准状况下)Cl2完全反应,则S2O32—将转化成
| A.S2- | B.S | C.SO32— | D.SO42— |
a mol Cu与含b mol HNO3的溶液恰好完全反应,则被还原的HNO3的物质的量一定是
| A.(b-2a) mol | B.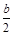 mol mol |
C. mol mol |
D.2a mol |
现有24mL浓度为0.05mol/L的Na2SO3溶液恰好与20mL浓度0.02mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中化合价为( )
| A.+2 | B.+3 | C.+4 | D.+5 |