C1O2 是一种杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+ H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法正确的是
| A.KClO3在反应中得到电子 | B.ClO2被氧化 |
| C.H2C2O4在反应中被还原 | D.1mol KClO3参加反应有2 mol 电子转移 |
1.92 g Cu投入到一定量的浓硝酸中,铜完全溶解,生成的气体的颜色越来越浅,共收集到 672 mL 的气体(标准状况下).将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水,则通入的氧气的体积为多少mL。
| A.168 | B.224 | C.336 | D.504 |
请用单线桥或双线桥表示出以下反应电子的转移情况:
2KMnO4 + 16HCl = 2KCl+ 2MnCl 2+ 5Cl2↑+ 8H2O,
当3.16 g KMnO4与50mL 12 mol·L-1过量浓盐酸完全反应(假设浓盐酸无挥发),通过计算回答:(1)反应中被氧化的HCl的物质的量为 ;转移了 个电子。
(2)产生的Cl2在标准状况下的体积为多少升?
(3)在反应后的溶液中加足量的AgNO3溶液可生成多少克沉淀?
NO2、NH3和O2组成的混合气体,在一定条件下恰好完全反应,生成N2和H2O,则原混合气体中 NO2、NH3和O2的体积比可能是(不考虑NO2与N2O4之间的转化)
| A.2:4:l | B.2:1:2 | C.1:l:1 | D.1:4:3 |
已知镁和稀硝酸反应时,每有1mol HNO3反应,就有0.8 mol电子转移,此时硝酸的还原产物可能是
| A.N2O | B.NO2 | C.N2O4 | D.NO |
一定条件下,等物质的量的下列物质分别与足量的浓盐酸反应,产生Cl2的物质的量最多的是
| A.MnO2 | B.KClO3 | C.KMnO4 | D.Ca(ClO)2 |
0.4mol/L Na2SO3溶液30mL与0.2mol/L K2R2O7溶液Y mL恰好反应,生成SO42-和R3+。Y值为
| A.40 | B.30 | C.20 | D.10 |
磁性氧化铁(Fe3O4)可用于制造录音磁带和电讯器材,其溶于稀硝酸的化学方程式为:
3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O。
(1)Fe3O4晶体的颜色为______________。
(2)Fe(NO3)2在水溶液中的电离方程式为________________________。
(3)上述反应中,氧化剂是_____________(填化学式),被还原的氮元素与未被还原的氮元素的物质的量之比为_________,每生成2.24L(标准状况下)NO时,转移电子的物质的量为____________mol。
向VmLFeBr2溶液中缓慢通入amolCl2,结果溶液中有50%的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为
A.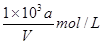 |
B.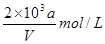 |
C.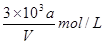 |
D.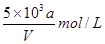 |
一定条件下硝酸铵受热分解的化学反应方程式为:5NH4NO3 = 2HNO3 + 4N2 + 9H2O,在反应中被还原与被氧化的氮原子数之比为
| A.5:3 | B.4:5 | C.5:4 | D.3:5 |
等物质的量的下列化合物与足量浓盐酸反应,得到氯气物质的量最多的是
己知:MnO4-+H++Cl-→Mn2++C12↑+H2O(未配平)
C1O3-+H++Cl-→C12↑+H2O(末配平)
ClO-+H++Cl-→C12↑+H2O(未配平)
| A.KC1O3 | B.KMnO4 | C.MnO2 | D.Ca(C1O)2 |
锌与很稀的硝酸反应生成Zn(NO3)2、NH4NO3和水。当生成1mol硝酸锌时,被还原的硝酸的物质的量为( )
| A.0.25mol | B.0.5mol | C.1mol | D.2mol |
120mL浓度为1 mol//L的Na2SO3溶液,恰好与100mL浓度为0. 4 mol//L的K2Cr2O7溶液完全反应,在还原产物中Cr元素的化合价
| A.+3 | B.+1 | C.+4 | D.+2 |
(1)请把符合要求的化学方程式的编号填在下列空白处:
①既属于分解反应又是氧化还原反应的是________。
②属于化合反应,但不是氧化还原反应的是________。
③既属于化合反应,又是氧化还原反应的是________。
④属于分解反应,但不是氧化还原反应的是________。
⑤不属于四种基本反应类型的氧化还原反应的是________。
| A.2NaHCO3Na2CO3+H2O+CO2↑ |
| B.2Na+Cl22NaCl |
| C.Zn+CuSO4===ZnSO4+Cu |
| D.2KMnO4K2MnO4+MnO2+O2↑ |
E.CaO+CO2CaCO3
F.4FeS2+11O22Fe2O3+8SO2
(2)根据反应Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是________,还原产物是________。
②氧化剂的与氧化产物的物质的量比是________。
③当有9.6g铜参与反应时,在标准状况下,产生气体的体积为________L。