制备粗硅的反应为:SiO2+2C Si+2CO↑,其中氧化剂与还原剂的物质的量之比为
Si+2CO↑,其中氧化剂与还原剂的物质的量之比为
| A.1 : 3 | B.3 : 1 | C.1 : 2 | D.2 : 1 |
已知Fe3O4可表示成(FeO·Fe2O3,),水热法制备Fe3O4纳米颗粒的总反应为:3Fe2+ + 2S2O32- +O2 + 4OH-= Fe3O4 +S4O62- +2H2O,下列说法正确的是
| A.O2和S2O32-是氧化剂,Fe2+是还原剂 |
| B.每生成1mol Fe3O4,则转移电子2 mol |
| C.参加反应的氧化剂与还原剂的物质的量之比为1︰1 |
| D.若有2 mol Fe2+ 被氧化,则被Fe2+ 还原的O2为0.5 mol |
(6分)用足量的NaOH溶液将448mlCl2(标准状况)完全吸收,计算①生成的NaClO的物质的量;②该反应中氧化剂与还原剂的物质的量之比;③该反应中电子转移总数。
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。工业上常通过以下两步反应制备K2FeO4:①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O ② Na2FeO4 + 2KOH=K2FeO4 + 2NaOH
下列说法不正确的是
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中Na2FeO4是还原产物 |
| C.Na2FeO4 中Fe为+6价,具有强氧化性,能杀菌消毒 |
| D.若有2 mol FeCl3发生反应,转移电子的物质的量为 6 mol |
在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol/L和1.5mol/L,现向该溶液中加入39.2g铁粉使其充分反应.下列有关说法正确的是
| A.反应后溶液中Fe3+物质的量为0.8mol |
| B.反应后产生13.44L H2(标准状况) |
| C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol |
| D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体 |
磁性氧化铁(Fe3O4)可用于制造录音磁带和电讯器材,其溶于稀硝酸的化学方程式为:
3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O。
(1)Fe3O4晶体的颜色为______________。
(2)Fe(NO3)2在水溶液中的电离方程式为________________________。
(3)上述反应中,氧化剂是_____________(填化学式),被还原的氮元素与未被还原的氮元素的物质的量之比为_________,每生成2.24L(标准状况下)NO时,转移电子的物质的量为____________mol。
向VmLFeBr2溶液中缓慢通入amolCl2,结果溶液中有50%的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为
A.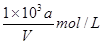 |
B.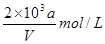 |
C.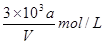 |
D.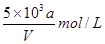 |
一定条件下硝酸铵受热分解的化学反应方程式为:5NH4NO3 = 2HNO3 + 4N2 + 9H2O,在反应中被还原与被氧化的氮原子数之比为
| A.5:3 | B.4:5 | C.5:4 | D.3:5 |
等物质的量的下列化合物与足量浓盐酸反应,得到氯气物质的量最多的是
己知:MnO4-+H++Cl-→Mn2++C12↑+H2O(未配平)
C1O3-+H++Cl-→C12↑+H2O(末配平)
ClO-+H++Cl-→C12↑+H2O(未配平)
| A.KC1O3 | B.KMnO4 | C.MnO2 | D.Ca(C1O)2 |
锌与很稀的硝酸反应生成Zn(NO3)2、NH4NO3和水。当生成1mol硝酸锌时,被还原的硝酸的物质的量为( )
| A.0.25mol | B.0.5mol | C.1mol | D.2mol |
120mL浓度为1 mol//L的Na2SO3溶液,恰好与100mL浓度为0. 4 mol//L的K2Cr2O7溶液完全反应,在还原产物中Cr元素的化合价
| A.+3 | B.+1 | C.+4 | D.+2 |
(1)请把符合要求的化学方程式的编号填在下列空白处:
①既属于分解反应又是氧化还原反应的是________。
②属于化合反应,但不是氧化还原反应的是________。
③既属于化合反应,又是氧化还原反应的是________。
④属于分解反应,但不是氧化还原反应的是________。
⑤不属于四种基本反应类型的氧化还原反应的是________。
| A.2NaHCO3Na2CO3+H2O+CO2↑ |
| B.2Na+Cl22NaCl |
| C.Zn+CuSO4===ZnSO4+Cu |
| D.2KMnO4K2MnO4+MnO2+O2↑ |
E.CaO+CO2CaCO3
F.4FeS2+11O22Fe2O3+8SO2
(2)根据反应Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是________,还原产物是________。
②氧化剂的与氧化产物的物质的量比是________。
③当有9.6g铜参与反应时,在标准状况下,产生气体的体积为________L。
24mL浓度为0.05mol・L-1的Na2SO3溶液,恰好与20mL浓度为0.02mol・L-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
| A.+2 | B.+3 | C.+4 | D.+5 |
将一定量的锌与100 mL 18.5 mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol/L,则下列叙述中错误的是( )
| A.反应中消耗的Zn的质量为97.5 g |
| B.气体A中SO2和H2的体积比为1∶4 |
| C.反应中被还原的元素只有一种 |
| D.反应中共转移电子3 mol |