(1)写出氯原子的原子结构示意图 ,NH4Cl的电子式 ;
(2)用电子式表示H2O的形成过程 ;
(3)已知一定条件下,白磷转化为红磷释放出能量,则等质量的白磷比红磷具有的能量 (填“高”、“低”),故白磷比红磷稳定性 (填“强”、“弱”),等质量的白磷和红磷充分燃烧均生成五氧化二磷, 放出热量多。
下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
|
|
|
① |
② |
③ |
|
|
| 3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
| 4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)在这些元素中,化学性质最不活泼的是_____(填具体元素符号,下同),原子结构示意图为_______。元素⑩名称为________在周期表中的位置________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是________,碱性最强的化合物的电子式是________。
(3)用电子式表示元素④与⑥的化合物的形成过程:________________,该化合物属于________(填“共价”或“离子”)化合物。
(4)表示①与⑦的化合物的电子式________,该化合物是由________(填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是______________。
(6)④和③形成含有非极性共价键的离子化合物的电子式____________。
(7)元素②的氢化物的结构式为________;该氢化物常温下和元素②的最高价氧化物对应水化物反应的化学方程式为______________。
Ⅰ.在①CaCl2、②KOH、③CO2、④NaHSO4、⑤Na2O2、⑥Na2S、⑦N2中,只含有离子键的是________________,只含有共价键的是________________,含有非极性共价键的是__________________,既含有离子键又含有共价键的是____________,属于共价化合物的是____________。
Ⅱ.将NaHSO4溶于水,破坏的化学键是_______________,写出其电离方程式_____________________;NaHSO4在熔融状态下电离,破坏的化学键是_____________,写出其电离方程式____________________。
有X、Y、Z三种短周期元素,分别位于不同的周期。已知X和Y原子最外层电子数相同,Z原子次外层只有2个电子,X和Z可以形成离子化合物X2Z,Y和Z可以形成共价化合物Y2Z
(1)写出X、Y、Z三种元素的元素符号:X是 ,Y是 ,Z是 ;
(2)X2Z的电子式 ,Y2Z的电子式 ;
(3)X2Z和 Y2Z反应的化学方程式 。
X、Y、Z、W、M、Q为原子序数依次增大的六种短周期元素,常温下,六种元素的常见单质中三种为气体,三种为固体。X与M,W与Q分别同主族, X是原子半径最小的元素,且X能与Y、Z、W分别形成电子数相等的三种分子,W是地壳中含量最多的元素。试回答下列问题:
(1)W、M、Q四种元素的原子半径由大到小的排列顺序是 > > (用元素符号表示)。
(2)元素M和Q可以形成化合物M2Q,写出M2Q的电子式 。
(3)Z、W、Q三种元素的简单气态氢化物中稳定性最强的是 (用分子式表示)。
(4)W的一种氢化物含18个电子,该氢化物与QW2化合时生成一种强酸,其化学方程式为
Z、W、Q四种元素组成的阴阳离子个数比为1:1的化合物A,已知A既能与盐酸反应生成气体,又能与氢氧化钠的浓溶液反应生成气体,且能使氯水褪色,写出A与足量氢氧化钠溶液在加热条件下反应的离子方程式 。
X、Y、Z、W是原子序数依次增大的短周期元素,X元素的族序数是周期序数的2倍;Y的单质在空气中燃烧生成一种淡黄色的固体;Z元素最高化合价与最低化合价绝对值之差等于4;W元素在周期表中位于非金属性最强的元素下方。请回答:
(1)X元素在周期表中的位置是 ;W-离子的结构示意图为 。
(2)X元素可形成多种气态氢化物,其中相对分子质量为26的气态氢化物的电子式为 ;25℃、101kPa时该气态氢化物热值为5×104 kJ•kg-1,则其标准燃烧热为 。
(3)写出一种适宜实验室制取W单质的离子方程式: 。
(4)室温时金可溶于王水(浓盐酸和浓硝酸混合物)生成HAuCl4,若反应过程中消耗的氧化剂与还原剂物质的量相等,则该化学方程式为 。
(15)H、C、N、O、Na、Cr是常见的六种元素。
(1)C位于元素周期表第____周期第___族;Cr的基态原子核外电子排布式为___________;C2H2分子中σ键与π键数目之比为____________。
(2)用“>”或“<”填空:
| 电负性 |
键长 |
键的极性 |
沸点(同压) |
| C_____N |
C=C_____C-C |
N-H____O-H |
甲醇____丁烷 |
(3)25℃、101kPa下:①2Na(s)+1/2O2(g)=Na2O(s) ΔH=-414kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ·mol-1
写出Na2O2与单质钠化合成Na2O固体的热化学方程式_________________________。
(4)我国已经立法规定酒驾入列。“酒精检测仪”中有红色CrO3和少量H2SO4,检测酒驾时产物有三价铬和CO2等,该反应的化学方程式为______________________________________。
【化学——物质结构与性质】氢、碳、氮都是重要的非金属元素,它们单质及其化合物在科学研究和工业生产中有重要的应用。
(1)下列微粒基态的电子排布中未成对电子数最多的是_______(填序号)
a.Fe
b.Mn
c.Cu
d.Cr
e.C
(2)含氮配合物W的结构如图所示(配位键未标出方向),请在结构图中用“→”标出W中所存在的所有配位键的方向。
(3)C、H元素形成的某有机化合物分子中共有16个电子,该分子中 键与
键与 键的个数比为_______;该有机化合物在一定条件下形成的聚合物中C原子采取_______杂化。
键的个数比为_______;该有机化合物在一定条件下形成的聚合物中C原子采取_______杂化。
(4)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为_______。该化合物的相对分子质量为M,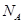 为阿伏加德罗常数。若该晶胞的边长为a pm,则该晶体的密度是_______g.pm
为阿伏加德罗常数。若该晶胞的边长为a pm,则该晶体的密度是_______g.pm 。
。
H、C、N、Cl、Na、Al是常见的六种元素
(1)H位于元素周期表第________周期第________族;C的基态原子核外有_________对成对电子;Cl原子的价电子表示式________.
(2)用“>”、“=”、“<”填空
| 稳定性 |
得电子能力 |
离子半径 |
电负性 |
| CH4____NH3 |
1H_____2H |
Na+_____Al3+ |
C____Al |
(3)用电子式表示NaCl的形成过程:__________________________________________.
(4)已知在常温常压下:
| 化学键 |
H—H |
H—Cl |
Cl—Cl |
| 键能kJ/mol |
a |
b |
c |
写出H2与Cl2反应的热化学方程式:_________________________________________.
(共10分)用下列:①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤Cl2 ⑥Ar ⑦CO2 等物质填空。 (1—4小题填序号)
(1)由离子键和非极性键构成的是
(2)由极性键和非极性键构成的是
(3)不存在化学键的是
(4)共价化合物有
(5)写出下列物质的电子式:Na2O2
(12分)下列物质:①H2②HF ③H2O2 ④KF ⑤NH4Cl ⑥C2H2⑦N2H4+⑧BF3⑨H2O ⑩N2(填序号)
(1)只含非极性键的是___________________
(2)只含极性键的极性分子是_____________
(3)既有极性键又有非极性键的是_________
(4)只有σ键的是_______________________
(5)既有σ键又有π键的是_______________
(6)含有配位键的是_____________________
(14分)氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。请回答下列问题:
(1)Na3N的电子式是_________________________,该化合物由________键形成。
(2)Na3N与盐酸反应生成________种盐,其电子式分别是
________________________________,________________________________。
(3)Na3N与水的反应属于________(填基本反应类型)反应。
(4)比较Na3N中两种粒子的半径:r(Na+)________ (填“>”“=”“<”) r(N3-)。
(10分)X、Y、Z是三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物。已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多1个电子层。
(1)X离子的结构示意图为________。
(2)Z2X属于________(共价或离子)化合物。
(3)Z2Y2中含有________键和________键,Z2Y2溶于水时发生反应的化学方程式是_______________。
有以下物质:①Ne;②NH4Cl;③KNO3;④NaOH;⑤Cl2;⑥SO2;⑦H2S;⑧Na2O2;⑨MgCl2。请用上述物质的数字序号填空:
(1)只存在离子键的是
(2)既存在离子键又存在极性键的是
(3)不存在化学键的是
(4)属于共价化合物的是
(共4分)(1)写出下列物质的电子式: HClO 。
(2)用电子式表示下列物质的形成过程:CaCl2 。