现有①BaCl2 ②金刚石 ③NH4Cl ④Na2SO4 ⑤干冰 ⑥碘 ⑦二氧化硅晶体七种物质,按下列要求回答(将物质的序号填入下列空格中):
(1)属于原子晶体的化合物是_____________。
(2)固态时属于分子晶体的是____________。
(3)熔化时需要破坏共价键的是___________,熔点最低的是___________。
(4)既含有离子键又含有共价键的是__________。
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;E的单质可做半导体材料;C与E两元素形成的化合物可与A、C、D形成的化合物Y发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M。1molM中含有42mol电子。回答下列问题:
(1)E元素在周期表中的位置 ;化合物M中含有的化学键类型有
(2)比较B、C、E形成的气态氢化物的稳定性由强到弱的顺序是(用化学式表示): ;写出C与A形成的18e-化合物的电子式 ;
(3)用电子式表示A2C的形成过程:
(4)写出题中生成M的化学方程式
下图为周期表中的一部分。已知A、B、C、D均为短周期元素,
A与D原子序数之和为C原子序数的1.5倍。
(1)B元素符号是: _______、D在元素周期表中第_______族。
(2)四种元素中原子半径最大的是(填元素符号)_______,B、C、D三种离子中半径最大的是(填离子符号)_______。
(3)B比C的氢化物的沸点高是因为_____ __;A、D两元素的气态氢化物相互反应的生成物的电子式: ,其中存在_______键、_______(填“极性”或“非极性”)共价键。
(4)写一个离子方程式证明C和D的非金属性相对强弱: 。
(5分)在HF、H2O、NH3、CH4、CO32-、CO2、HI分子中
(1)CO32-的价层电子对的空间构型为
(2)以极性键相结合,具有正四面体结构的非极性分子是 。
(3)以极性键相结合,具有三角锥型结构的极性分子是 。
(4)以极性键相结合,具有V型结构的极性分子是 。
(5)以极性键相结合,而且分子极性最大的是 。
(10分)有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同。请回答下列问题:
(1)B元素在周期表中的位置为 ;
(2)A与氢元素能形成原子物质的量之比为1:1的化合物,其电子式为 ;
(3)向D与E形成的化合物的水溶液中滴入NaOH溶液直至过量,观察到的现象是 ,
最后阶段反应的离子方程式为 ;
(4)B、C、D、E的最高价氧化物的水化物的酸性从强到弱的顺序为(物质用化学式表示)
。
(12分)(1)一定条件下,一定量的氢气和氧气反应生成1mol水蒸气时放出241.8kJ的热量,写出该反应的热化学方程式: 。
(2)下列物质:①干冰 ②水晶 ③氯化镁 ④氩 ⑤氢氧化钡 ⑥碳酸钠 ⑦CCl4
a.熔化时只克服离子键的是 ,熔化时只克服分子间作用力的是 。
b.只含共价键的是 ,既含共价键又含离子键的是 ;
c.写出⑦的结构式 。
有A、B、C、D、E五种元素,它们均为短周期元素。已知A是非金属性最强的元素,且E与A同族;金属B的原子核内质子数比前一周期的同族元素多8,其单质不能从CuSO4溶液中置换出Cu;C元素有三种同位素,Cl、C2、C3,C1的质量数分别为C2、C3的1/2和1/3;D的气态氢化物溶于水后显碱性。
(1)写出B元素的离子结构示意图 ;C2粒子的符号: ;
(2)B、E两种元素形成化合物的电子式:
(3)A、E两种元素形成的氢化物沸点较高的是: (用化学式表示),其原
因是 。
(4)写出D的气态氢化物与其最高价氧化物的水化物反应的离子方程式
(5)写出D的氢化物(过量)与E的单质发生氧化还原反应生成一种单质和一种盐的化学方程式 。
现有①BaCl2 ②金刚石 ③KOH ④H2SO4 ⑤干冰 ⑥碘片 ⑦晶体硅 ⑧金属铜 八种物质,按下列要求回答:(填序号)
(1)熔化时不需要破坏化学键的是________,熔化时需要破坏共价键的是________,
熔点最高的是________,熔点最低的是________。
(2)属于离子化合物的是________,只有离子键的物质是________,晶体以分子间作用力结合的是________。
(3)请写出③的电子式 ,⑤的电子式 。
A、B、C、D、E都为短周期元素,A是所有元素中相对原子质量最小的;B的+2价阳离子和C的-1价阴离子都与氖原子具有相同的电子层排布;D在C的下一周期,可与B形成BD2型离子化合物;E和C为同一周期元素,其最高价氧化物的水化物为强酸。
(1)五种元素的元素符号:A 、B 、C 、D 、E 。
(2)B的原子结构示意图为: ;其在周期表中的位置是第 周期,第 主族。
(3)用电子式表示B与C形成化合物的过程:
X、Y、Z、W为按原子序数由小到大排列的四种短周期的元素。其中Y、W位于同一主族,Z、W位于同一周期;Y所组成的单质和氢化物中分别有一种具有漂白性;Z是同一周期中金属性最强的元素,X的某同位素原子的质子数与中子数相等且应用于核聚变反应。请回答下列问题:
(1)W的元素名称是_____。(2)X2Y2的电子式是_______。
(3)Z2WY3与X2WY4反应的离子方程式是____________ _
(4)如图所示的装置,烧杯中盛放的溶液为X2WY4,接通电流表G后,指针发生偏转,此时,负极材料是:__________正极反应式是_____ ___。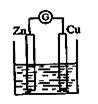
(5)若把铜片放入X2WY4溶液中,溶液无明显的变化,若在X2WY4溶液中加入X2Y2后,观察到铜片附近的溶液变蓝色,请写出反应的化学方程式:____________。
有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出AB2的电子式为___________。
(2)用电子式表示化合物C2D的形成过程___________________________________。
(11分,每空1分)下表是元素周期表的一部分。根据表中的10种元素,用元素符号或化学式填空:
| 族 期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
① |
|
|
|
|
|
|
|
| 2 |
|
|
|
② |
|
③ |
|
|
| 3 |
|
|
④ |
⑤ |
|
⑥ |
⑦ |
⑧ |
| 4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)在①~⑩元素中,金属性最强的金属元素是________。
(2) 在①~⑩元素中,________(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的化学方程式是_______________________。
(3)在①~⑩元素中,形成的最高价氧化物的水化物的酸性最强的酸的分子式是________。
(4)④、⑥、⑦、⑨所形成的单核离子中,半径最大的离子是________。
(5)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。A.MnO2 B.FeCl3 C.Na2SO3 D.KMnO4
(6)用电子式表示元素⑦与元素⑨形成的化合物的形成过程: 。
用电子式表示元素⑥与元素①形成的化合物的形成过程: 。
(7)①与③和①与⑥均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为 。
(8)比较⑩与⑦单质氧化性的强弱的反应的化学方程式是
比较②与⑥单质的非金属性的强弱的反应的化学方程式是
A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B与Z的最外层电子数之比为2︰3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1) X在周期表中的位置是__________________________
(2) 化合物Y2X2的电子式为 ;它含有的化学键类型有 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3) A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为_____________________________________。
(4) A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正负极电极反应式为_________________________。
(5) 写出化合物Y2X2与水反应的离子方程式_____________________。
(6) B的最高价氧化物的结构式为_______________________________。
(7分)用下列:①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤Cl2 ⑥Ar ⑦CO2 等物质填空。(填序号)
(1) 由离子键和非极性键构成的是 (2) 由极性键和非极性键构成的是
(3) 不存在化学键的是 (4) 共价化合物有
(5) 含有极性共价键的离子化合物的是