湖南省衡南县高一下学期期末考试化学试卷
环境污染已成为人类社会面临的重大威胁,各种污染数不胜数。下列名词与环境污染无关的是
①温室效应 ②赤潮 ③酸雨 ④光化学污染 ⑤臭氧层空洞 ⑥水俣病 ⑦潮汐 ⑧大脖子病
| A.①②③ | B.⑦⑧ | C.①⑤⑥ | D.②⑤⑦ |
下列各项中表达正确的是( )
A.F原子结构示意图: |
B.H2O的电子式: |
| C.1H、2H、3H是三种不同元素 | D.乙烯的分子式: C2H4 |
下列各组物质中属于同分异构体的是
| A.正丁烷和异丁烷 | B.金刚石和石墨 | C.12 C和13C | D.乙烯和乙烷 |
下列反应中,属于取代反应的是 ( )
| A.乙醇在一定条件下与氧气反应生成乙醛 | B.苯的硝化反应 |
| C.乙烯在一定条件下生成聚乙烯 | D.乙烯与溴的四氯化碳溶液反应 |
下列关于化学反应的速率和限度的说法不正确的是( )
| A.任何可逆反应都有一定的限度 |
| B.影响化学反应速率的条件有温度、催化剂、浓度等 |
| C.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| D.决定反应速率的主要因素是反应物的性质 |
下列反应既属于氧化还原反应,又是吸热反应的是( )
| A.铝与稀盐酸的反应 | B.灼热的木炭与CO2反应 |
| C.甲烷在氧气中的燃烧反应 | D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
下图是某有机物分子的比例模型,则该物质不具有的性质是 
| A.使紫色石蕊变红 | B.与钠反应 |
| C.发生酯化反应 | D.发生氧化反应 |
在2A+2B C+5D反应中,表示该反应速率最快的是( )
C+5D反应中,表示该反应速率最快的是( )
A.v(A)="0.5" mol/(L·s) B.v(B)="0.3" mol/(L·s)
C.v(C)="0.4" mol/(L·s) D.v(D)="1" mol/(L·s)
有a、b、c、d四种金属,将a与b用导线连结起来浸入稀硫酸溶液中,b不被腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应剧烈;将Cu浸入b的盐溶液里,无明显变化。如果把Cu浸入c的盐溶液里,有c的单质析出。据此判断它们的活动性由强到弱的顺序是( )
| A.d>c>a>b | B.d>b>a>c | C.b>a>d>c | D.d>a>b>c |
绿色化学提倡化工生产应提高原子利用率。原子利用率表示目标产物的质量与生成物总质量之比。在下列制备环氧乙烷(  )的反应中,原子利用率最高的是( ).
)的反应中,原子利用率最高的是( ). 
A、B、C、D、E五种元素原子序数依次增大,且均不超过18。其中A与C、B与E分别为同族元素。原子半径A<B<E<D<C,B原子最外层电子数是内层电子数的3倍,C、D的核外电子数之和与B、E核外电子数之和相等。下列说法正确的是
A.原子最外层电子数:B<A B.A与E形成的化合物是离子化合物
C.最高价氧化物对应的水化物碱性:C<D D.B与E可以形成EB2型化合物
山梨酸是一种常见的食物添加剂,它是一种无色针状晶体或白色粉末,它的结构简式为CH3—CH=CH—CH=CH—COOH。下列关于山梨酸的叙述不正确的是 ( )
| A.山梨酸易溶于乙醇 | B.山梨酸能与氢气发生加成反应 | C.山梨酸能和乙醇反应生成酯 | D.1mol山梨酸能和金属钠反应生成1mol氢气 |
将0.2 mol下列烃完全燃烧后,生成的气体缓缓通过0.5 L 2mol/L的NaOH溶液中,生成正盐和酸式盐的物质的量之比为1:3,则该烷烃是( )
| A.乙烷 | B.丙烷 | C.丁烷 | D.戊烷 |
X、Y为短周期元素,X原子中K、L、M各电子层的电子数之比为1:4:1,Y原子比X原子少3个电子,下列叙述正确的是
| A.X、Y形成化合物表示为X2Y |
| B.X、Y形成的化合物中所含离子都是10电子微粒 |
| C.X原子半径小于Y的原子半径 |
| D.Y位于周期表中第ⅦA族,其最高正化合价为+7 |
在一定温度下,体积固定的密闭容器中进行可逆反应A(g) + 3B(g)  2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是
2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是
A.单位时间内生成n mol A,同时生成3n mol B
B.A、B、C的浓度不再发生变化
C.混合气体的压强不再发生改变
D.C生成的速率与C分解的速率相等
原电池是化学对人类的一项重大贡献。(1)①某兴趣小组为研究原电池原理,设计如图装置。a和b不连接时,烧杯中发生反应的离子方程式是__________。
②a和b用导线连接,Cu极为原电池__________极(填“正”或“负”),电极反应式是__________。Zn极发生__________(填“氧化”或“还原”)反应。溶液中H+移向__________(填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻了__________g。
(2)有同学想把Ba(OH)2•8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?________(填“是”或“否”)。
实验室用下图装置制取乙酸乙酯。
(1)加热前在大试管中加入几粒碎瓷片的作用是 ,
(2)导气管不能插入饱和Na2CO3溶液液面以下是为了 ,
(3)实验室制取乙酸乙酯的化学反应方程式为: 。
(4)饱和Na2CO3溶液的作用是 , , 。
某可逆反应从0—2分钟进行过程中, 在不同反应时 间各物质的量的变化情况如下图所示。则该反应的的反应物是 ,生成物是 ,化学方程式为 ;反应开始至2分钟时,能否用C表示反应速率?若能,其反应速率为 _____ ,若不能,则其原因为 _ ________________ ;2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了 ____ 状态。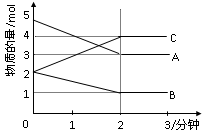
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;E的单质可做半导体材料;C与E两元素形成的化合物可与A、C、D形成的化合物Y发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M。1molM中含有42mol电子。回答下列问题:
(1)E元素在周期表中的位置 ;化合物M中含有的化学键类型有
(2)比较B、C、E形成的气态氢化物的稳定性由强到弱的顺序是(用化学式表示): ;写出C与A形成的18e-化合物的电子式 ;
(3)用电子式表示A2C的形成过程:
(4)写出题中生成M的化学方程式


 粤公网安备 44130202000953号
粤公网安备 44130202000953号