有一包固体粉末,由CaCO3、Na2SO4、KCl、Ba(NO3)2、CuSO4中的三种物质组成,取样品进行如下实验:
(1)写出实验过程中发生反应的离子方程式 。
(2)固体粉末中一定不存在的物质是 ,一定存在的物质是 。
。
(3)将固体粉末可能的组合填入下表:(可以不填满,也 可以再补充)
可以再补充)
| 序号 |
化学式 |
| Ⅰ |
|
| Ⅱ |
|
| Ⅲ |
|
(4)请设计一个实验进一步确定混合物的组成,简述实验步骤、现象和结论。
_________________________________________________________________________。
2011年5月份以来,受到拉尼娜现象和全球大气环流异常共同作用的影响,我国南方出现持续罕见的旱情,为此专家建议尽快发展高能抗旱保水剂用来调控农田水分和作物耗水,减缓水资源短缺和干旱的危害。已知有机物I为一种保水剂,可通过烃A经下列转化生成:
提示: 不能稳定存在。
不能稳定存在。
请回答下列问题:
(1)A和I的结构简式为:A I
(2)F中官能团的名称为:
(3)反应②和⑦的反应类型为:② ⑦
(4)反应④的化学方程式为:
(5)M是一种普遍使用的抗生素类药物,它是由2个F分子在一定条件下脱去2个水分子形成的环状酯,写出该反应的化学方程式:
(6)D有两种能发生银镜反应且属链状化合物的稳定同分异构体,请写出它们的结构简式:
淡黄色固体X和气体A存在如下转化关系:

请回答下列问题:
(1)固体X的名称 A的化学式 。
(2)写出反应①③的化学方程式,并指出氧化剂。
反应① , 。
反应③ , 。
(3)写出②④反应的离子方程式:
反应② 。
反应④ 。
A、B、C、D、E、F、G为常见物质,其中C为淡黄色固体。甲、乙、丙为常见气体。各物质的转化关系如下图所示。
回答下列问题:
(1)C的名称是 ;D的俗称__________;F的化学式 ;
A+甲→C的反应条件是 。
(2)在一定条件下,甲+乙→F,该反应属于 。
①氧化还原反应 ②非氧化还原反应 ③化合反应 ④分解反应
⑤复分解反应 ⑥置换反应 ⑦离子反应
(3)写出下列变化的离子方程式。
①A+F→E+乙: 
 。
。
②D+F+丙→G: 。
有A、B、C、D四种元素,A元素形成的离子中只有一个质子,B原子的最外层电子数是次外层的3倍,C元素的一价阳离子核外有10个电子,D元素的原子得到一个电子后能形成与氩原子电子层结构相同的离子。回答下列列问题:
(1)画出D元素的离子结构示意图__________________;
(2)工业上用电解C和D两元素形成的化合物的水溶液生产D的单质,写出该反应的化学方程式_______________________,电解后的溶液能使酚酞变红的是与电源的________极相连接的区域;
(3)D单质能和A、B、C三元素形成的化合物反应,该反应的化学方程式是________________,当有0.1mol的D单质反应时,电子转移__________个;
(4)B、C、D三元素能形成一种化合物,1mol该化合物中有36mol电子,该化合物的水溶液是一种____剂,它与A、D两元素形成的化合物的水溶液反应时能产生一种有毒气体,该反应的化学方程式是______。
(14分)金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,转化关系如下:
已知,气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。
请回答下列问题:
(1) A和B两溶液混合产生白色沉淀,该白色沉淀的化学式
(2) C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该单质的电子式
(3)完成铝在碱性条件下与NO3-反应的离子方程式 。
(4)过量D的水溶液与A溶液反应的离子方程式是 。
(5)D→C反应的化学方程式是 。
(6)除去气体C中的杂质气体E的化学方法: (用化学方程式表示)
(7)Al与NO3-在酸性条件下反应,Al与被还原的NO3-的物质的量之比是 。
已知:甲、乙、丙为常见单质,甲常温下为固体,乙为黄绿色气体,丙为无色气体。A、B、C、D均为化合物,D为红褐色沉淀,它们之间有下图转化关系。请回答以下问题。
(1)写出下列物质的化学式;乙 ;B 。
(2)写出③反应的化学方程式: 。
(3)写出②反应的离子方程式: 。
A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空:
(1)若A可用于 自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则B的化学式可能是 ;实验室制取A的离子方程式为 。
自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则B的化学式可能是 ;实验室制取A的离子方程式为 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,则反应①的化学方程式为 。
(3)若B有两性,则反应②的离子方程式是 。
(4)若D为空气质量预报必报的气体,A、B、C的的焰色反应都呈黄色,则可以证明B是否变质的一组试剂是 (请写出 试剂名称)。
试剂名称)。
(5)若C是淡黄色固体,D是一种常见气体,则B→ C反应的化学方程式为 ,C的电子式为 。
下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),X分解所得A、B、C混合气体的平均相对分子质量为24,其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。
(1)写出下列各物质的化学式:
X: ;F: ;G: 。
(2)写出下列变化的离子方程式:
F→G: ;
G→E: 。
(3)实验室里,C常采用 法来收集。
A、B、C、X均为中学常见的纯净物,它们之间有如图转化关系(副产物已略去)。
回答下列问题:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若A、B、C为含金属元素的无机化合物,X为强电解质溶液,A溶液与C溶液反应生成B,则B的化学式为________,X的化学式可能为(写出不同类物质)________或________,反应①的离子方程式为________________________或________________________。
工业上制取铝的流程如下: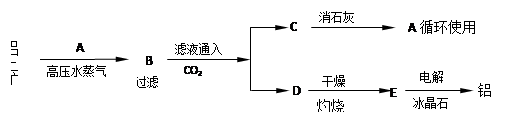
注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A ,B ,C ,D ,E 。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| |
Al2O3 |
Fe2O3 |
Na2O |
| 铝土矿 |
55% |
16% |
0% |
| 赤泥 |
15% |
48% |
8% |
试求制取1t Al2O3所需铝土矿和苛性钠的质量。(写过程)
已知A、B、C、D的组成元素都属于短周期元素,其中A、D为单质,B、C为化合物,它们之间的关系转化如下图所示,请按要求写出有关反应式,是离子反应的只写离子方程式。
(1)若A、D的组成元素同主族:
①B是水
②B、C均为氧化物:
(2)若A、D的组成元素不同主族
①B是水且水是还原剂:
B是水且水是氧化剂
②B、C均为氧化物
由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转换关系,A是地壳中含量最多的金属元素。请回答:
(1)写出下列物质的化学式:乙 、丁 、戊 。
(2)写出甲物质在工业上的一种主要用途: 。
(3)写出甲→乙+丙反应的离子方程式: ;
A→乙+C反应的化学方程式:
已知A、B、C是单质,其中A是金属,各物质间的转化关系如图:
回答下列问题:(1)写出下列物质的化学式(各1分):
(1)A:________、B:________、乙:________、
丙:________、丁:________、戊:________
(2)写出A与NaOH溶液的化学方程式 ;
写出丁生成戊的离子方程式 ;
A、B、C、D、E、F是中学化学中常见的气体,G是一种固体非金属单质,它们具有如下的性质:
①A、B、E能使湿润的蓝色石蕊试纸变红,F能使湿润的红色石蕊试纸变蓝,C、D不能使湿润的石蕊试纸变色。
②A和F相遇产生白烟。
③B和E都能使品红溶液褪色。
④将红热的铜丝放入装有B的集气瓶中,瓶内充满棕黄色的烟。
⑤C和D相遇生成红棕色气体,且D可助燃。
⑥G是常见的半导体材料
回答下列问题:
(1)A的化学式是 ,②中的白烟是 (填化学式)。
(2)④中发生反应的化学方程式是
(3)C的化学式是 ,E的化学式是
(4)写出工业上制G的化学方程式
(5)B是一种有毒气体,实验室可用 吸收B,反应的离子方程式是
写出实验室制取B的化学方程式