下列化学用语正确的是
A.NaHCO3的水解:HCO3-+H2O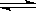 H3O++CO32- H3O++CO32- |
B.醋酸铵的电离:CH3COONH4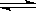 CH3COO-+NH4+ CH3COO-+NH4+ |
| C.H2的燃烧热为285.8kJ/mol:H2(g)+ 1/2O2(g)=H2O(g);△H=-285.8kJ/mol |
D.碳在高温下还原二氧化硅 SiO2+2C Si+2CO↑ Si+2CO↑ |
下列离子方程式中,属于水解反应的是
A.CH3COOH+H2O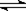 CH3COO-+H3O+ CH3COO-+H3O+ |
B.CO2+H2O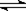 HCO3- +H+ HCO3- +H+ |
C.CO32-+H2O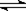 HCO3-+OH- HCO3-+OH- |
D.HS-+H2O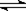 S2-+H3O+ S2-+H3O+ |
下列有关说法正确的是
| A.反应NH3(g)+HCl(g)= NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀 |
| C.CH3COOH溶液加水稀释后,电离平衡正向移动,溶液中的c(CH3COO-)增大 |
| D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
室温下0.1mol/L的NH4CN溶液的pH等于9.32。下列说法错误的是
| A.上述溶液能使甲基橙试剂变黄色,石蕊试液变蓝 |
| B.室温下,HCN是比NH3·H2O更弱的电解质 |
| C.上述溶液中NH4+的水解程度大于CN-的水解程度 |
| D.室温下,0.1mol/LNaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度 |
下列有关说法正确的是
| A.常温下,0.1 mol/L NH4Cl溶液加蒸馏水稀释,溶液的pH不断增大,但无限接近7 |
| B.25 ℃时,溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14 |
| C.pH=6的纯水中,c(OH-)=10-8 mol·L-1 |
| D.稀释0.01 mol·L-1的醋酸溶液时,溶液中所有的离子浓度均减小 |
分别将下列物质:①CuSO4 ②Na2O2 ③NaCl ④Ca(HCO3)2 ⑤FeCl3投入水中,对其溶液加热蒸干,仍能得到原物质的是 ( )
| A.①②③ | B.①③ | C.③④ | D.③ |
下列说法正确的是v( )
| A.盐溶液都是中性的 |
| B.盐溶液的酸碱性与盐的类型无关 |
| C.NaHCO3溶液显酸性 |
| D.碳酸钠溶液显碱性,溶液中c(OH-)>c(H+) |
温度相同,浓度均为0.2 mol·L-1的①(NH4)2SO4,②NaNO3,③NH4HSO4,④NH4NO3,⑤CH3COONa溶液,它们的pH由小到大的排列顺序是
| A.③①④②⑤ | B.①③⑤④② |
| C.③②①⑤④ | D.⑤②④①③ |
下列说法正确的是
| A.酸式盐的水溶液一定显碱性 |
| B.醋酸铵溶液呈中性是因为溶液中H+的物质的量和OH-的物质的量相等 |
| C.NaHSO3溶液的PH大于Na2SO4溶液的PH |
| D.只要酸与碱的物质的量浓度和体积分别相等,它们反应后的溶液就呈中性 |
下列水解的离子方程式正确的是
A.S2﹣+2H2O H2S+2OH﹣ H2S+2OH﹣ |
B.Fe3++3H2O Fe(OH)3+3H+ Fe(OH)3+3H+ |
C.HCO3﹣+H2O CO32﹣+H3O+ CO32﹣+H3O+ |
D.HS﹣+H2O H2S↑+OH﹣ H2S↑+OH﹣ |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为
| A.0.15 mol·L-1 | B.0.2 mol·L-1 |
| C.0.3 mol·L-1 | D.0.4 mol·L-1 |