在pH为4~5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。现欲除去溶液中的杂质离子,下述方法中可行的是 ( )
| A.向溶液中加入纯Cu将Fe2+还原 |
| B.向溶液中通入H2S使Fe2+沉淀 |
| C.向溶液中通入Cl2,再通入CuO粉末调节pH为4~5 |
| D.向溶液中通入Cl2,再通入NH3调节pH为4~5 |
下列说法中正确的是 ( )
| A.等物质的量浓度NaCl和CH3COONa溶液等体积混合, c(Cl-)>c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.25℃时,若10mL盐酸(pHa)与100mLBa(OH)2溶液(pHn)混合后恰好中和,则pHa+pHn=13 |
| C.等物质的量浓度的硫酸与醋酸钠溶液等体积混合,c(SO42-)+c(OH-)=c(H+)+c(CH3COOH) |
D.向氨水中加水稀释, 减小 减小 |
已知25℃时,0.2mol/L某酸HA 与0.1mol/LNaOH等体积混合,溶液pH>7;含等物质的量的盐NaB和酸HB混合液pH<7。该温度下,在物质的量浓度均为0.1mol/L的NaA和NaB混合溶液中,下列排序正确的是 ( )
A.c(Na+)>c(OH-)>c(HB)>c(HA) B.c(Na+)>c(OH-)>c(A-)>c(B-)
C.c(Na+)>c(OH-)>c(HA)>c(HB) D.c(OH-)>c(Na+)>c(B-)>c(A-)
下列叙述中,正确的是
| A.0.1 mol•L-1 CH3COOH溶液加水稀释时,所有离子的浓度都减小 |
B.NH4Cl溶液显酸性的原因:NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |
| C.0.2 mol•L-1盐酸与等体积0.05 mol•L-1 Ba(OH)2溶液混合后,溶液pH为1 |
| D.25℃时pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
已知HCN的电离常数K=6.2×10-10。用物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,经测定溶液呈碱性。则下列关系式正确的是
| A.c(CN-)>c(Na+) | B.c(CN-)<c(HCN) |
| C.c(HCN)+ c(CN-)=0.2mol·L-1 | D.c(CN-)+ c(OH-)=0.1mol·L-1 |
用酒精灯加热下列溶液,蒸干后灼烧,所得固体质量最大的是
| A.20mL 2mol/L FeCl3溶液 |
| B.40mL 1mol/L NaHCO3溶液 |
| C.20mL 1mol/L Na2SO3溶液 |
| D.40mL 2mol/L NH4HCO3溶液 |
用酒精灯加热蒸干下列物质的溶液然后灼烧,可以得到该物质固体的是
| A.AlCl3 | B.Na2CO3 | C.Na2SO3 | D.KMnO4 |
下列溶液中各微粒的浓度关系正确的是
A.0.2 mol/L的CH3COOH溶液与0.1 mol/L CH3COOH溶液中c(H+)之比为2:1
B.0.1 mol/L NaHCO3溶液中,c(Na+) = 2c(CO32—) + c(HCO3—) + c(H2CO3)
C.0.1 mol/L 的NaHA溶液,其pH = 4,则c(HA—)>c(A2—)>c(H2A)
D.只含Na+、CH3COO—、H+、OH—的酸性溶液中,c(H+)>c(CH3COO—)>c(Na+)>c(OH—)
根据下表信息,判断0.10mol/L的下列各溶液pH值最大的是
|
|
某溶液中含有NH4+、H+、SO42-和OH-,对该溶液的描述一定正确的是 ( )
| A.该溶液可能呈酸性,也可能呈碱性或中性 |
| B.只能是硫酸铵和硫酸的混合溶液 |
| C.离子浓度由大到小的顺序是:c(NH4+)>c(SO42-)>c(H+)>e(OH一) |
| D.离子浓度存在下列关系:c(NH4+)+c(H+)=c(OH一)+c(SO42-) |
工业上用重晶石(BaSO4)制备BaCO3的常用方法主要有高温煅烧还原法、沉淀转化法等。高温煅烧还原法的工艺流程可简单的表示如下:
已知:BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H="+571.2" kJ•mol-1
Ba(s)+S(s)+2O2(g):BaSO4(s)△H=—1473.2 kJ•mol-1
Ba(s)+S(s)=BaS(g)△H=—460 kJ•mol-1
请回答:
(1)工业上煅烧重晶石矿粉时,为使BaSO4得到充分还原和维持反应所需的高温,应采取的措施是 。
(2)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:
BaSO4(s)+CO2-3(aq)=BaCO3(s)+SO2-4(aq)
则:在实验室中将少量BaSO4沉淀全部转化为BaCO3的实验操作方法与步骤为
(3)与高温煅烧还原法相比,用饱和Na2CO3溶液沉淀转化法的优点主要有
向1.00 L 0.3mol·L-1NaOH溶液中缓慢通入CO2气体至溶液增重8.8g。有关该溶液说法正确的是 ( )
| A.溶质为Na2CO3 |
B.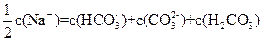 |
C. |
D.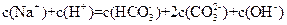 |
某混合溶液中所含离子的浓度如下表,则Mn+离子及a值可能为 ( )
| 所含离子 |
NO-3 |
SO2-4 |
H+ |
Na+ |
Mn+ |
| 浓度(mol·L-1) |
3 |
1 |
2 |
1 |
a |
| A.Mg2+、1 | B.Ba2+、0.5 | C.Al3+、1.5 | D.Fe2+、2 |
在一定条件下,Na2CO3溶液存在水平平衡:CO2-3+H2O  HCO-3+OH-。下列说法正确的是 ( )
HCO-3+OH-。下列说法正确的是 ( )
| A.稀释溶液,上述可逆反应平衡常数不变 |
| B.通入CO2,溶液pH增大 |
| C.加入NaOH固体,平衡向正反应方向移动 |
D.升高温度, 不变 不变 |