(8分)硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:
H2SO4=H++HSO4—, HSO4  H++SO42—。
H++SO42—。
请回答下列有关问题:
(1)Na2SO4溶液呈 填“弱酸性”、“中性”或“弱酸性”);
(2)H2SO4溶液与BaCl2溶液反应的离子方程式为 ;
(3)在0.10mol·L—1的Na2SO4溶液中,下列离子浓度关系正确的是 (填写编号)
| A.c(Na+)=c(SO42—)+c(HSO4—)+c(H2SO4) |
| B.c(OH—)=c(HSO4—)+c(H+) |
| C.c(Na+)+c(H+)=c(OH—)+c(HSO4—)+2c(SO42—) |
| D.c(Na+)="2" c(SO42—)+2 c(HSO4—) |
(4)写出NaHSO4溶液中溶质电离常数(Ka)的表达式 ;
常温下有浓度均为0.5mol/L的四种溶液:①Na2CO3②NaHCO3③HCl ④NH3?H2O(1)上述溶液中,可发生水解的是 (填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度大到小的
顺序为 。
(3)向溶液④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值 (填增大、
减小、不变)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填
大于、小于、等于)。
(5)取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出的c(H+)= 。
在温度T下,c(OH-)=0.1 mol·L-1的Ba(OH)2的PH值为11。
(1)该温度下,100ml水中含有OH-约有_ 个。
(2)该温度下,在PH=8的Ba(OH)2溶液中加入PH=5的盐酸,欲使混合溶液pH=7,则Ba(OH)2溶液与所加盐酸的体积比为__ __
若有等体积的a:PH=1的盐酸,b:PH=1的硫酸,c:物质的量浓度为0.1 mol·L-1的醋酸(均用物质序号回答下列问题):
①欲均加水稀释到相同PH值,所加水的体积关系是: 。
②分别加入足量的锌粉,产生氢气体积(相同温度和压强)大小关系是
③某学生用蒸馏水润湿的PH试纸测定PH值,误差最小的是
(Ⅰ)
现有下列物质: ①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡 ⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KCl ⑧NaOH溶液
请用以上物质回答下列问题。(填序号)
(1)在上述状态下能导电的物质是 ;
(2)属于弱电解质的是 ;
(3)属于非电解质,但溶于水后的水溶液能导电的是 ;
(Ⅱ)现有下列电解质溶液:①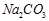 ②
②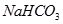 ③
③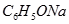 ④
④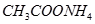 ⑤
⑤ (已知酸性
(已知酸性 。)
。)
(1)在这五种电解质溶液中,既能与盐酸又能与烧碱溶液反应的是(填写序号) 。
(2)常温下,物质的量浓度相同的①、②、③溶液pH大小顺序为(填序号) > > 。
(3)写出⑤与足量NaOH溶液混合加热时反应的离子方程式 。
常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
(1)由图中信息可知HA为________酸(填“强”或“弱”),理由是____________
(2)常温下一定浓度的MA稀溶液的pH=a,则a________7(填“>”、“<”或“=”),用离子方程式表示其原因为__________________________;,此时,溶液中由水电离出的c(OH-)=________。
(3)请写出K点所对应的溶液中离子浓度的大小关系:__________
(4)K点对应的溶液中,c(M+)+c(MOH)________2c(A-)(填“>”、“<”或“=”);若此时溶液中,pH=10,则c(MOH)+c(OH-)=________mol·L-1。
设水的电离平衡曲线如图所示:
⑴若以A点表示水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 .
⑵将pH=8的Ba(OH)2溶液与PH=5的稀盐酸相混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2与盐酸的体积比为
在a.b两支试管中,分别装上质量相等形状相同的一颗锌粒,然后向两支试管中:
(1)分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。则
a.b两支试管中的现象:相同点是 ;不同点是
反应完毕后生成气体的总体积是a b。
(2)分别加入相同PH、相同体积的稀盐酸和稀醋酸时,两支试管中的反应速率在反应刚开始时是a b(填“大于”、“等于”或“小于”下同),当两种酸都反应完毕后生成气体的体积是a b
写出下列几种溶液的pH或pH的范围
(1)0.05mol/LH2SO4溶液 ;(2)0.01mol/LNaOH溶液
(3)pH=12NaOH溶液加水稀释100倍 ;
(4))pH=5HCl溶液加水稀释1000倍 。
(12分)在温度T ℃下,某Ba(OH)2稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 |
氢氧化钡的体积/mL |
盐酸的体积/mL |
溶液的pH |
| ① |
22.00 |
0.00 |
8 |
| ② |
22.00 |
18.00 |
7 |
| ③ |
22.00 |
22.00 |
6 |
(1)依据题意判断,T ℃________25 ℃(填“大于”、“小于”或“等于”),该温度下水的离子积KW=________。
(2)b=________,原Ba(OH)2稀溶液的物质的量浓度为________。
(3)该温度下,向1 L硫酸与硫酸钠的混合溶液中加入3 L该Ba(OH)2的稀溶液时,沉淀正好达最大值,从所得溶液中取出4 mL并加水稀释至20 mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为________,其中Na2SO4的物质的量浓度为________。
有A、B、C、D四种强电解质,它们在水中电离可产生表中离子(每种物质只含一种阴离子且互不重复)。
| 阳离子 |
Na+、Ba2+、NH4+ |
| 阴离子 |
CO32-、Cl-、OH-、SO42- |
已知:
①A、C溶液的pH均大于7,A、B的溶液中水的电离程度比纯水大,A、D焰色反应的火焰均为黄色;
②C溶液和D溶液相遇时只观察到有白色沉淀产生,B溶液和C溶液相遇时只观察到有刺激性气味的气体产生,A溶液和D溶液混合时无明显现象。
请填写下列空白:
(1)A是___________,B是___________,C是____________,D是___________。
(2)常温,将1 mL pH =12的C溶液加水稀释至100mL,所得溶液中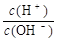 = 。
= 。
(3)常温下,0.15 mol·L-1的C溶液与0.20 mol·L-1盐酸混合,所得混合液的pH=13,则C溶液与盐酸的体积比= _______________。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是 。
某同学用0.1082mol/L 的NaOH溶液滴定未知浓度的盐酸,以下是实验数据记录表。
| 实验序号 |
待测盐酸溶液的体积mL |
滴定管读数 |
消耗标准NaOH溶液的体积mL |
|
| 初读数 |
末读数 |
|||
| 1 |
20.00 |
0.00 |
19.90 |
19.90 |
| 2 |
20.00 |
0.05 |
|
|
列出求算待测盐酸溶液浓度的计算式(须含上表相关数据,不必计算结果)
某同学用0.1082mol/L 的NaOH溶液滴定未知浓度的盐酸,以下是实验数据记录表。
| 实验序号 |
待测盐酸溶液的体积mL |
滴定管读数 |
消耗标准NaOH溶液的体积mL |
|
| 初读数 |
末读数 |
|||
| 1 |
20.00 |
0.00 |
19.90 |
19.90 |
| 2 |
20.00 |
0.05 |
|
|
请根据右图(滴定管的局部)读出第2次实验的末读数,
填充上表中的两个空格。
CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。
根据题意完成下列填空:
(1)理论上,为了制得纯净的CuSO4·5H2O晶体,需要消耗稀硫酸、稀硝酸溶质物质的量之比为 ,发生反应的离子方程式为 。
(2)实际制得的胆矾晶体中还是含有一些杂质,通常采用 法提纯。
(3)实际生产过程中对所加稀硝酸的浓度控制要求比较高,通常用标准氢氧化钠溶液来滴定。滴定过程中若用酚酞作指示剂,终点现象是  。请在右图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。
。请在右图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。
(4)上述使用的标准氢氧化钠溶液已经通过基准物质的标定。下列物质中通常可用来标定碱液的基准物质是 。
| A.醋酸 | B.草酸 | C.苯甲酸 | D.苯酚 |
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.2 |
0.1 |
pH<7 |
请回答:
(1) 从①组情况分析, HA是 酸(选填“强”、“弱”)。
(2) ②组情况表明,c 0.2 (填“>”、“=”或“<”)。
(3) 从③组实验结果分析,说明HA的电离程度______NaA的水解程度(填“>”、“=”或“<”),该混合溶液中离子浓度由大到小的顺序是 。
(4) ①组实验所得混合溶液中由水电离出的c(OH-)= mol·L-1。