(1)H2O2的水溶液为二元弱酸,科学家对H2O2结构的认识经历了较为漫长的过程,最初他们提出了两种观点:
a. (式中O→O表示共用电子对由前一个氧原子提供)和 b.H—O—O—H
(式中O→O表示共用电子对由前一个氧原子提供)和 b.H—O—O—H
①请用电子式表示b的结构 。
②写出H2O2在水溶液中的电离方程式 。
(2)①用单质碘和氯酸钾可以制得碘酸钾,其中涉及的一个反应为:
I2 + KClO3 + H2O → KH(IO3)2 + KCl + Cl2↑.因此有人认为I2的氧化性强于氯气,你
(填“同意”或“不同意”)该观点,理由是 。
②用电化学方法也可以制碘酸钾.原理是以石墨为阳极,不锈钢为阴极,以碘化钾溶液为电解质溶液,在一定电流和温度下进行电解(同时不断搅拌电解质溶液)其电解总反应式为:

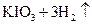 试写出阳极的电极反应式 。
试写出阳极的电极反应式 。
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是 ( )
I2+SO2+2H2O==H2SO4+2HI 2FeCl2+Cl2==2FeCl3 2FeCl3+2HI==2FeCl2+2HCl+I2
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |
下列五个反应中氧化剂氧化能力由强到弱的顺序为( )
①2Fe+3Cl
 2FeCl
2FeCl
②Fe+2HCl FeCl
FeCl +H
+H ↑
↑
③2KMnO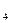 +16HCl(浓)
+16HCl(浓) 2KCl+2MnCl
2KCl+2MnCl +5Cl
+5Cl ↑+8H
↑+8H O
O
④MnO +4HCl(浓)
+4HCl(浓) MnCl
MnCl +Cl
+Cl ↑+2H
↑+2H O
O
⑤O +4HCl(浓)
+4HCl(浓) 2Cl
2Cl ↑+2H
↑+2H O
O
A.Cl >MnO >MnO >O >O >KMnO >KMnO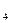 >HCl >HCl |
B.KMnO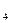 >MnO >MnO >O >O >Cl >Cl >HCl >HCl |
C.KMnO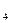 >O >O >MnO >MnO >Cl >Cl >HCl >HCl |
D.KMnO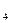 >O >O >Cl >Cl >MnO >MnO >HCl >HCl |
反应5KCl+KClO +3H
+3H SO
SO
 3Cl
3Cl ↑+3K
↑+3K SO
SO +3H
+3H O氧化生成和还原生成的氯分子数之比是( )
O氧化生成和还原生成的氯分子数之比是( )
A1∶1 B5∶1 C1∶5 D3∶1
多种氧化剂和多种还原剂共存时,存在“争先恐后,强者优先”现象。请理论预测,在含有Cu(NO )
) 、Mg(NO
、Mg(NO )
) 和AgNO
和AgNO 的溶液中加入适量锌粉,首先置换出来的是( )
的溶液中加入适量锌粉,首先置换出来的是( )
| A.Mg | B.Cu | C.Ag | D.H |
有A、B、C、D四种物质,已知它们能发生下列变化:①A2++B===B2++A、②A2++C===C2++A、③B2++C===C2++B、④C2++D===D2++C。由此可推知,各物质的氧化性、还原性强弱顺序正确的是
A.氧化性:A2+>B2+>C2+>D2+
B.氧化性:D2+>B2+>C2+>A2+
C.还原性:A>C>B>D
D.还原性:A>B>C>D
已知X2、Y2、Z2、W2四种物质的氧化能力为W2>Z2>X2>Y2,下列氧化还原反应能发生的是
| A.2NaW+Z2===2NaZ+W2 | B.2NaX+Y2===2NaY+X2 |
| C.2NaY+W2===2NaW+Y2 | D.2NaZ+X2===2NaX+Z2 |
下列反应都有沉淀生成,其中属于氧化还原反应的是( )
| A.Na2SO4+BaCl2===2NaCl+BaSO4↓ | B.4Fe(OH)2+O2+2H2O="=" 4Fe(OH)3↓ |
| C.FeCl3+3KOH===Fe(OH)3↓+3KCl | D.CuCl2+2NaOH===Cu(OH)2↓+2NaCl |
①A+B2+ =A2++B , ②D +2H2O=D(OH)2 + H2↑,③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-="E" ,B—2e-=B2+
A.E2+>B2+>A2+>D2+ B.D2+>E2+>A2+>B2+
C.D2+>B2+>A2+>E2+ D.A2+>B2+>D2+>E2+
已知:X2、Y2、Z2、W2四种物质的氧化能力W2>Z2>X2>Y2,下列氧化还原反应能发生的是( )
| A.2NaW+Z2=2NaZ+W2 | B.2NaX+Z2=2NaZ+X2 |
| C.2NaY+W2=2NaW+Y2 | D.2NaZ+X2=2NaX+Z2 |
已知反应:2FeCl3+2KI=2FeCl2+2KCl+I2②2FeCl2+Cl2=2FeCl3③I2+SO2+2H2O=H2SO4+2HI,判断下列物质的还原能力由强到弱的顺序是( )
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |
已知X2、Y2、Z2、W2四种物质的氧化能力强弱顺序为W2>Z2>X2>Y2,则下列氧化还原反应能发生是( )
| A.2W-+Z2====2Z-+W2 | B.2X-+Z2====2Z-+X2 |
| C.2Z-+Y2====2Y-+Z2 | D.2Z-+X2====2X-+Z2 |
在碘化钾和硫酸的混合溶液中加入过氧化氢水溶液,迅速发生反应放出大量气体,反应过程可表示如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)H2O2在反应③中的作用是______(填正确选项的标号)
| A.氧化剂 | B.还原剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂也不是还原剂 |
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为______________(填“对”或“不对”),其理由是___________________________________________.
(3)上述反应说明H2O2、I2、HIO氧化性从强到弱的顺序是_______>________>______.