据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4OH- 2CO32-+6H2O,则下列说法正确的是
2CO32-+6H2O,则下列说法正确的是
| A.构成该电池的正极和负极必须是两种活性不同的金属 |
| B.充电时有CH3OH生成的电极为阳极 |
| C.放电时电解质溶液的pH逐渐增大 |
| D.放电时负极的电极反应为:CH3OH-6e- +8OH- = CO32- + 6H2O |
H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l)  H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是
H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是
| A.电极a为电池的正极 |
B.电极b上发生的电极反应为:O2+2H2O+4e =" 4" OH =" 4" OH |
| C.电路中每流过4mol电子,电池内部释放632kJ热能 |
| D.每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
据媒体报道:以氢氧燃料电池为动力的公交车即将在北京试运行。质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂为电极,导电离子是H+。下列对该燃料电池的描述正确的是
①正极反应为:O2+4H++4e—= 2H2O ②电子由负极流向正极
③总的化学反应为:2H2+O2 2H2O ④氢离子通过电解质向正极移动
2H2O ④氢离子通过电解质向正极移动
A.①②③ B.①②④ C.②③④ D.①②③④
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钻(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为 ,下列说法正确的是( )
,下列说法正确的是( )
A.充电时,电池的负极反应为LiC6-e- Li+C6 Li+C6 |
B.放电时,电池的正极反应为CoO2+Li++e- LiCoO2 LiCoO2 |
| C.羧酸、醇等含活泼氢气的有机物可用作锂离子电池的电解质 |
| D.锂离子电池的比能量(单位质量释放的能量)低 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O===Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
用铅蓄电池电解甲、乙电解池中的溶液。已知铅蓄电池的总反应为:
Pb (s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O (l),电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是
| A.d极为阴极 |
| B.放电时铅蓄电池负极的电极反应式为:PbO2(s)+4H+(aq)+SO42-(aq)+4e-=PbSO4 (s)+2H2O (l) |
| C.若利用甲池精炼铜,b极应为粗铜 |
| D.若四个电极材料均为石墨,当析出6.4 g Cu时,两池中共产生气体3.36 L(标准状况下) |
【改编】LED系列产品是被看好的一类节能新产品, 下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是
| A.a处通入氢气,发生了还原反应:H2-2e-+2OH-=2H2O |
| B.b处通入氧气,为电池的正极 |
| C.该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替 |
| D.P-型半导体连接的是电池负极 |
某充电宝锂离子电池的总反应为: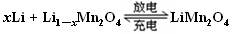 ,某手机镍氢电池总反应为:
,某手机镍氢电池总反应为: (M为储氢金属或合金),有关上述两种电池的说法不正确的是
(M为储氢金属或合金),有关上述两种电池的说法不正确的是
| A.锂离子电池放电时Li+向正极迁移 |
| B.镍氢电池放电时,正极的电极反应式:NiOOH+H2O+e-="=" Ni(OH)2+OH- |
| C.上图表示用锂离子电池给镍氢电池充电 |
| D.锂离子电池充电时,阴极的电极反应式:LiMn2O4—xe-="=" Li1-xMn2O4+ xLi+ |
Li﹣Al/FeS电池是一种正在开发的电动车用二次电池,该电池反应式为:2Al+6Li++3FeS=2Al3++3Li2S+3Fe.有关该电池的下列说法中,错误的是( )
| A.作为二次电源,该电池在使用的过程中至少存在3种形式的能量转化 |
| B.Li﹣Al在电池中作为负极材料,负极的电极反应式为Li﹣e﹣=Li+ |
| C.该电池替代现在电动车广泛使用的铅蓄电池可以减少重金属的污染 |
| D.充电时,阳极发生的电极反应式为:Li2S+Fe﹣2e﹣=2Li++FeS |
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如下图装置①。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列有关叙述不正确的是
| A.该燃料电池负极发生的电极反应为:N2H4+4OH-−4e-==N2↑+4H2O |
| B.用该燃料电池作为装置②的直流电源,产生7.1g Cl2至少需加入0.5 mol N2H4 |
| C.该燃料电池中,电子从左侧电极经外电路流向右侧电极,溶液OH-迁移到左侧 |
| D.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如下,该电池工作时反应为: 4VB2 + 11O2→4B2O3 + 2V2O5。下列说法正确的是( )

| A.电极a为电池负极 |
| B.VB2中V的化合价为+4价 |
| C.电子由VB2极经KOH溶液流向a电极 |
| D.VB2极发生的电极反应为:2VB2 + 22OH−-22e−=V2O5 + 2B2O3 + 11H2O |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法不正确的是 ( )
①在标准状况下,每消耗5.6L CH4可以向外电路提供2mole-
②通过甲烷电极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
③通过甲烷的电极为电池的正极,通过氧气的电极为负极
④电池放电后,溶液PH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
英国赫瑞瓦特大学陶善文博士研究出以尿素为动力的燃 料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,关于该电池描述正确的是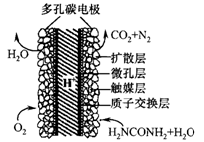
| A.电池工作时H+移向负极 |
| B.该装置还可以将电能转化成为化学能 |
| C.理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2 |
| D.电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+ |
一种新型熔融盐燃料电池具有高发电效率。现用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,其总反应为:2CO+O2===2CO2。则下列说法中正确的是 ( )
| A.通CO的一极是电池的正极 |
B.负极发生的电极反应是:O2+2CO2+4e-―→2CO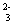 |
C.负极发生的电极反应是:CO+CO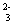 -2e-―→2CO2 -2e-―→2CO2 |
| D.正极发生氧化反应 |