二硫化亚铁是Li/FeS2电池的正极活性物质,可用水热法合成。FeSO4、Na2S2O3、S及H2O在200 ℃连续反应24 h,四种物质以等物质的量反应,再依次用CS2、H2O洗涤、干燥及晶化后得到。
(1)合成FeS2的离子方程式为_____________________________________。
(2)用水洗涤时,如何证明SO42—已除尽?________________________________________。
(3)已知1.20 g FeS2在O2中完全燃烧生成Fe2O3和SO2气体放出8.52 kJ热量,FeS2燃烧反应的热化学方程式为__________________________。
(4)取上述制得的正极材料1.120 0 g(假定只含FeS一种杂质),在足量的氧气流中充分加热,最后得0.800 0 g红棕色固体,试计算该正极材料中FeS2的质量分数(写出计算过程)。
(共10分)写出符合要求的离子方程式
1)向FeBr2溶液中通入少量Cl2___________________________________________
2)向NaAlO2-溶液中通入足量CO2________________________________________
3)Ba(OH)2溶液中加入足量NaHCO3____________________________________
4)Na2O2投入FeCl2溶液中_______________________________________________
5)NaHCO3溶液中有少量Na2CO3的除杂反应_______________________________
在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,能够观察到的实验现象是易拉罐突然变瘪了,可经过一段时间之后,又可以观察到的现象是 ,试解释易拉罐变瘪的原因 ,并解释后一现象的原因 ,写出反应过程中的两个离子方程式 、 。
某结晶水合物A含有两种阳离子和一种阴离子。将溶有90.60gA的水溶液分成两等份,向第一份逐滴加入NaOH溶液,溶液先出现白色沉淀后完全溶解,此过程中产生2.24 L(标准状况)刺激性气味的气体。向第二份加入过量的Ba(OH)2溶液,过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.60 g。
请回答以下问题:
(1)A的摩尔质量为 。
(2)试通过计算确定该结晶水合物的化学式为 。
(3)若第二份加入75.00 mL2.00 mol·L-1的Ba(OH)2溶液,则得到的沉淀质量为 。
某探究性学习小组设计如右图所示装置分别进行如下探究实验,请回答下列问题:

| 实验 |
药品 |
制取气体 |
量气管中的液体 |
| Ⅰ |
Cu、稀HNO3 |
|
H2O |
| Ⅱ |
NaOH固体、浓氨水 |
NH3 |
|
| Ⅲ |
镁铝合金、足量NaOH溶液 |
H2 |
H2O |
(1)实验I通过收集并测量NO气体的体积来探究铜样品的纯度,有的同学认为该实验设计不可行,主要原因是 ;
(2)实验Ⅱ中量气管中的液体最好是 (填字母编号, 下同)
A.NaOH溶液 B.氨水 C.煤油 D.氯化铵溶液
实验剩余的NH3需吸收处理,以下各种尾气吸收装置中,不能防止倒吸的是 ;

(3)①写出实验Ⅲ中涉及的离子反应方程式 ;
②反应前,先对量气管进行第一次读数。读数时,应注意的操作是 ,并使视线与凹液面最低处相平;反应后,待装置温度冷却到室温时,再对量气管进行第二次读数。实验前,如拆去导管D,测得的气体体积将 (填“偏大”、“偏小”、或“无影响”)。
③实验Ⅲ在25℃、1.01×105Pa条件下获得以下数据:
| 编号 |
镁铝合金质量 |
量气管第一次读数 |
量气管第二次读数 |
| ① |
1.0g |
10.0mL |
376.6mL |
| ② |
1.0g |
10.0mL |
364.7mL |
| ③ |
1.0g |
10.0mL |
377.0mL |
根据上述数据,计算出镁铝合金中铝的质量分数为 。
某校化学兴趣小组用如图所示过程除去AlCl3中含有Mg2+、K+杂质离子并
尽可能减少AlCl3的损失。回答下列问题: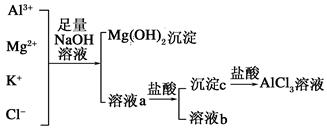
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:________________
(2)氢氧化钠溶液能否用氨水代替,为什么?______ __________。
(3)溶液a中存在的阴离子有_____ ___;在溶液a中加入盐酸时需控制盐酸的量,为什么______________为此,改进的方法是将盐酸改成通入 气体。
有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑
④X+Ca(OH)2―→Y+CaCO3↓
回答下列问题:
(1)W、Y、Z的化学式分别是:W:________、Y:________、Z:________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式)
(3)若④反应在溶液中进行,写出其离子方程式
按要求回答下列问题:
(1)生产普通玻璃的主要原料是______。
(2)PbSO4难溶于水,易溶于醋酸钠溶液,且发生复分解反应,化学方程式为:
PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb,该反应的离子方程式为 。
(3)铁制品在潮湿的空气中易被氧化而锈蚀。以下是探究铁制品在潮湿的空气中铁元素被氧化价态的一个实验方案,请你将它补充完整(检验铁元素的价态必须使用中学化学中最灵敏的试剂):取铁锈样品,
某研究小组以CaCl2和H2为原料,试图制备 +1价Ca的化合物,结果发现产物中只有两种化合物(甲和乙)。元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性。请回答下列问题:
(1)生成甲的化学反应方程式为 。
(2)甲与水反应可得H2,其化学方程式是 。
(3)在加热条件下,乙的水溶液(浓)与MnO2反应的离子方程式是 ;乙的水溶液与Fe反应所得的溶液不稳定,保存该溶液的措施是 。
(4)请写出一个你认为可能得到CaCl的化学方程式(以CaCl2为原料) 。
(1)(2)题每空1分,(3)(4)小题每空2分,共10分
A、B、C、D、E 5瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3和AgNO3中的一种.已知:
①A与B反应有气体生成;
②B与C反应有沉淀生成;
③C与D反应有沉淀生成;
④D与E反应有沉淀生成;
⑤A与E反应有气体生成;
⑥②和③的反应中生成的沉淀是同一种物质。
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是___ ___;
(2)A是_______________,B是_______________,C是_______________,
D是_______________,E是_______________。
(3)A 与E 反应的离子方程式是_________________________________________
(4)④中反应的离子方程式是
写出下列反应的离子方程式
(1)硫酸铜溶液与氢氧化钠溶液混合
(2)碳酸钠溶液与稀盐酸混合
(3)氢氧化钡溶液与稀硫酸混合
(4)少量的碳酸氢钠溶液与过量的澄清石灰反应
向炭粉、Cu和Fe2O3组成的混合粉末中加入一定量的稀硫酸,充分反应后过滤,得到溶液A,将沉淀物洗涤、干燥,得到固体B。
(1)碳的原子结构示意图为 ,氧元素在周期中的位置是 。
(2)加入稀硫酸后,发生反应的离子方程式 ,溶液A中一定存在的金属阳离子是 。
(3)关于固体B的成分,下列选项中可能的有 。
A.炭粉
B.炭粉和Cu
C.炭粉和Fe2O3
D.Cu和Fe2O3
E.炭粉、Cu和Fe2O3
(12分)某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是________。
(2)根据上述框图反应关系,可推出沉淀C的成分: ;
写出沉淀D的一个用途____ ____;写出沉淀B的一个用途____ ____;检验溶液E中阳离子的操作方法(只检验一种即可) 。
(3)写出①、②、③三个反应的化学方程式(属离子反应的写离子方程式)
①______________________________________________________________;
②________________________________________ ____________________;
③______________________________________________________________;
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2 NaClO3+4 HCl=2 ClO2↑+Cl2↑+2 NaCl+2 H2O
方法二:2 NaClO3+H2O2+H2SO4=2 ClO2↑+O2↑+2 Na2SO4+2 H2O
(1)方法一的离子方程式为 .
(2)方法二中被氧化的物质是 ,若反应中有0.1mol电子转移,则产生的ClO2气体在标准状况下的体积为 L.
(3)用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是 。
有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行以下实验:
①取少量白色固体加到足量的水中,得到白色沉淀,上层清液为无色。
②向上述悬浊液中加入足量的稀硝酸,白色沉淀消失,并有气泡产生。
③取少量②的溶液滴入硝酸钡溶液,有白色沉淀生成,再加入稀硝酸,白色沉淀不消失。
根据上述实验现象判断:白色固体中一定含有 ,
一定不含有 , 可能会有 ;
上述实验中有关反应的离子方程式 。