(1)已知亚氯酸(HClO2)不稳定,可分解,分解反应的离子方程式为:HClO2→ClO2↑+H++Cl﹣+H2O(未配平).当有3.2mol电子发生转移时,发生分解的HClO2的物质的量是 mol.
(2)有Fe2+、NO3﹣、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中氧化剂与还原剂的物质的量之比为 .
我国规定饮用水质量标准必须符合下列要求:
| pH |
6.5~6.8 |
| Ca2+、Mg2+总浓度 |
<0.0045mol/L |
| 细菌总数 |
<100个/L |
以下是源水处理成自来水的工艺流程示意图:
源水→曝气池  一级沉降池
一级沉降池 二级沉降池
二级沉降池  过滤池→自来水
过滤池→自来水
(1)源水中含Ca2+ 、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式 。
(2)凝聚剂除去悬浮固体颗粒的过程 (填写编号,多选倒扣分)
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4.7H2O是常用的凝聚剂,它在水中最终生成 沉淀。
(3)通入二氧化碳的目的是 和 。
(4)气体A的作用是 。这种作用是基于气体A和水反应的产物
具有 性.
(5)下列物质中, 可以作为气体A的代用品。(填写编号,多选倒扣分)
①Ca(ClO)2 ②NH3 (液) ③K2FeO4 ④SO2
化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
。
(2)现有一瓶胃舒平药片(复方氢氧化铝),请写出其与胃酸(主要成分为稀盐酸)反应的离子方程式 。
完成下列化学方程式并改写成离子方程式:(每题3分)
(1) AgNO3 + BaCl2:
(2) Na2CO3 + Ca(OH)2:
用相应的离子方程式说明原因:
(1)配制氯化铁溶液时,往往需要加入少量的稀盐酸: 。
(2)热的纯碱溶液可以用来除油污: 。
(3)泡沫灭火器中装的是NaHCO3和Al2(SO4)3两种浓溶液,可用来灭火: 。
请你参与识别化肥的探究活动,有五种化肥,分别是硫酸钾、氯化钾、碳酸氢铵、氯化铵和硝酸铵。
第一步:称取五种化肥各10 g,分别研细;
第二步:硝酸铵和熟石灰反应的化学方程式是:_____________________________________。
第三步:另取三种铵盐各少量,分盛于三支试管中,均滴入少量盐酸,无明显现象的是____________,有气泡放出的是________。反应的化学方程式:______________________________________________________________。
第四步:另取氯化铵和硝酸铵两种铵盐进行识别,写出识别时发生反应的化学方程式:_____________________________________________________________。
第五步:取两种钾盐,分别在试管中配成溶液,各滴入几滴氯化钡溶液,生成白色沉淀的钾盐是________,无明显现象的钾盐是________。
Ⅰ.在MgCl2溶液中滴入NaOH溶液,会有白色沉淀出现,该白色沉淀不能溶解于过量的氢氧化钠中。反应的离子方程式是 ;但Al(OH)3却能溶解在过量NaOH溶液中,该反应的离子方程式是 。
Ⅱ.在含有0.4molHCl和0.1molMgSO4的混合溶液中逐滴加入Ba(OH)2 溶液,产生的沉淀质量m与加入Ba(OH)2的物质的量n之间的关系如图所示。
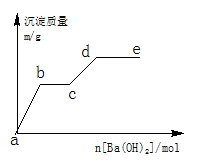
(1)a→b过程中发生反应的离子方程式是
(2)b→c发生反应的离子方程式是
(3)d点沉淀质量是 g。
A~G各物质间的关系如图,其中B、D为气态单质。
请回答下列问题:
(1)物质C、E分别为 、 。(填名称)
(2)反应①可选用不同的A进行,若反应在常温下进行,其化学方程式为 。
(3)反应②的离子方程式为 。
(4)新配制的F溶液应加入________以防止其转化为G。请设计实验检验F、G的混合溶液中F的金属阳离子。(写出试剂、操作、现象、结论) 。
现有下列十种物质:
①H2;②铝;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁液体;⑧氨水;⑨稀硝酸;⑩Al2(SO4)3
上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 |
金属单质 |
氧化物 |
溶液 |
胶体 |
电解质 |
| 属于该类的物质 |
|
|
|
|
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-= H2O,该离子反应对应的化学方程式为 。
(3)⑩在水中的电离方程式为 ,
(4)少量的④通入⑥的溶液中反应的离子方程式为 。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是 (填化学式),氧化剂与还原剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。该反应的离子方程式为 。
钨是我国丰产元素。自然界中钨主要以钨(+6)酸盐的形式存在。黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4)。黑钨矿传统冶炼工艺流程图如下:
(1)已知上述转化中,除最后一步外,W的化合价未发生变化,则产品C的化学式为 ;如何将其冶炼成单质(用化学方程式表示): 。
根据金属的活动性不同,金属的冶炼方法一般有 三种。
(2)写出第一步转化中“Mn2+→MnO2”的离子方程式 。
(3)我国钨化学研究的奠基人顾翼东先生采用另外的反应制得了一种蓝色的、非整比的钨的氧化物WO(3-x)。这种蓝色氧化钨具有比表面大、易还原的优点。一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在正五价和正六价两种价态的钨,已知x的值为0.1,则蓝色氧化钨中这两种价态的钨原子数之比为 。
完成下列化学方程式或离子方程式。
①.过氧化钠与二氧化碳反应化学方程式:
②.铝和NaOH溶液反应化学方程式:
③.氢氧化铝和NaOH溶液反应离子方程式:
④.硫酸亚铁与氢氧化钠溶液离子方程式:
⑤.FeCl3和Cu反应离子方程式:
某晶体(结晶水合物)由五种短周期元素组成。常温下,将该晶体溶于蒸馏水后可电离出三种离子(忽略水的电离),其中两种离子含有的电子数均为10个。将该溶液分成等量2份,一份中加入足量稀盐酸,无明显现象,再加入BaCl2溶液,产生白色沉淀;向另一份中逐滴加入NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。

请回答下列问题:
(1)若该晶体的摩尔质量为906g·mol-1,写出该晶体的化学式 ;
(2)B点溶液的pH 7(填“<”、“>”或“=”),用化学用语表示其原因 。
(3)若向该晶体的水溶液中逐滴加入Ba(OH)2溶液至产生最多的沉淀,写出该变化的离子方程式 。
(4)C点溶液中所含溶质的化学式为 ;此时溶液中各种离子浓度由大到小顺序为 。
某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是
Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+)。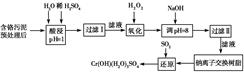
| 氢氧化物 |
Fe(OH)3 |
Mg(OH)2 |
Al(OH)3 |
Cr(OH)3 |
| pH |
3.7 |
11.1 |
8 |
9(>9溶液) |
部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见上表。
(1)酸浸时,为了提高浸取率可采取的措施为________________(至少写一条)。
(2)调pH=8是为了除去________(填Fe3+、Al3+、Ca2+、Mg2+,下同)。
(3)钠离子交换树脂的原理为Mn++nNaR―→MRn+nNa+,被交换的杂质离子是________。
(4)试配平反应方程式: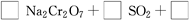
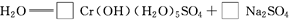 ;
;
生成1 mol Cr(OH)(H2O)5SO4消耗SO2的物质的量为________。
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
(1)工业上制备ClO2的反应原理为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是________。
| A.只有还原性 | B.还原性和酸性 |
| C.只有氧化性 | D.氧化性和酸性 |
②若上述反应中产生0.1 mol ClO2,则转移电子的物质的量为________mol。
(2)目前已开发出用电解法制取ClO2的新工艺。
①上图是用石墨作电极,一定条件下电解饱和食盐水制取ClO2的示意图。则阳极产生ClO2的电极反应式为_____________________________________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为________mol,用平衡移动原理解释阴极区pH增大的原因:______________________________________。
(3)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-a mg/L,现用ClO2将CN-氧化,产物中有两种气体生成,其离子反应方程式为________________;处理100 m3这种污水,至少需要ClO2________mol。
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式: 。
(2)下列三种情况下,离子方程式与 (1)相同的是 (填序号)。
A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用如图中的 (填序号)曲线表示。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示。向该烧杯中缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将 。