下列各组离子在指定溶液中,能大量共存的是
| A.含有NaClO的溶液中:K+,NH4+,Fe3+,Br-,SO32- |
| B.所含溶质为Na2S2O3的溶液:K+、SO42-、NO3-、H+ |
| C.加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42- |
| D.使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42- |
下列解释事实的离子方程式正确的是
| A.铁和稀硝酸反应制得浅绿色溶液:Fe+ 4H+ + NO3- =Fe3+ + NO↑+ 2H2O |
| B.向Ca(ClO)2溶液中通入过量CO2制取次氯酸:2ClO-+ H2O + CO2=2HClO + CO32- |
| C.向酸性KMnO4溶液中通入SO2:2MnO4-+ 5SO2 + 4OH-=2Mn2++ 5SO42-+ 2H2O |
| D.0.01 mol·L—1 NH4Al(SO4)2溶液与0.02 mol·L—1 Ba(OH)2溶液等体积混合:NH4++ Al3++ 2SO42-+ 2Ba2++ 4OH—=2BaSO4↓+ Al(OH)3↓+ NH3·H2O |
下列表示化学反应的离子方程式正确的是
| A.Na2O2与水反应:Na2O2 + H2O = 2Na+ + 2OH- + O2↑ |
B.用惰性电极电解MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
| C.Ba(OH)2溶液中加入过量的NaHSO4溶液:Ba2++SO42-+OH-+H+=BaSO4↓+H2O |
| D.硫酸亚铁溶液中加入酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O |
下列离子方程式中正确的是
| A.将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HClO |
| B.向FeBr2溶液中通入过量Cl2:2Fe2++4Br-+2Cl2=2Fe3++2Br2+4Cl- |
| C.向硫酸氢钾溶液中加入Ba(OH)2溶液至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| D.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
下列离子方程式正确的是
| A.向澄清石灰水中加入等物质的量的NaHCO3溶液:Ca2++2OH-+ 2HCO3- = CaCO3↓+CO32-+2H2O |
| B.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O |
| C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
| D.明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
下列离子方程式中,正确的有( )个
⑴澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
⑵氢氧化钡与硫酸反应:OH-+H+=H2O
⑶铜片与硝酸银溶液反应:Cu+Ag+=Cu2++Ag
⑷氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-=Mg(OH)2↓
⑸铁片投入稀盐酸中:2Fe+6H+=2Fe3++3H2↑
⑹氨水与盐酸的反应:OH-+H+=H2O
⑺碳酸氢钠与盐酸反应:HCO3-+H+=CO2↑+H2O
⑻Na2O与水反应:O2-+H2O=2OH-
⑼少量的NH4HSO4溶液与Ba(OH)2溶液的反应:NH4++H++SO42-+Ba2++2OH-=NH3.H2O+H2O+BaSO4↓
⑽向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性: 2H++SO42-+Ba2++2OH-= 2H2O+BaSO4↓
| A.1 | B.2 | C.3 | D.4 |
下列反应的离子方程式错误的是
A.NH4HCO3溶液与足量的NaOH溶液混合加热:NH4++HCO3-+2OH- NH3↑+CO32-+2H2O NH3↑+CO32-+2H2O |
| B.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O |
| C.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| D.等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合:Ca2++HCO3-+OH-=CaCO3↓+H2O |
下列选项中,离子方程式书写正确的是
| A.向硝酸银溶液中加入足量的氨水:Ag+ +2NH3·H2O = Ag(NH3)2+ + 2H2O |
| B.向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:3Fe2++4H++NO3-= 3Fe3++ 2H2O+NO↑ |
| C.泡沫灭火器的灭火原理:2Al3+ +3CO32-+3H2O = 2Al(OH)3↓+ 3CO2↑ |
| D.用足量的氨水处理合成氨工业的尾气:SO2+ NH3·H2O = NH4+ + HSO3- |
下列离子方程式中正确的是
| A.NH4HCO3溶液与过量NaOH溶液反应:NH4+ + OH_ = NH3↑+2H2O |
| B.向FeBr2溶液中通入Cl2,当n(FeBr2)=n(Cl2)时:2Fe2++4Br−+3Cl2=2Fe3++2Br2+6Cl− |
| C.向FeI2溶液中通入Cl2,当n(FeI2):n(Cl2)=1:1时: 2I−+Cl2=I2+2Cl− |
| D.向烧碱溶液中通入CO2,当n(NaOH):n(CO2)=3:2时: OH−+CO2=HCO3− |
类推思维是化学解题中常用的一种思维方法。下列有关离子方程式的类推正确的是
| |
已知 |
类推 |
| A |
将Fe加入CuSO4溶液中 Fe+Cu2+===Cu+Fe2+ |
将Na加入到CuSO4溶液中 2Na+Cu2+===Cu+2Na+ |
| B |
稀硫酸加入Ba(OH)2溶液至中性 2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O |
NaHSO4溶液加入Ba(OH)2溶液至中性 H++SO42-+Ba2++OH-===BaSO4↓+H2O |
| C |
向氯化铝溶液中加入足量NaOH溶液 Al3++4OH-===AlO2-+2H2O |
向氯化铝溶液中加入足量氨水 Al3++4NH3·H2O===AlO2-+2H2O+4NH4+ |
| D |
向Ca(OH)2溶液中通入过量CO2 CO2+OH-===HCO3- |
向Ca(OH)2溶液中通入过量SO2 SO2+OH-===HSO3- |
能正确表示下列反应的离子方程式是
| A.向碳酸氢钙溶液中滴入过量澄清石灰水:Ca2++2HCO3—+2OH— =CaCO3↓+CO32—+2H2O |
B.NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-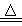 NH3+SO32-+2H2O NH3+SO32-+2H2O |
| C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性: H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D.向KIO3与KI混合溶液中加入醋酸发生反应生成I2:IO3-+5I-+6H+=3I2+3H2O |
下列图示与对应的叙述相符的是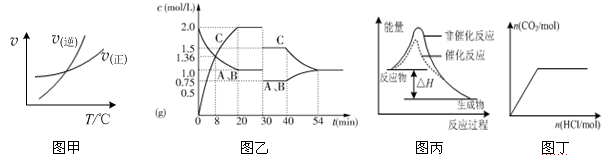
| A.由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0 |
B.图乙代表等物质的量的气体A和B,在一定温度下发生反应A(g)+B(g) 2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等 2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等 |
| C.图丙表示该反应为放热反应,且催化剂不能改变反应的焓变 |
| D.图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系 |
下列离子方程式正确的是
| A.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
B.甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH- HCOO-+NH4++2Ag↓+3NH3+H2O HCOO-+NH4++2Ag↓+3NH3+H2O |
| C.向小苏打溶液中加入醋酸:CO32-+2CH3COOH ===CO2↑+H2O+2CH3COO- |
D.乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2+OH— Cu2O↓+CH3COO—+3H2O Cu2O↓+CH3COO—+3H2O |
下列解释事实的离子方程式正确的是
| A.用惰性电极电解氯化镁溶液:2Cl-+2H2O电解Cl2↑+ H2↑+2OH- |
| B.一定量Cl2通入FeI2溶液中,完全反应后测得溶液中c(Fe 3+)=c(Fe2+):5Cl2+8I-+2Fe2+=4I2+2Fe 3++10Cl- |
| C.向CH2Br-COOH中加入足量的氢氧化钠溶液并加热:CH2Br-COOH+OH-−加热→CH2Br-COO-+ H2O |
| D.用氢氟酸在玻璃上“刻字”:SiO2+4H++4F-= SiF4↑+2H2O |