下列化学反应的离子方程式书写正确的是
| A.钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B.小苏打与醋酸反应:HCO3—+H+==CO2↑+H2O |
C.氯气与水反应:Cl2 +H2O 2H+ + Cl—+ ClO— 2H+ + Cl—+ ClO— |
| D.氯化铝溶液与过量氨水反应:3NH3?H2O+ Al3+ =Al(OH)3↓+3NH4+ |
下列离子方程式正确的是
| A.硫酸铜溶液与氢氧化钡溶液反应:Ba2+ + SO42- =BaSO4↓ |
| B.用醋酸溶解水垢中的Mg(OH)2:2H+ + Mg(OH)2=Mg2++2H2O |
| C.工业上用氨水吸收二氧化硫:2OH- + SO2 = SO32- + H2O |
| D.在NaOH溶液中加入少量Ca(HCO3)2溶液:Ca2++2HCO3 - +2OH - = CaCO3↓+ CO32- + 2H2O |
下列离子方程式中,正确的是
| A.铁与氯化铁溶液反应:Fe + Fe3+ ="=" 2Fe2+ |
B.大理石与稀盐酸反应:CO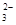 + 2H+ ="=" CO2 ↑ + H2O + 2H+ ="=" CO2 ↑ + H2O |
C.铜与稀硝酸反应:Cu + H+ + NO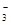 ="=" Cu2+ + NO↑ + H2O ="=" Cu2+ + NO↑ + H2O |
| D.氯气与氢氧化钠溶液反应:Cl2 + 2OH-="=" Cl- + ClO- + H2O |
“探险队员”——盐酸,不小心走进了化学迷宫,迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
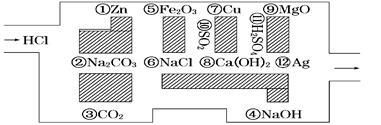
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)_____________。
(2)在不能“吃掉”盐酸的物质中,属于非电解质的是________(填写物质序号),在能“吃掉”盐酸的物质中,属于电解质的是 (填写物质序号)。
(3)如果将盐酸换成碳酸镁,它能沿着盐酸走出的路线“走出”这个迷宫吗?填“能”或“不能”_____,写出离子方程式说明其原因: 。
(4)写出氧化铝与④反应的化学方程式 ,氧化铝属于 ____________氧化物(填“酸性”“碱性”或“两性”)。
下列离子方程式表达不正确的是 ( )
A.小苏打溶液跟烧碱溶液反应: |
B.氢氧化钡溶液跟硫酸反应: |
C.三氯化铁溶液跟过量氨水反应: |
D.氢氧化铝与氢氧化钠溶液反应: |
下列离子方程式中,正确的是
| A.稀硫酸与氢氧化钡溶液反应:H+ +OH—=H2O |
| B.铁与氯化铁溶液反应:Fe +2Fe3+=3Fe2+ |
| C.实验室制氯气:MnO2+4HCl=Mn2++2Cl—+Cl2↑+2H2O |
| D.向氯化铝溶液滴加少量氨水:Al3++3OH—=Al(OH)3↓ |
金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3+ +Fe3+。下列说法正确的是
| A.可用电解熔融CeO2制取金属铈,铈在阳极生成 |
B.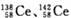 是同素异形体 是同素异形体 |
| C.铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2 |
| D.铈的原子核外有58个电子 |
已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
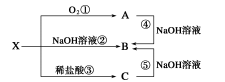
(1)写出下列物质的化学式:X ,A ,B C ;
(2)写出以下反应的离子方程式:
②
④
在如图所示的一些常见单质,化合物等物质之间的转化关系中(有些反应过程中的水,部分产物和反应条件未全部列出),已知反应①是氯碱工业的最基础的反应,A、B、F、H、J的焰色反应均为黄色,热的F溶液可以去除物品表面的油污,I为地壳中含量最多的金属元素的单质,L是典型的两性氧化物,在常温常压下C、D、G均为气体,D呈黄绿色,G是形成温室效应的主要气体.
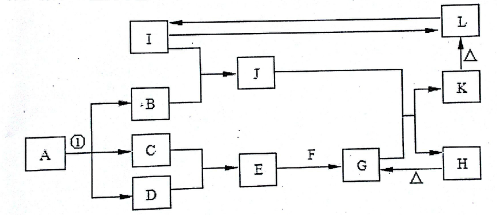
(1)反应①进行的条件为 .
(2)化合物F的化学式为 .
(3)I与氧化铁反应的化学方程式为 .
(4)J的水溶液与G反应生成K和H的离子方程式为 .
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是 (用离子方程式表示),FeCl3净水的原理是 。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+) = 1.0 × 10-3 mol·L-1 , c(Cl-) = 5.3 × 10-2 mol·L-1,则该溶液的pH约为 。
②完成NaClO3氧化FeCl2的离子方程式:  Fe2++
Fe2++ ClO3-+
ClO3-+  =
=  Fe3++
Fe3++ Cl-+
Cl-+ 。
。
(3)FeCl3在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是 (填序号)。
| A.加水稀释 | B.降温 | C.加入NH4HCO3 | D.加入NH4Cl |
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
盛放NaOH溶液的试剂瓶不能用玻璃塞,是为了防止发生反应(用离子方程式表示)________,避免瓶口与瓶塞粘在一起。
硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
| 物质 |
熔点/℃ |
沸点/℃ |
其它性质 |
| SO2Cl2 |
-54.1 |
69.1 |
①易水解,产生大量白雾 ②易分解:SO2Cl2  SO2↑+Cl2↑ SO2↑+Cl2↑ |
| H2SO4 |
10.4 |
338 |
吸水性且不易分解 |
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器A冷却水的进口为 (填“a”或“b”)。
(2)仪器B中盛放的药品是 。
(3)实验时,装置丁中发生反应的离子方程式为 。
(4)装置丙的作用为 ,若缺少装置乙,则硫酰氯会水解,该反应的化学方程式为 。
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4 + SO2Cl2,此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的方法是 。
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液): 。
下列离子方程式正确的是
| A.铁粉撒入稀硫酸中2Fe + 6H+ →2Fe3+ + 3H2↑ |
| B.向AlCl3溶液中加入过量的氨水:Al3++4NH3·H2O→AlO2-+4NH4++2H2O |
| C.把金属钠放入冷水中:Na+H2O→Na++OH-+H2↑ |
| D.用氢氧化钠溶液除去铝表面的氧化铝:Al2O3+2OH-→2AlO2-+H2O |
下列离子方程式正确的是
| A.氧化镁与稀硝酸反应:O2-+2H+=H2O |
| B.向稀硫酸溶液中撒入铁粉 2Fe +6H+ = 2Fe3+ +3H2 ↑ |
| C.向碳酸钙中加入盐酸 CO32-+ 2H+ = H2O +CO2 ↑ |
| D.向氢氧化钠溶液中通入少量二氧化碳 2OH-+ CO2 = CO32-+H2O |