空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。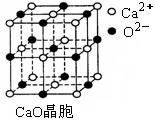
请回答下列问题:
⑴ S、N、O的第一电离能由大到小的顺序为 。
⑵ 血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒。
① 写出亚铁离子的基态电子排布式 。
② CO有多种等电子体,其中常见的两种为 。
⑶ SO2是一种大气污染物,为减轻SO2污染,火力发电厂生产中常在
燃煤中加入CaO以“固硫”。 CaO晶胞如右图所示,其中Ca2+的配位
数为 ,CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分
别为:CaO-3 401kJ/mol、NaCl-786kJ/mol。CaO晶体的熔点 NaCl
晶体的熔点(填“高于”、“等于”或“低于”)。
⑷ 随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来
越为人们所关注。甲醛是室内主要空气污染物之一(其沸点是-19.5 ℃),甲醇是“假酒”中的主要
有害物质(其沸点是64.65 ℃),甲醇的沸点明显高于甲醛的主要原因是: 。
现有六种元素A、B、C、D、E、F均为周期表中前20号元素,且原子序数依次增大。已知A和B是形成化合物种类最多的两种元素;B元素和C元素通常形成电子数为14或22的化合物。D元素的原子半径是短周期主族元素中最大的;E元素在地壳中含量居第二位;F是组成人体骨骼的牙齿的主要元素。
请回答以下问题:
(1)请画出F的离子结构示意图: ;由C、A两种元素形成的18电子化合物的电子式为 ;
(2)工业上制取E单质的化学方程式为: ;
(3)由以上六种元素两两组合所形成的化合物中,既含有离子键又含有非极性共价键的常见化合物有 和 (填化学式);它们都能与水反应生成气体,写出其中一个属于非氧化化还原反应的化学方程式 ;
(4)由A、B两种元素形成的正四面体分子是一种常见的气体燃料。通常状况下1g该物质完全燃烧生成液态水时所释放的能量为51.25kg/mol,请写出表示其燃烧热的热化学方程式: ;
(5)下图是中学常见的几种晶体结构。有关说法正确的是 (填选项)。
A.氯化钠的晶体结构中,和钠离子最近且等距离的氯离子组成了一个正八面体
B.干冰晶体是CO2分子通过范德华力结合形成的
C.石墨晶体中碳原子数与所形成的共从键数目之比为2:3
D.金刚石晶体是由五个碳原子形成的正四面体分子构成的
下表是元素周期表的一部分,表中所列字母分别代表短周期中的一种元素:
| |
|
|
|||||
| |
|
|
|
A |
B |
|
|
| C |
|
D |
|
|
|
|
|
(1)A单质电子式是 ;B元素在周期表中的位置是 。
(2)D单质与C的最高价氧化物对应水化物反应的离子方程式是 。
(3)A的气态氢化物与其最高价氧化物对应水化物反应所得产物的名称是 ,该产物对水的电离起促进作用的原因是 。
(13分)X、Y、W、Q都是短周期元素,已知Y、X、W、Q的原子半径依次增大,X、Y 同周期,X、W 同主族,W 原子核内的质子数等于X、Y 原子核内的质子数之和,W 原子最外层电子数是Q 原子最外层电子数的3 倍。
(l)写出下列元素符号:X______,Y______,W______,Q________。
(2)W元素的单质有广泛用途,工业上制备该单质的化学方程式为:
______________________________________________________________________。
(3)Y元素的某种单质通大酸性淀粉碘化钾溶液中,溶液变蓝,同时生成Y元素的另一种单质,该反应的离子方程式为:
______________________________________________________________________。
(4)Y、W、Q三种元素可组成一种盐,其溶液中各离子的浓度从大到小的顺序为
______________________________________________________________________。
四种短周期元素的性质或结构信息如下表,请根据信息回答下列问题:

(1)元素在周期表中的位置是,写出A原子的电子排布式。
(2)写出单质与水反应的化学方程式。A与C形成的化合物溶于水后,溶液的pH7(填"大于"、"等于"或"小于")。
(3)元素最高价氧化物晶体的硬度(填"大"、"小"),其理由是。
(4)、
两元素非金属性较强的是(写元素符号)。写出能证明这一结论的一个实验事实。
已知A、B、C、D、E是短周期原子序数依次增大的五种元素。且原子半径C>D>E>A>B,A、E同主族,A、B、E的原子序数之和与D元素最高价氧化物对应水化物中的电子总数相等,且最高价氧化物对应水化物中的电子数C、D之和与E相等。试推断:
(1)A_____________,B_____________,C_____________,D_____________,E_____________(填元素符号)。
(2)写出C单质在空气中燃烧产物的电子式__________________________。
(3)同周期元素中最高价氧化物对应水化物电子总数与E相等的还有_____________、_____________。(填元素符号,至少填两个)
(4)写出由A、D两元素形成的化合物与水反应的化学反应方程式____________________
_____________________________________________________________________。
未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机。这类材料中研究得较多的是化合物G。
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:①化合物G的化学式为__________________。②由1 mol NH3和0.75 mol E恰好完全反应,化合物E的分子式为_______________________。
(2)粉末状G能够与空气中的氧气和水作用,所得产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料。与氧反应所得的产物还有一种单质;与水反应生成另一种产物是该种单质元素的氢化物。请写出化合物G与水反应的化学方程式_______________________________________________________________________________。
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-xAlxOxY8-x。在接近于1 700 ℃时x的极限值约为4.0,在1 400 ℃时x为2.0,以保持整个化合物呈电中性。试问:①赛伦中各元素的化合价为Si_________,Al_________,O_________,Y_________。赛伦的晶体类型为_________。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层 只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是 ,A、B、C、D的第一电离能由小到大的顺序为 。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是 ;
(3)A的最高价含氧酸根离子中,其中心原子采取 杂化,D的低价氧化物分子的空间构型是 。
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为 ;(每个球均表示1个 原子)
A、B、C、D都是短周期元素,原子半径:D > C > A > B。已知:A、B同周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的3倍。试回答:
(1)写出元素A的名称: A 。
(2)写出由B、D组成的两种化合物的电子式: 、 。
(3)C的固态氧化物属于 晶体。
(4)写出C的氧化物与D的氧化物对应的水化物反应的离子方程式:
。
在周期表主族元素中,甲元素与乙、丙、丁三元素上下或左右紧密相邻。甲、乙两元素的原子序数之和等于丙元素的原子序数。这四种元素的最外层电子数之和为20。据此可以推断:
(1)元素甲为_______________,元素丙为_______________。
(2)元素乙和丁所形成化合物的化学式为_______________或_______________。
(3)四元素所形成的化合物相对分子质量最大的是_______________(写化学式),其分子内电子数为__________,它与水反应的化学方程式为__________(只写一个)。
元素A和B分别是处于第三、四周期的主族元素,它们的离子的电子层相差两层。已知A处于第m主族,B处于第n主族,且B的单质中含有共价键。
(1)A原子核外的电子总数是___________,最高价氧化物的化学式是___________。
(2)B原子的结构示意图是___________,其气态氢化物的化学式是___________。
(3)若它们的离子均带一个单位的电荷,则A是___________元素,B单质的电子式为___________。
(1)对于 ,按下列要求各举一例:
,按下列要求各举一例:
①Z、n、b相同而A不同___________。
②A、n、b相同而Z不同___________。
③A、Z、b相同而n不同___________。
④A、Z、n相同而b不同___________。
⑤A、Z相同而n、b不同___________。
(2)已知An+1、B(n+1)+、Cn-、D(n-1)-四种离子具有相同的电子层结构,则
①四种元素原子序数由大到小的顺序为(用A>B>C>D的形式填写,下同):______________。
②四种元素原子半径由大到小的顺序为:______________。
③四种元素离子半径由大到小的顺序为:______________。
A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p亚层中有3个电子。
⑴C原子的电子排布式为_______,若A元素的原子最外层电子排布为1s1,则A与C按个数比1:1形成的化合物的电子式__________。
⑵当n=2时,B的原子结构示意图为________,B与C形成的化合物的结构式为___________。
⑶若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,元素A在周期表中的位置是__________,A、B、C、D四种元素的第一电离能由大到小的顺序是 _____________________(用元素符号表示)。
下表是元素周期表的一部分。
| 周期 族 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 一 |
A |
|
|
|
|
|
|
|
| 二 |
|
|
|
|
D |
|
F |
H |
| 三 |
B |
|
C |
|
E |
|
G |
|
根据A—H元素在周期表中的位置,用化学式填写下列空白。
(1)单质中氧化性最强的是________________,还原性最强的是________________,化学性质最不活泼的是________________。
(2)最高价氧化物对应水化物的酸性最强的酸是________________________,最稳定的氢化物是________________。
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列为________________。
(4)D、E、F三种元素按原子半径由大到小的顺序排列为________________。
(5)A的氧化物常温下呈____________态,它和B的单质反应后所得溶液的pH_______7。