工业上制取CuCl2的生产流程如下:
请结合下表数据,回答下列问题:
| 物 质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| 完全沉淀时的pH范围 |
≥9.6 |
≥6.4 |
3~4 |
⑴ 溶液A中加入NaClO的目的是 ;
此反应离子方程式为 ;
⑵ 在溶液B中加入CuO的作用是 ;
⑶ 操作a的目的是 ;
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:
(1)在一定条件下,有aL氧气和臭氧的混合气体,当其中的臭氧完全转化为氧气,体积变为1.2aL,原混合气体中氧气的质量分数为 。
(2)若在标况下,在臭氧发生器中装入100mL氧气,最后体积为95mL。最终状态时混合气体的密度是 g/L。(保留一位小数)
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应 器中,充分加热后,粉末的质量变为21.6g。原混合气中臭氧的体积分数为__________________。
器中,充分加热后,粉末的质量变为21.6g。原混合气中臭氧的体积分数为__________________。
运用化学反应原理研究常见元素的单质及其化合物有重要意义。
(1)合成氨反应N2 (g)+3H2(g)  2NH3(g),△H<0。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不变”)。
2NH3(g),△H<0。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不变”)。
(2)向Na2C2O4溶液加入少量石蕊,溶液显 色,请用离子方程式表示出现该现象的原因: ;
(3)pH相同的氨水和氢氧化钠,分别用蒸馏水稀释至原来溶液的100倍,则稀释后两种溶液的pH分别为m和n,则m n(选填“>”“<”“=”);
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl―NH4Cl为电解质溶液制造新型燃料电池。请写出该电池的正极反应式 。
(5)氢气燃烧热值高。实验测得,在常温常压下,4gH2完全燃烧生成液态水,放出571.6kJ热量,则表示H2燃烧热的热化学方程式为 。
(6)某温度(t℃)时,测得0.01mol・L-1的NaOH溶液的pH=11。在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合,若所得混合液为中性,且a+b=12,则Va∶Vb= 。
A、C、E是中学化学中常见的单质,A是固体,C、E是无色无味的气体,D是黑色晶体,它们之间的转化关系如下图所示。
(1)写出A、B、C的化学式:
A___________________;B_________________;C______________。
(2)写出A、B转化为D、E的化学方程式_____________________________________。
(3)写出A与足量稀硝酸反应的离子方程式___________________________________。
下表是某地市场上销售的一种“加碘盐”包装袋上的部分文字说明。请根据此表,结合初中学过的化学知识,完成下列问题:
| 配料表 |
精制海盐、碘酸钾(KIO3) |
| 含碘盐 |
20—40 mg·kg-1 |
| 储藏方法 |
密封避光、防潮 |
| 使用方法 |
烹调时待食品熟后加入碘盐 |
(1)碘酸钾属于哪类物质?___________(填“纯净物”“混合物”“单质”“氧化物”)。
(2)根据含碘盐的食用方法,可推测碘酸钾的化学性质:碘酸钾在受热时_________________。
(3)我国规定,食盐含碘量为每千克食盐含碘0.035 g,相当于每千克食盐含碘酸钾___________g。
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
(1)D的化学式(分子式)是_______________,E的化学式(分子式)是_______________。
(2)A和B反应生成C的化学方程式是
_______________________________________________。
(3)E和F反应生成D、H和G的化学方程式是
_______________________________________。
①—⑩分别代表有关反应物中的一种物质,请完成下列各题: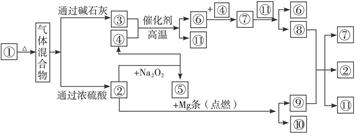
(1)①③④的化学式分别是__________________、___________________、_________________。
(2)⑧与⑨反应的化学方程式是
____________________________________________________。
有四瓶贴有标签的溶液,它们可能是碳酸钾、硝酸钡、硫酸氢钠和硫酸钾溶液。现进行有关实验,并记录部分现象。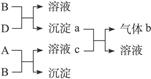
(1)推断A是_____________、B是______________、C是______________、D是_____________。
(2)D和B反应的离子方程式是____________________________________________________。
(3)A和B反应的化学方程式是
_____________________________________________________。
溴酸钾与溴化钾在酸性溶液中反应,溴元素完全转化成单质溴,试写出反应的离子方程式:__________________________,该反应中,___________mol溴酸钾中含有m g溴元素。它能___________(填“氧化”或“还原”)___________ mol的 Br-。
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH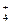 、Cl-、Mg2+、Fe3+、CO
、Cl-、Mg2+、Fe3+、CO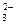 、SO
、SO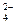 ,现每次取100.00 mL进行实验。
,现每次取100.00 mL进行实验。
①第一份加入AgNO3溶液有沉淀产生。
②第二份加足量NaOH后加热,收集到气体0.896 L(标准状态下)。
③第三份加足量BaCl2后,得干燥沉淀6.27 g,沉淀经足量盐酸洗涤干燥后,剩2.33 g。
试完成有关问题:
(1)判断K+、Cl-是否存在?K+_______,Cl-_______。(填下列序号)
A.一定存在
B.可能存在
C.一定不存在
(2)肯定存在的离子的原溶液中的物质的量浓度分别为________________。
在一定条件下可实现下图所示物质之间的变化
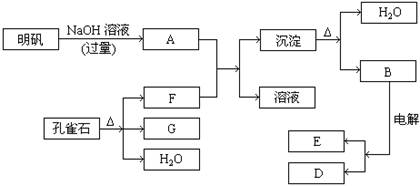
请填写以下空白:
(1)孔雀石的主要成份是CuCO3·Cu(OH)2(碱式碳酸铜)受热易分解。上图中的F是 。
(2)写出明矾溶液与过量的NaOH溶液反应的离子方程式
(3)图中所得G和D都为固体混合后在高温下可发生反应写出该反应化学方程式 。
(4)每生成1mol D同时生成 mol E。
某地有一池塘,生长着丰富的水生植物和多种鱼虾。后来,由于化工厂将大量污水排入池塘中,使水质恶化,各种水生生物先后死亡。根据题意回答下列问题:
(1)从生态平衡角度看,池塘这种变化说明了 。
(2)造成这种变化的原因是 。
(3)经检测,污水中含有0.012 mol·L-1的游离溴。可用亚硫酸钠除去污水中的溴,请写出其化学方程式 。
(4)处理这种污水5 L,需加入0.05 mol·L-1的亚硫酸钠__________L,才能将溴全部除去。
(5)要使池塘恢复本来面目.首先要解决的问题是__________.首先要恢复的生物是__________。
根据下图所示的A、B、C、D、E 五种物质的相互转化关系,按如下关系填写相应的物质和有关反应的化学方程式: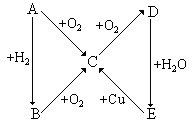
(1)当A是气体单质时,B是_________,C是____________,E是______________,由D 生成E的反应的化学方程式是__________________。
(2)当A是固体单质时,A是_________,B是____________,D是______________,由E 生成C的反应的化学方程式是__________________。
(9分)下图所涉及的物质均为中学化学中的常见物质, 其中C为O2、D为Cl2、E为Fe单质,其余为化合物。它们存在如图转化关系,反应中生成的水及次要产物均已略去。
(1)写出有关物质的化学式:
F______,G______,H______。
(2)指出MnO2在相关反应中的作用,反应①中是______剂,反应②中是______。
(3)若反应①是在加热条件下进行,则A是______;若反应①是在常温条件下进行,则A是______。
(4)写出B与MnO2共热获得D的离子方程式________________________________。
(5)写出B与F反应的化学方程式_______________________________________。
(12分)2009年2月3日下午,山西省太原市第四人民医院举行了祝贺太原禽流感患儿彭杰(女)康复出院及病情报告会。禽流感病毒是一种没有超常抵抗力的病毒。研究证明,许多常用消毒药品如漂粉精、漂白粉、高锰酸钾等,都可以将禽流感病毒杀灭。氯气及氢氧化钙充分反应,使次氯酸钙成为主要成分,得到漂粉精,其稳定性比漂白粉高。
将漂粉精溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的离子方程式为______________________________。另取少许上层清液,先滴加适量的________(填化学式)酸化,再滴加________(填化学式)溶液即可检验Cl-的存在,发生反应的离子方程式为____________________________。再取少许上层清液,滴加几滴酚酞溶液,溶液呈红色,随后溶液迅速褪色,说明漂粉精溶液呈______性并具有______性。