某校研究性学习小组选择使用下列仪器和药品,验证由铜和适量浓硝酸反应产生的气体中含有NO(实验中使用的N2和O2的用量可自由控制)。已知:①NO+NO2+2OH-====2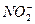 +H2O;②气体液化温度:NO2:21 ℃、NO:-152 ℃
+H2O;②气体液化温度:NO2:21 ℃、NO:-152 ℃
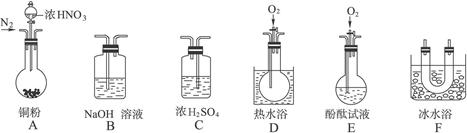
(1)现有甲、乙、丙三位同学分别设计了以下三个实验方案(用仪器的连接顺序表示)。
甲:A→C→F→D→B 乙:A→B→C→E 丙:A→F→D→B
甲、乙、丙三位同学提出的实验方案是否能验证Cu与适量浓HNO3反应产生的气体中含有NO(填“能”或“不能”):
甲:_______________;乙:_______________;丙:_______________。
具体说明不能验证的主要原因(能验证的方案,不必回答原因):
甲方案:______________________________________________________________________。
乙方案:______________________________________________________________________。
丙方案:______________________________________________________________________。
(2)实验开始时首先通入足量的N2,其目的是____________________________________。
(3)确认气体中含NO的现象是_________________________________________________。
(4)如果O2过量,则装置B中发生反应的离子方程式是______________________________。
用如图所示装置进行下列实验。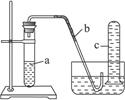
(1)在检查装置气密性后,向试管a中加入10 mL 6 mol·L-1稀硝酸和1 g铜片,立即将带有导管的橡皮塞塞紧管口。请写出试管a中有可能发生的所有反应的化学方程式________________________________________。
(2)该实验刚开始速率缓慢,随后逐渐加快,这是由于_______________________________。
(3)为了使产生的气体不至于逸散到空气中,请写出向试管a中加入试剂的操作方法______________________________________________________________________________。
(4)欲较快地制取NO,可采取的措施有(列举两种)_________________________________、________________________________________。
电子工业使用的印刷线路板,是在敷有铜膜的塑料板上以涂料保护所需的线路,然后用FeCl3的溶液与未受保护的铜膜反应以去掉铜,腐蚀后的废液中含有大量的Cu2+。为了回收这一部分Cu2+并制成硫酸铜晶体(CuSO4·5H2O),常用如下步骤:
①向废液中加过量的铁屑,搅拌,静置;②滤出固体物质;③将滤出的固体物质加热煅烧;④把煅烧后的物质放在硫酸中溶解;⑤调节溶液的pH在3.4—4之间,使Fe(OH)3沉淀完全,过滤;⑥浓缩滤液,析出晶体;⑦将过滤得到的晶体溶解,再结晶。
(1)上述③步操作所得煅烧产物成分是_______________。
A.CuO B.CuO和FeO C.CuO和Fe2O3 D.CuO和Fe3O4
(2)上述第⑤步操作中,调节溶液的pH宜加入的物质是_______________。
A.氧化铜粉末 B.NaOH溶液 C.稀氨水 D.Na2CO3
(3)上述第⑥步操作中,用浓缩滤液而不用蒸干溶液的主要原因是_______________。
A.蒸干所得到的物质可能含有无水硫酸铜
B.温度升高CuSO4溶解度增大
C.温度升高Cu2+被还原为Cu
D.温度升高CuSO4分解
实验室里化学试剂的保存方法是不相同的,下图中A、B、C、D是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内:①浓硫酸②碳酸钠溶液③大理石④酒精⑤氯水⑥浓硝酸
| A |
B |
C |
D |
 |
 |
 |
 |
| ( ) |
( ) |
( ) |
( ) |
大气压强对许多物理实验和化学实验有着重要影响,制取氨气并完成喷泉实验。
(1)写出实验室制取氨气的化学方程式: 。
(2)收集氨气应使用 法,要得到干燥的氨气可选用 作干燥剂。
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是 ,该实验的原理是 。
(4)如果只提供如图2的装置,请说明引发喷泉的方法。
水蒸气通过灼热的煤所产生的混合气,其主要成分是CO、H2,还含有CO2和水蒸气,请用下图所示装置设计一个实验,以确认上述混合气中含有CO和H2。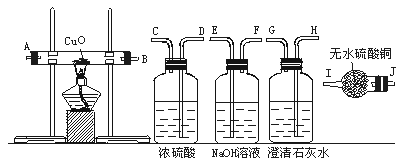
(1)连接上述装置的正确顺序是:(填接口字母)混合气→( ),( )接( ),( )接( ),( )接( ),( )接( ),( ).
(2)确认混合气中含有H2的实验现象是__________,其理由是_________________。
(12分)在右图所示的实验装置中,A中盛有品红溶液,B中盛有NaOH溶液。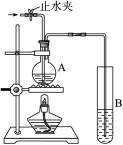 请回答下列问题:
请回答下列问题:
(1)若向A中通入足量的二氧化硫气体,A中的现象是______________________。
(2)若向A中通入足量的氯气后,再加热A,A中的溶液______(填“能”或“不能”)恢复到原来的颜色。
(3)如果A中盛的是氨水,B中盛的是无色酚酞溶液,微热A,B中溶液会变为红色,则此时表现氨水具有______性和______性。
(4)如果A中盛的是浓硫酸,加入铜,加热反应,此反应中表现浓硫酸的酸性和______性。
(5)如果A中盛的是盐酸,加入铜粉,为了让铜粉溶解,可以加入NaNO3,反应的离子方程式为:3Cu+2NO+8H+===3Cu2++2NO↑+4H2O,请用单线桥标出其电子转移的方向和数目。