(12分)(1)为测定一种气态烃A的化学式,取标准状况下一定体积的A置于密闭容器中,再通入一定体积的O2,用电火花引燃,定性实验表明产物是CO2、CO和水蒸气。相关方案如下:(箭头表示气体流向,实验前系统内空气已排除)
试回答(不要求写计算过程):
A的实验式(最简式)是___________,根据所学知识,气态烃A的分子式为___________。
(2)质子核磁共振(PMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中,每一个结构中的等效氢原子的PMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中的等效氢原子数成正比。现有某有机物,化学式为C6H12。已知该物质可能存在多种结构,a、b、c是其中的三种,请根据下列要求填空:
①a与氢气加成生成2―甲基戊烷,则a的可能结构有___________种。
②b能使溴水和酸性高锰酸钾褪色,PMR谱中只有一个信号,则b的结构简式为:___ __,
其命名为:
③c不能使酸性高锰酸钾溶液褪色,不能与溴水加成褪色,可萃取溴水中的溴;PMR谱中也只有一个信号,则c的结构简式为:___________________________
碳、氢、氧3种元素组成的有机物A,相对分子质量为102,含氢的质量分数为9.8%,分子中氢原子个数为氧的5倍。一定条件下,A与氢气反应生成B,B分子的结构可视为1个碳原子上连接2个甲基和另外2个结构相同的基团。且B的核磁共振氢谱显示有3组不同的峰。
(1)A的分子式是 。
(2)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量相等且生成水的量也相等的是(填序号) 。
A.C5H12O3 B.C4H10 C.C6H10O4 D.C5H10O
(3)①B的结构简式是 。
②A不能发生的反应是(填序号) 。
A.取代反应 B.消去反应 C.酯化反应 D.还原反应
(4)与A互为同分异构体的羧酸有 种。
(5)A还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,其中一种的分子中有2个甲基,该异构体的结构简式是: 。
(1)经元素分析后,发现某烃的含碳量为82.76%,氢的质量分数则为17.24%,且相对分子质量为58,该烃的分子式 。
(2)某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重7.2g,氢氧化钠溶液增重30.8g。推测它的分子式 和结构简式 。
(3)某含氧有机物,它的相对分子质量为46.O,碳的质量分数为52.2%,氢的质量分数为33.0%,NMR中只有一个信号,请写出其结构简式 。
(4)某有机化合物仅由碳、氢、氧三种元素组成 ,经测定其相对分子质量为90 。称取该有机物样品1.8 g ,在足量纯氧中完全燃烧 ,将产物先后通过浓硫酸和碱石灰 ,两者分别增重1.08 g和2.64 g 。该有机物的分子式 。
(8分)填写下列空白:
(1)烃A与含氢量最高的烃B属于同系物。在光照下1体积A最多能与6体积氯气完全反应(同温同压),则A的结构式是 。
(2)烃C的相对分子质量是72,C的一溴代物种数是它的同分异构体中最多的,C的名称是 。
(3)芳香烃D分子中含56个电子,碳与氢元素质量比为12:1,其加聚反应的化学方程式为 。
(4)分子式为C8H10的芳香烃,其苯环上的一氯代物有 种。
两种有机物A和B可以互溶,有关性质如下:
| |
相对密度(20℃) |
熔点 |
沸点 |
溶解性 |
| A |
0.7893 |
-117.3°C |
78.5°C |
与水以任意比混溶 |
| B |
0.7137 |
-116.6°C |
34.5°C |
不溶于水 |
(1)若要除去A和B的混合物中少量的B,可采用_____________(填代号)方法即可得到A。
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液
(2)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下),则该物质的最简式为_____________,若要确定其分子式,是否必需有其它条件_________(填“是”或“否”)。 已知有机物A的质谱、核磁共振氢谱如下图所示,则A的结构简式为_____________。

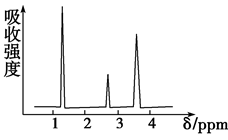
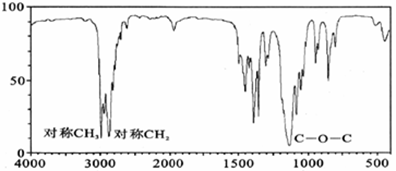
(3)若质谱图显示B的相对分子质量为74,红外光谱如图所示,则B的结构简式为_________________,其官能团的名称为_________________。
(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重19.8g和35.2g。计算混合物中A和B的物质的量之比___________。
(12分)为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1:2:3。
④用红外光谱仪处理该化合物,得到如图三所示图谱。
试回答下列问题:
(1)有机物A的相对分子质量是__________。
(2)有机物A的实验式是____________________。
(3)能否根据A的实验式确定A的分子式______(填“能”或“不能”),若能,则A的分子式是__________(若不能,则此空不填)。
(4)写出有机物A的结构简式______________。
(7分) 某有机物A只含有C、H、O三种元素,常用作有机合成的中间体。现将8.4 g该有机物在14.56L(标况下)O2经充分燃烧后将产生的热气体(无有机物)先通过足量的无水CaCl2固体,发现该固体增重7.2g,然后再将该剩余气体通入足量的澄清石灰水,石灰水增重22.0g;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1。(注:—OH接在不饱和碳上为不稳定结构)
(1)通过计算确定该有机物A的分子式为 ,A的结构简式为 。
(2)有机物B是A的同分异构体,1 mol B可与1mol Br2加成。该有机物所有碳原子在同一个平面,没有顺反异构现象。请写出B的结构简式是 。
为测定某有机化合物A的结构,进行如下实验:
(一)分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下),则该物质中各元素的原子个数比是________。
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为__________,该物质的分子式是________。
(3)根据价键理论,预测A的可能结构并写出结构简式_______________________。
(二)结构式的确定:
(4)核磁共振氢谱能对有机物分子中不同化学环境的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(ClCH2OCH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________。

Ⅰ.有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和粘合剂等高聚物。为研究X的组成与结构,进行了如下实验:
(1)有机物X 的质谱图为: |
(1)有机物X的相对分子质量是__________________。 |
| (2)将10.0 g X在足量O2中充分燃烧,并使其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。 |
(2)有机物X的分子式是 __________________。 |
| (3)经红外光谱测定,有机物X中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3︰1。 |
(3)有机物X的结构简式是 __________________。 |
Ⅱ.Diels-Alder反应为共轭双烯与含有烯键或炔键的化合物相互作用生成六元环状化合物的反应,最简单的反应是: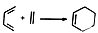 ,
,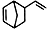 是由A(C5H6)和B经Diels-Alder反应制得。
是由A(C5H6)和B经Diels-Alder反应制得。
(1)Diels-Alder反应属于 反应(填反应类型):A的结构简式为 。
(2)写出与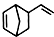 互为同分异构体,且一溴代物只有两种的芳香烃的名称: ;写出生成这两种一溴代物所需要的反应试剂和反应条件: 。
互为同分异构体,且一溴代物只有两种的芳香烃的名称: ;写出生成这两种一溴代物所需要的反应试剂和反应条件: 。
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是(写出计算过程) 。
(2)X与金属钠反应放出氢气,反应的化学方程式是 。
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是 。
(4)X与酸性高锰酸钾溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W。若184 g X和120 g Z反应能生成106 g W,计算该反应的产率(实际产量与理论产量之比) 。
某研究性学习小组做了以下实验:向溴水中加入足量乙醛溶液,观察到溴水褪色的现象。
[提出问题]
产生上述现象的原因是什么?
[提出猜想]
①溴水与乙醛发生取代反应。
②___________________________________________________。
③___________________________________________________。
[设计方案]
方案一:检验褪色后溶液的酸碱性。
方案二:测定反应前溴水中Br2的物质的量和反应后Br-离子的物质的量。
[实验探究]
取含0.005mol Br2的溶液10mL,加入足量乙醛溶液使其褪色,再加入过量AgNO3溶液,过滤、洗涤、干燥后称重固体质量为1.88g。
[解释与结论]
假设测得反应前溴水中Br2的物质的量为a mol,
若测得反应后n(Br-)=0mol,则说明溴水与乙醛发生了____________反应。
若测得反应后n(Br-)=amol,则说明溴水与乙醛发生了____________反应。
若测得反应后n(Br-)=2amol,则说明溴水与乙醛发生了____________反应。
若已知CH3COOAg易溶解于水,试通过计算判断溴水与乙醛发生反应的类型为___________。
理由是_________________________________________ _________________。
其反应方程式为_______________________________________________________。
[反思与评价]
方案一是否可行?__________。理由是_______________________________________。
氢气是清洁的能源,也是重要的化工原料。
(1)以H2为原料制取氨气进而合成CO(NH2)2的反应如下:
N2(g)+3H2(g)=2NH3(g) △H=―92.40 kJ·mol-1
2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=―159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) △H=+72.49 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为 。
(2)用丙烷和水为原料在电催化下制氢气,同时得到一种含有三元环的环氧化合物A,该反应的化学方程式为 。该反应也可生成A的同分异构体——另一种环氧化合物B,B的核磁共振氢谱为下图中的 (填“a”或“b”)。
(3)已知叠氮酸(HN3)不稳定,同时也能与活泼金属反应,反应方程式为:
2HN3=3N2↑+H2↑
2HN3+Zn=Zn(N3)2+H2↑
2 mol HN3与一定量Zn完全反应,在标准状况下生成67.2 L气体,其中N2的物质的量为 。
(4)已知H2S高温热分解制H2的反应为:H2S(g) H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。
H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。
(5)用惰性电极电解煤浆液的方法制H2的反应为:C(s)+2H2O(l)=CO2(g)+2H2(g)现将一定量的1 mol·L-1 H2SO4溶液和适量煤粉充分混合,制成含碳量为0.02 g·mL-1~0.12g·mL-1的煤浆液,置于右图所示装置中进行电解(两电极均为惰性电极)。则A极的电极反应式为 。
能够水解的某有机化合物A经里比希法测得其中含碳为72.0%、含氢为 6.67%,其余含有氧。
现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为150。
方法二:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1∶2∶2∶2∶3。如下图A。
方法三:利用红外光谱仪测得A分子的红外光谱如下图B。
试填空。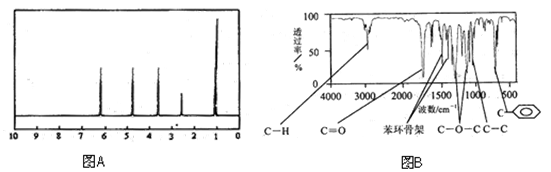
(1)A的分子式为_______________________。
(2)A的分子中只含一个甲基的依据是_______________(填序号)。
a.A的相对分子质量 b.A的分子式
c.A的核磁共振氢谱图 d.A分子的红外光谱图
(3)A的结构简式为 ___________________________ 。
(共8分)
(1)标准状况下,1.68L无色可燃气体在足量氧气中完全燃烧,若将产物通入足量澄清石灰水,得到的白色沉淀质量为15g;若用足量碱石灰吸收燃烧产物,增重9.3g.
①燃烧产物中水的质量为_________ g
②若原气体是单一气体,它的分子式为____________
(2)在100℃时,某有机物蒸汽20ml与60ml氧气混合,点燃后恰好完全反应,生成CO2与水蒸气体积为1:1.5 若将混合气体通过盛浓硫酸的洗气瓶后,气体变为40ml。有机物的分子式为___________
A和B两种有机物可以互溶,有关性质如下:
| |
相对密度(20℃) |
熔点 |
沸点 |
溶解性 |
| A |
0.7137 |
-116.6°C |
34.5°C |
不溶于水 |
| B |
0.7893 |
-117.3°C |
78.5°C |
与水以任意比混溶 |
(1)要除去A和B的混合物中的少量A,可采用_______________方法即可得到B。
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
(2)若B的分子式为C2H6O,核磁共振氢谱表明其分子中有三种化学环境不同的氯原子,强度之比为3︰2︰1。则B的结构简式为__________。
(3)若质谱图显示A的相对分子质量为74,红外光谱如图所示,则A的结构简式为_________________。

(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重14.4g和26.4g。计算混合物中A和B的物质的量之比______________。